



最近,中组部“青年千人计划”专家、南开大学特聘研究员叶萌春课题组利用Ni/Al作双金属催化剂,膦氧化合物SPO化合物作配体,在JACS上报道了咪唑的C-H键与烯烃的对映选择性的外型环化反应,成功地构建了具有β-手性中心的双环或多环咪唑,文章DOI: 10.1021/jacs.8b02547。
氮β位具有手性中心的双环或多环咪唑广泛存在于生物活性分子中。因此,对该结构的高效构建,一直以来是化学家的追求。采用传统的合成方法如缩合或多步合成法,一般很难构建β位的手性中心。在之前的研究中,Bergman和Ellman等人利用C-H键活化的方法,成功地构建了三环咪唑结构,但过程中形成的手性中心位于γ位(图1a),不适于β位手性中心的构建(图1b,式1)。Cavell等从咪唑盐出发,在Ni催化下,实现了咪唑的C-H键与烯烃的分子内外型环化反应(图1b,式2)。受该工作的启发,叶萌春课题组猜想可以采用路易斯酸活化的咪唑作为底物,在Ni催化下实现它与烯烃外型环化的不对称版本(图1b,式3)。
然而,该反应的实现充满着挑战。对该不对称的外型环化反应而言,配体的选择极为重要。近期,一种在空气中稳定存在的二级膦氧(SPO)配体引起了不少课题组的关注。继Hiyama和Nakao报道的Ni/Al双催化的工作后,Cramer等人利用SPO作配体,在Ni/Al双金属催化下,实现了烯烃的不对称氢甲酰胺化反应。在此,叶萌春课题组利用含双叔丁基苯基的二级膦氧化合物Taddol-SPO作配体,实现了咪唑与烯烃的分子内不对称外型环化反应(图1b,式3)。
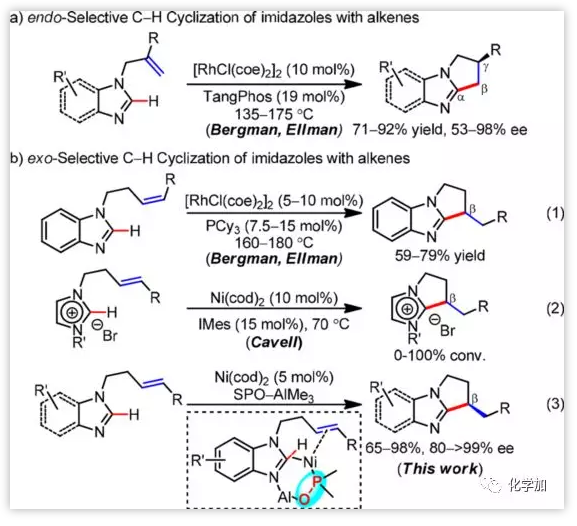
图 1 咪唑的C-H键与烯烃选择性环化反应。图片来源:JACS
对于条件优化,作者研究发现当使用含双叔丁基苯基的二级膦氧化合物Taddol-SPO作配体,5 mol %的Ni(cod)2和20 mol %的AlMe3作为催化剂,反应产率为92%,而ee值高达97%,得最优条件(图 2)。
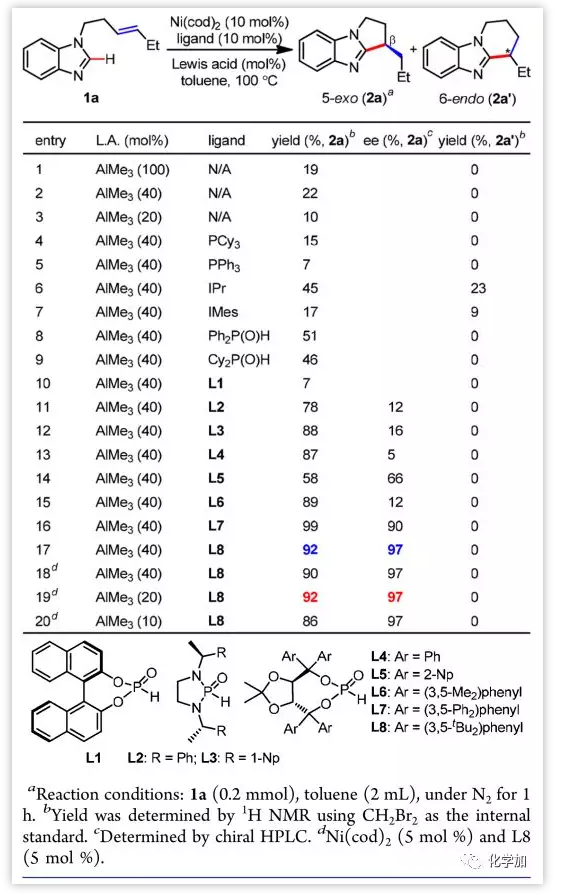
图 2 条件优化。图片来源:JACS
有了最佳条件后,作者扩大了底物的范围。首先,作者考察了不同烯烃的反应情况。从图中可以看出,不同的烯烃结构如端烯,二取代,三取代的烯烃均可以高效地参与反应,反应不仅产率高,并且取得了非常高的ee值(图 3)。此外,Z型和E型的烯烃均能顺利地参与反应,并得到同样的立体构型。
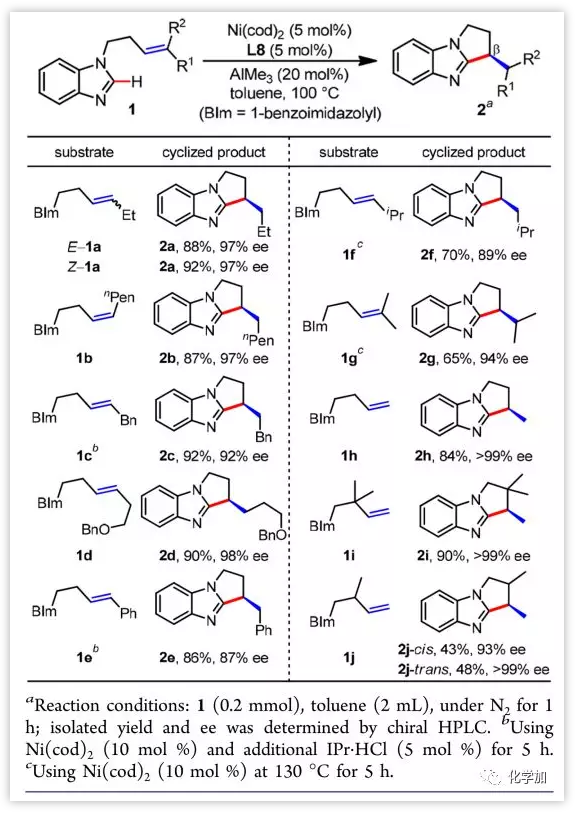
图 3 烯烃的底物范围。图片来源:JACS
此外,作者还考察了咪唑的底物范围。芳环上官能团如OMe、F、Cl、Br、CF3、COOMe等均能得到很好的兼容,反应性和立体选择性也非常好(图 4)。
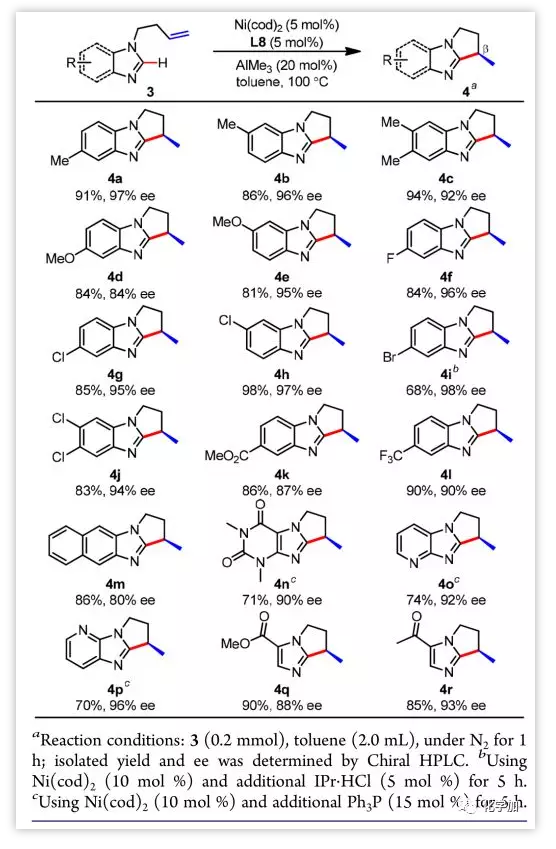
图 4 咪唑的底物范围。图片来源:JACS
为了对反应的机理有一定的认识,作者还做了如下的研究实验(图5):底物d-1h在标准条件下反应得到d-2h,说明对烯烃加成的H源于咪唑的H(图5,式4)。KIE等于1说明了C-H键活化应该不包含在决速步中(图5,式5)。不同底物的竞争实验结果表明该反应是分子内的过程(图5,式6)。同时,作者还通过核磁和当量络合物的转化实验,证明了SPO可同时与Ni和Al配位。过程中,Ni与H和烯烃作用,而Al作为路易斯酸活化咪唑。这些结果表明H作为配体从咪唑向烯烃转移是更加有利的(path a),但也无法排除氧化加成的途径(path b)。
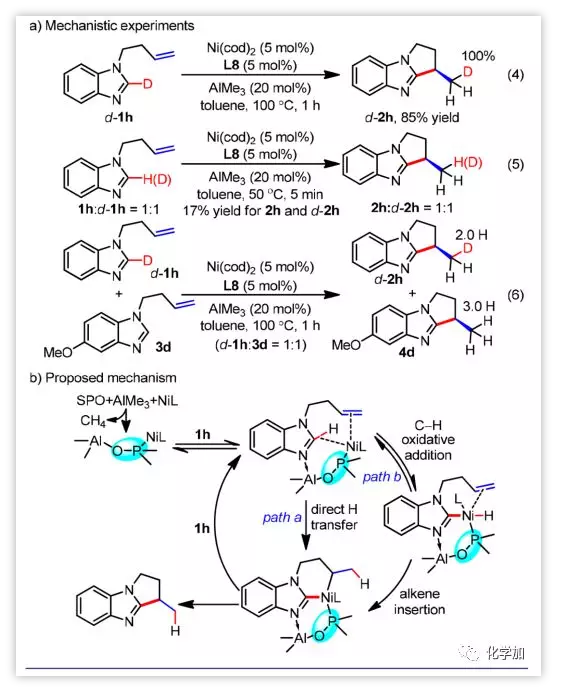
图 5 机理研究。图片来源:JACS
综上所述,叶萌春课题组利用含双叔丁基苯基的二级膦氧化合物Taddol-SPO作配体,实现咪唑与烯烃的分子内不对称外型环化反应。不同结构的烯烃和咪唑均能参与反应,产率高,对映选择性好。鉴于双环和多环咪唑的重要性,该反应具有一定的应用前景。
文章链接: https://pubs.acs.org/doi/10.1021/jacs.8b02547