

正文
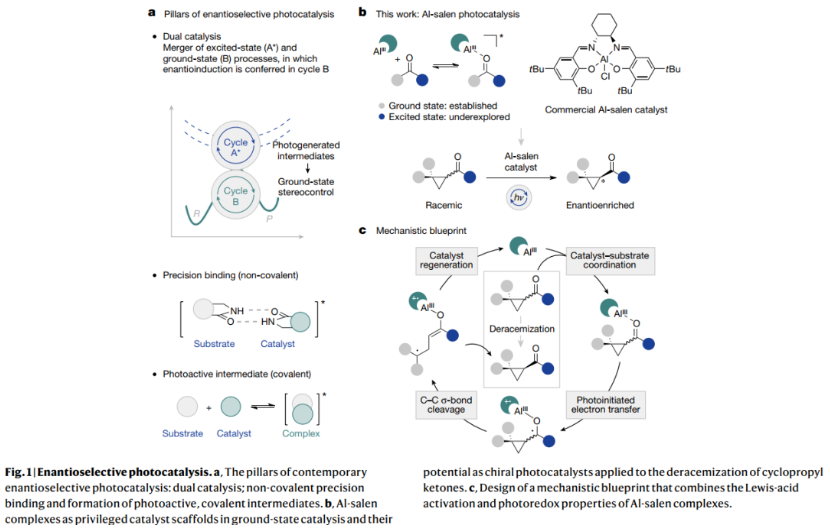
催化剂设计和简化操作平台的进步最终导致了通过不可逆激活模式获取激发电子态的多种方法。这些策略减轻了微观可逆性,并减少了对化学计量试剂和危险操作条件的依赖,从而允许在与敏感环境兼容的温和条件下产生活性物种。生物共轭和细胞图谱中的应用进一步反映了这种复兴在整个科学领域继续享有的广度和影响。尽管这一成功凸显了光催化在形成新键方面的有效性,但活化的非共价性质,加上所产生的中间体的高反应性,使得对映体控制成为一个显著的挑战(Fig.1a)。一种解决途径是双重催化,其中光催化剂与已建立的基态手性催化模式一起工作。对映选择性成键事件通常由涉及光产生中间体的二次光反应发生。 相比之下,使用手性光催化剂直接赋予对映选择性的过程明显不足:这加剧了与识别和开发“特权手性光催化剂”相关的挑战。Bach等人的开创性工作已经确定了源自坎普三酸的内酰胺基骨架在光化学过程中协调对映选择方面的有效性:该蓝图模拟生物识别,其中催化剂和底物中的互补氢键单元确保结构预组织。这种古老的有机催化剂发色团的模块化可以进行调整,以实现带有合适酰胺基团的底物的对映选择性能量转移和单电子转移过程。基于底物的识别单元也已成功用于开发用于对映选择性光催化的手性Ir(III)配合物。Meggers等人的优雅研究表明,酰基咪唑底物与手性 Ir(III) Lewis 酸结合,可实现直接、可见光诱导的不对称氧化还原催化过程。Yoon、Baik等人也令人信服地证明了精确氢键单元在这种情况下的重要性,以实现由手性氢键铱敏化剂控制的对映选择性激发态光反应。 总的来说,这些里程碑表明,当存在互补(氢键)识别单元时,在单一手性光催化剂的支持下可以实现显著水平的对映诱导。扩展该模型以包括具有用于识别的常见官能团的底物是非常有吸引力的,并且最终将导致更通用的手性光催化剂的识别。然而,这项工作的目的是确定可以在激发态模型中复制的基态识别模式。这促使作者探索地球上丰富的铝的强亲氧性,以创建新兴手性蓝图的Lewis酸-Lewis碱组分(Fig.1b)。对这一关键相互作用的进一步信心源于芳基酮的成熟光化学,特别是在Lewis酸活化下。由于在基态催化过程中取得成功,手性Al-salen 催化剂被认为是调节初级和次级光反应的有吸引力的候选者。Lewis酸度、独特的手性配体球和明确的光学性质的结合使得Al-salen配合物成为扩展现有手性光催化剂组合的有希望的候选者。下载化学加APP到你手机,更加方便,更多收获。
图片来源:Nature
为了验证salen光催化的概念,设想了环丙烷的去消旋化(Fig. 1b):这源于作者对光催化烯烃异构化的兴趣、烯烃π-系统和环丙基沃尔什轨道之间的反应性相似性以及与实现诱导相关的历史性挑战。通过相邻的低位反键轨道激活环丙烷的能力使得环丙基酮作为这一努力的底物特别有吸引力。这一转变将有助于人们对使用低分子量光催化剂进行光驱动小分子去消旋化的兴趣日益增长。对于这一不断增长的库,预计手性Al-salen配合物可以通过电子转移到羰基来有效地用于环丙基酮的去消旋化:这将通过底物配位和随后配体发色团的激发,然后是手性环境中的电子转移来实现(Fig.1c)。
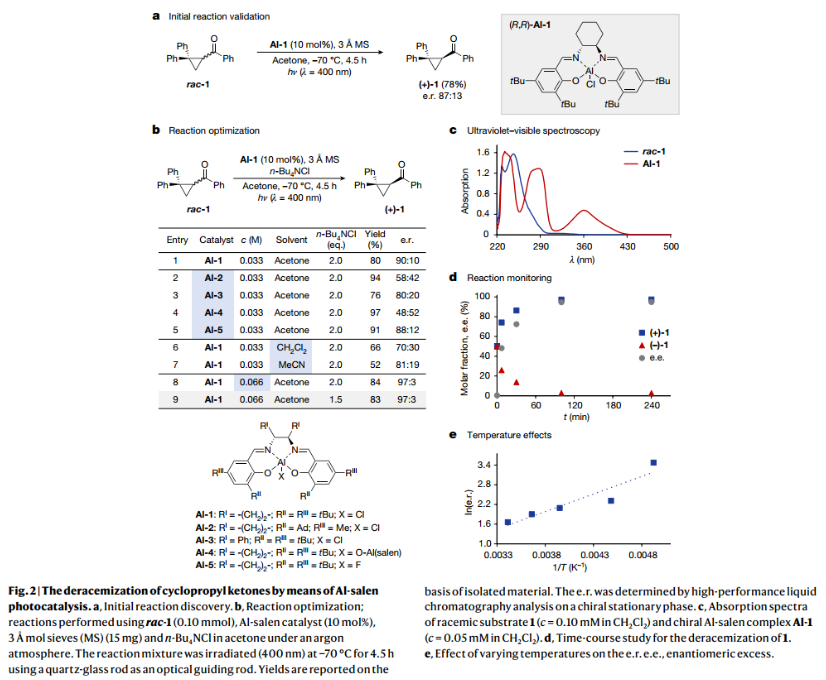
首先,作者在-70 °C下使用商业可得的Al-salen配合物Al-1,丙酮作溶剂研究了环丙烷rac-1的催化去消旋作用,对反应条件进行了筛选和优化(Fig.2a)。得到的最佳条件为:商业催化剂Al-1为最佳催化剂,丙酮为最佳溶剂,c = 0.066 M为最佳浓度,n-Bu4Cl为添加剂,-70 °C下反应6 h。
图片来源:Nature
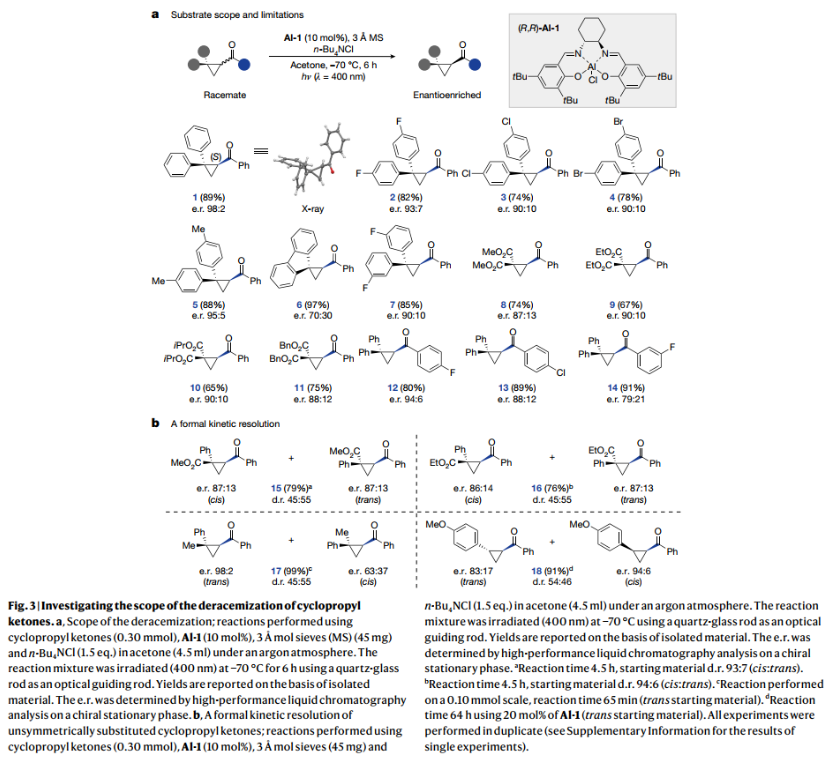
接着,作者研究了该反应的底物范围(Fig.3a),对位取代底物(1-5)具有高产率和高对映选择性,,er为 90:10-98:2,1的单晶确定其绝对构型为(S)。高张力的环丙烷6选择性显著下降(er 70:30)。间位取代的7的产率为85%,er为90:10。对位取代基的化合物12 (p-F)和13 (p-Cl)的产率分别为80%和89%,er分别为 94:6和88:12。对于非对称取代的环丙烷(Fig.3b),在催化剂Al-1条件下,在低温下照射偕Ph/酯底物15和16得到了光稳定组合物,并且两种非对映异构体占比几乎相等。作者还研究了反式二取代环丙烷18的反应性,形成顺式非对映体(er 94:6)的同时,还对映选择性的形成了反式异构体,er为 83:17。
图片来源:Nature
图片来源:Nature
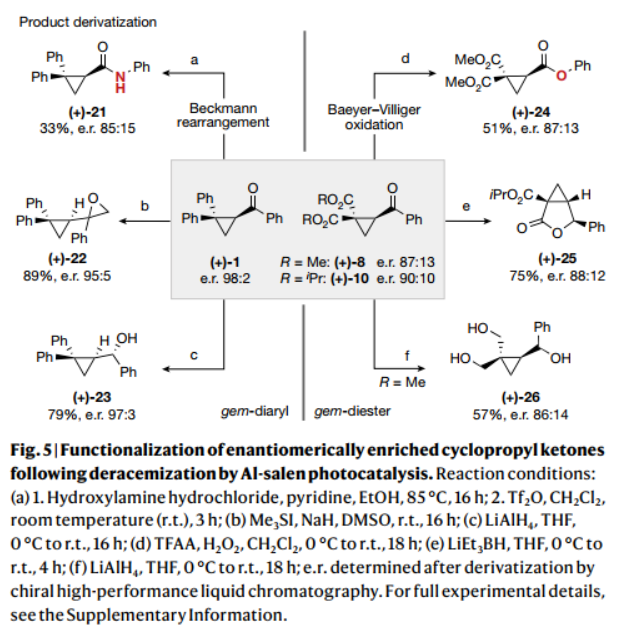
为了证明该方法的合成效用,作者对偕二芳基和偕二酯衍生物(+)-1和 (+)-8/(+)-10进行了进一步的衍生化(Fig.5)。通过Beckmann重排或Baeyer-Villiger氧化可直接转化为酰胺(+)-21或酯(+)-24。(+)-1的Johnson-Corey-Chaykovsky环氧化和氢化铝锂还原,分别生成(+)-22和(+)-23,以完全非对映选择性的方式进行,三乙基硼氢化锂条件下还原/内酯化序列,获得稠合内酯衍生物(+)-25。(+)-8的还原能够在不损害光学纯度的情况下得到三醇(+)-26。
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn