

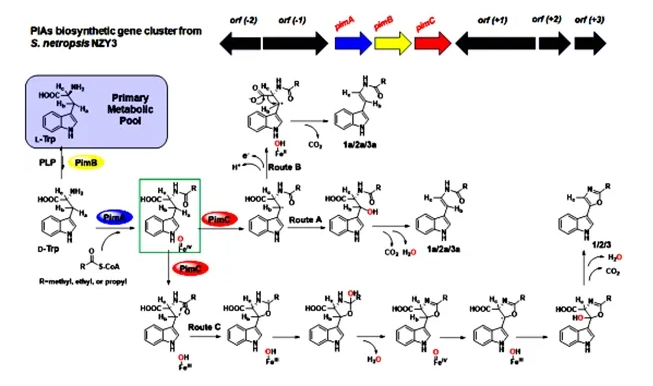
吲哚噁唑环存在于多种天然产物及其化学衍生物的结构中,含有该药效团的化合物普遍显示出优异的生物学和药学活性,如抗肿瘤、抗肠道病毒、抗血栓形成、抗癫痫、抗植物病毒、抗植物致病真菌、抗农业害虫、除草等,在疾病治疗和农业保护等领域均具有重要的应用价值。作为一类广泛被重视和关注的药效团,虽然噁唑啉环或噁唑环在天然产物中的多样化生物合成方式被广泛报道,然而除了假单胞菌来源的labradorins(Angew. Chem. Int. Ed.,2021)以外,大多数吲哚噁唑类化合物的生物合成方式仍然尚未阐明,很大限制了人们对吲哚噁唑生物合成方式的科学认知,并成为该类化合物走向绿色规模化应用的一个关键瓶颈问题。Pimprinines类化合物是链霉菌代谢产生的一类结构多样并且生物活性显著的吲哚噁唑生物碱,然而其生物合成机制一直悬而未决。该团队通过同位素标记、生物信息学分析、基因组挖掘、基因簇异源表达、基因敲除与回补以及前体的体内生物转化与定量检测等多种策略,成功定位到链霉菌NZY3中pimprinines生物合成基因簇。通过蛋白表达纯化、酶功能的生物化学表征、产物有机结构波谱解析、体外一锅法等多种策略,阐明了PimB是一种新型的PLP依赖的色氨酸消旋酶催化D-色氨酸的形成,扮演了合成途径“守门人”的角色,PimA是一种特殊的D-色氨酸-N-酰基转移酶,而PimC是目前唯一一种催化N-酰基-D-色氨酸产生吲哚噁唑药效团的α-酮戊二酸/FeII依赖的双加氧酶,揭示出一条前所未见的D-构型底物顺次导向的精准分子装配线。与假单胞菌不同,这种以D型氨基酸作为途径开关的方式体现了链霉菌次级代谢调控的复杂性和精密性。进一步,通过PimC关键残基的点突变与生化表征、同位素标记与质谱追踪等技术手段,该研究证实吲哚噁唑环的形成采用一种自由基重排与环缩合的方式发生,同时伴随着脱水和脱羧基反应。此外,PimC还可以通过经典的“羟基回弹”机制或“β正离子”机制,产生含有反式双键的代谢副产物,显示出催化功能的多样化。鉴于pimprinines重要的医用和农用价值,该研究不仅为吲哚噁唑类天然产物的生物合成机制研究提供新的科学理论见解,也为进一步深入开展该类高附加值生物碱的合成生物学研究提供了新颖的酶工具元件,为实现pimprinines及其类似物的大规模生产奠定了坚实的理论和物质基础。
该研究的实施得到了国家自然科学基金和陕西省科技创新团队等多个项目资助。
原文链接:https://pubs.acs.org/doi/10.1021/jacs.5c01705
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn