

正文
氮杂环丙烷具有较大的环张力,是现代有机合成中重要的合成砌块,其开环反应可高效构建氨基酸、杂环化合物及生物碱等重要骨架。2-烷基取代氮杂环丙烷在亲核开环和传统过渡金属催化条件下,倾向于断裂位阻较小的Ca-N键生成直链产物;而2-苯基和2-乙烯基取代衍生物则更易断裂位阻较大的苄基(Cb-N)或烯丙基(Cb-N)键,选择性地形成支链产物(Figure 1a)。为突破底物依赖的选择性限制,兰州大学王刚伟课题组利用路易斯酸辅助,碘负离子介导的可逆、非区域选择性氮杂环丙烷开环,生成β-胺基碘化物I和II。随后Ni催化剂对两种β-胺基碘化物(I和II)进行区分:即Ni与二级的β-胺基碘化物II反应速率更快,形成更稳定的仲/叔自由基IV。与此同时,中间体I转化成一级自由基III的速率慢于其可逆关环生成氮杂环丙烷的速率。根据Curtin-Hammett规则,反应能够高选择性地生成1,3-自由基阴离子中间体IV。通过该策略,实现催化剂控制的氮杂环丙烷与2-芳基-1,3-二烯自由基-极性交叉环加成,构建氮杂环庚烷(J. Am. Chem. Soc. 2025, 147, 2675-2688)。近日,该团队基于此策略实现大位阻动态动力学开环烷基Heck偶联反应、脱氟烷基化反应以及通过链行走实现的远端去饱和化反应(Figure 1d)。
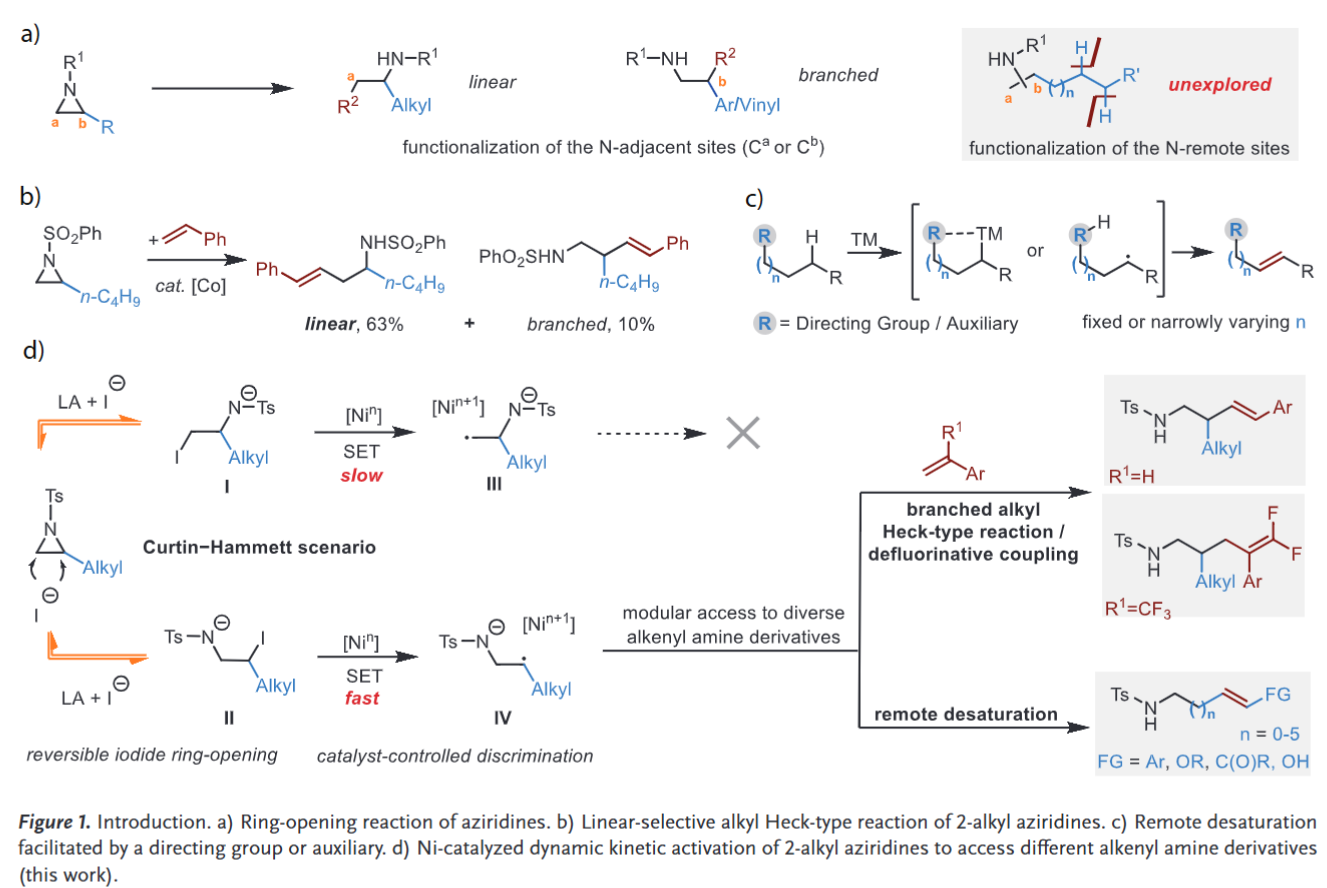
(图片来源 Angew. Chem. Int. Ed.)
作者以2-苯乙基-1-甲苯磺酰基氮杂环丙烷1a和1-甲氧基-4-乙烯基苯2a作为模型底物进行了反应条件优化。经过系统筛选,确定以溴化镍为催化剂、dppp为配体、碘化钾为碘源、DMF为溶剂在50 oC下反应48小时为最优条件。值得注意的是,机理研究表明在烷基Heck反应过程中,氮杂环丙烷开环产生的NTs阴离子可能作为碱来促进Ni-H中间体的还原消除以促进镍催化剂的催化循环。
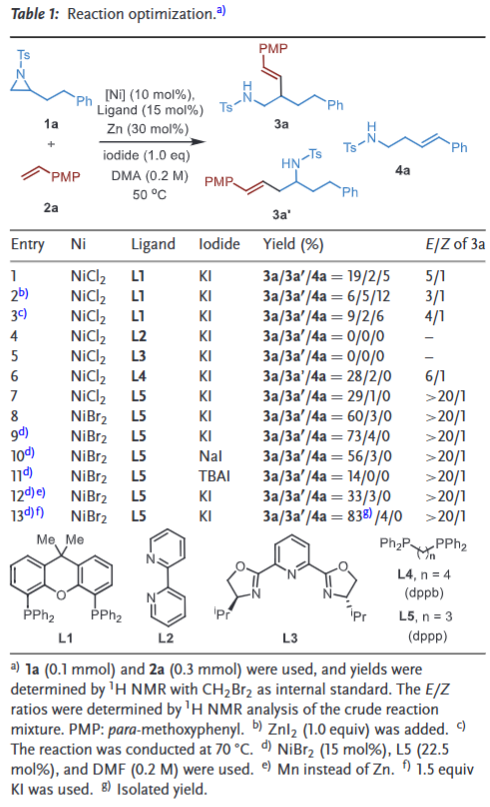
(图片来源 Angew. Chem. Int. Ed.)
在最优条件下,作者对烷基Heck反应进行底物普适性考察(Scheme 1),结果表明该反应具有中等至良好的官能团兼容性和区域选择性,但对非活化脂肪族烯烃及α,β-不饱和烯烃的转化仍存在局限性。
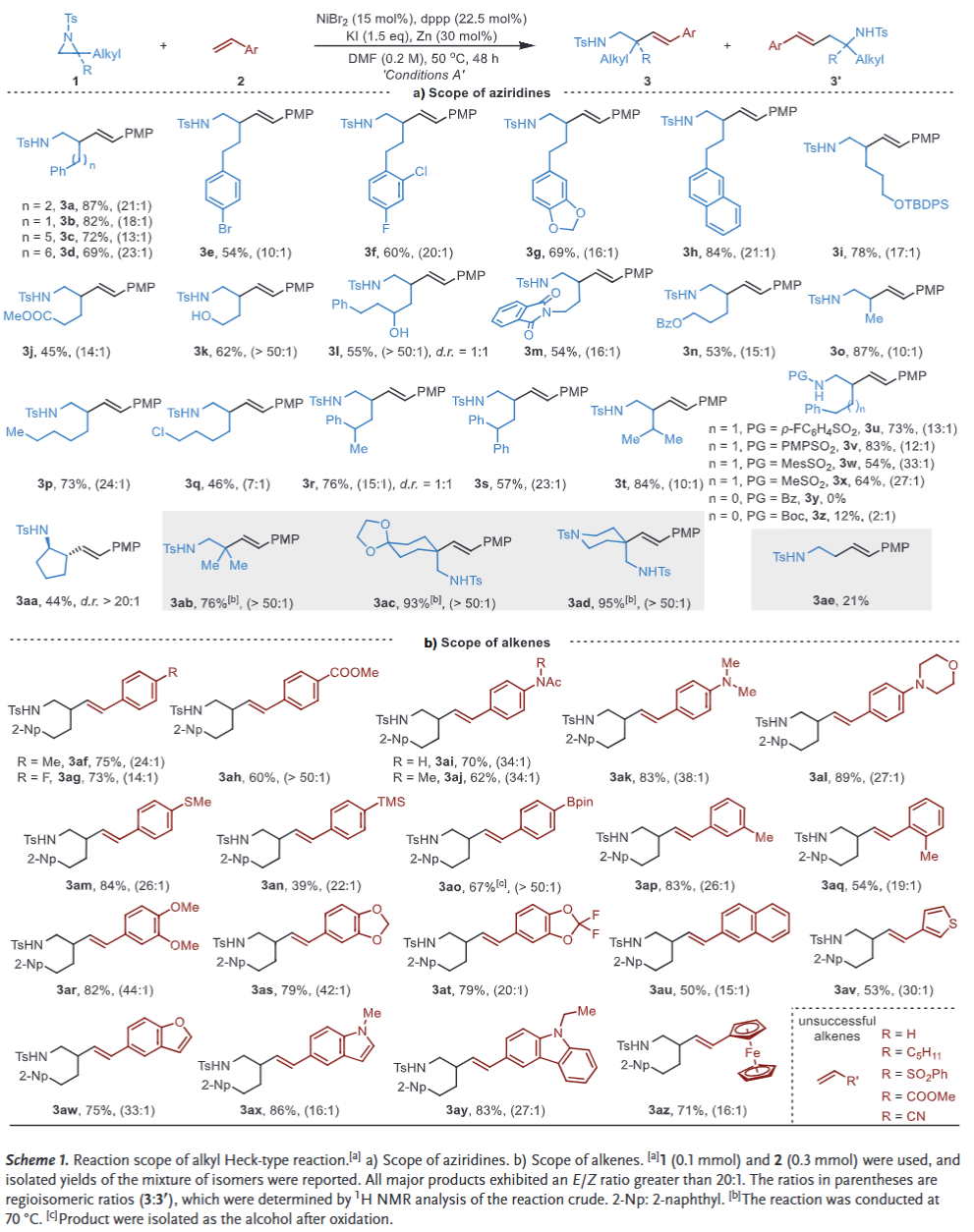
(图片来源 Angew. Chem. Int. Ed.)
偕二氟烯烃作为羰基化合物的理想生物电子等排体,在药物化学中具有重要价值。本研究发展了一种三氟甲基烯烃与2-烷基氮杂环丙烷的脱氟偶联策略,高效构建了一系列结构新颖的支链偕二氟双高烯丙基胺衍生物(Scheme 2)。该反应表现出中等至良好的产率(up to 87%)和区域选择性,并成功实现了产物向单氟四氢吡啶化合物的转化。
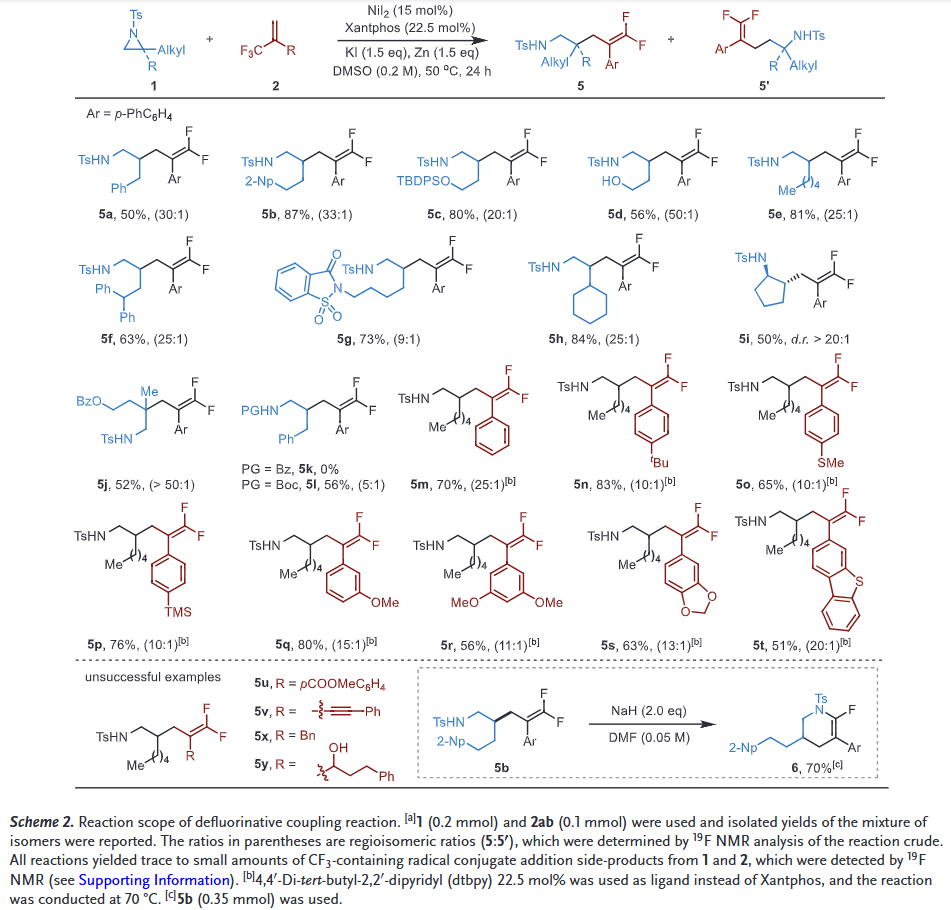
(图片来源 Angew. Chem. Int. Ed.)
经过系统的条件优化,该远程去饱和化反应展现出优异的立体选择性和区域选择性,产物E/Z比大于20:1,且未检测到其他位置异构体。进一步的底物适用性研究表明:1)含供电子或吸电子取代基的芳基氮杂环丙烷均能顺利转化;2)末端烷基链上的硅醚(-OTBDPS)、酯基(-CO2R)、羟基(-OH)以及非末端羟基等官能团均具有良好的耐受性,可顺利转化为相应的烯基胺类化合物。
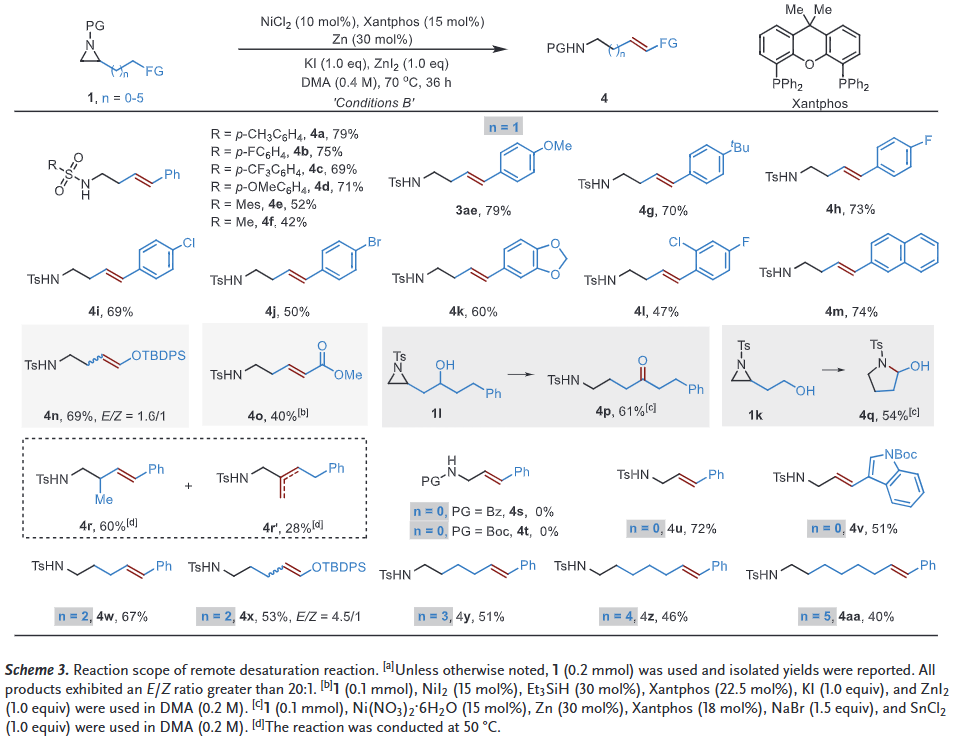
(图片来源 Angew. Chem. Int. Ed.)
为了验证该方法合成应用价值,作者将支链选择性烷基Heck型反应拓展至复杂分子(Figure 2),各类药物分子均能高效转化为高烯丙胺衍生物。在放大实验中,1aq 的远端去饱和化反应保持同等效率,该产物可作为关键前体,通过已知转化策略构建多种氮杂环(Figure 2b)。底物 1h 在1.0 mmol规模下同时实现远程去饱和与Heck型反应,产物 4m 和 3h 经相同条件卤代酰胺化,可分别高效构建二取代和三取代吡咯骨架(Figure 2c)。此外,由高烯丙醇衍生的氮杂环丙烷1k与1-氟-4-乙烯基苯2c反应获得的烷基Heck型产物9,可作为合成脂肪酸酰胺水解酶(FAAH)抑制剂的关键中间体(Figure 2d)。
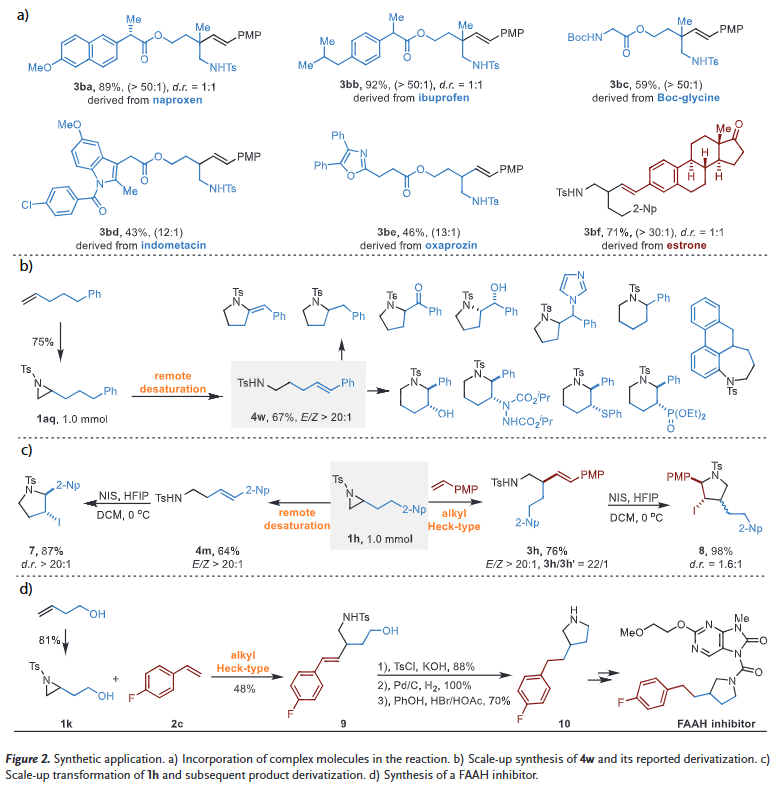
(图片来源 Angew. Chem. Int. Ed.)
本研究通过系列对照实验深入探究了烷基Heck型反应的机理(Figure 3)。烷基heck反应中,原位生成的ZnI₂与KI共同介导了的氮杂环丙烷1a可逆碘开环过程(Figure 3a,详见支持信息)。交叉实验显示:由1a位阻较小C-N键开环得到的β-碘胺11和1g与2a反应时,同时生成大位阻Heck偶联产物3a和3g(Figure 3b);β-碘胺12参与反应时也观察到相同现象(Figure 3c)。这些结果证实反应先经过非区域选择性的可逆碘开环步骤,再通过催化剂控制实现高区域选择性。值得注意的是,手性底物1a(ee>98%)部分转化时得到外消旋产物3a(Figure 3d),该现象提示反应可能涉及自由基中间体,但回收的1a仍保持原有对映体纯度,这与Doyle报道的Ti催化自由基开环导致立体消旋的结果明显不同。氘代实验进一步显示:deuterio-2a与1a反应时,产物deuterio-3a的C-3和C-4位均出现氘掺入(Figure 3e);当deuterio-2a与2g等摩尔混合后与1h反应,产物同样在C-3/C-4位显示氘掺入(Figure 3f)。这些结果表明Ni-H物种的β-氢消除及其NTs阴离子的再生是可逆过程。关键机理研究表明:氮杂环丙烷开环产生的NTs阴离子可能作为碱促进Ni-H中间体的还原消除,进而推动镍催化循环。实验证据包括:(1)β-碘胺11/12与2a反应几乎不生成目标产物(Figure 3g)(2)直接将烷基碘化物13与2a反应,产率仅有5%,但是将13加入1a与2a反应8小时后的体系,产物14产率提升至24%(Figure 3h)。结合Figure 3b-c结果,证实NTs阴离子在促进Ni催化剂周转中起关键作用:既作为碱加速Ni-H物种还原消除,又作为质子受体参与产物NHTs结构的形成。
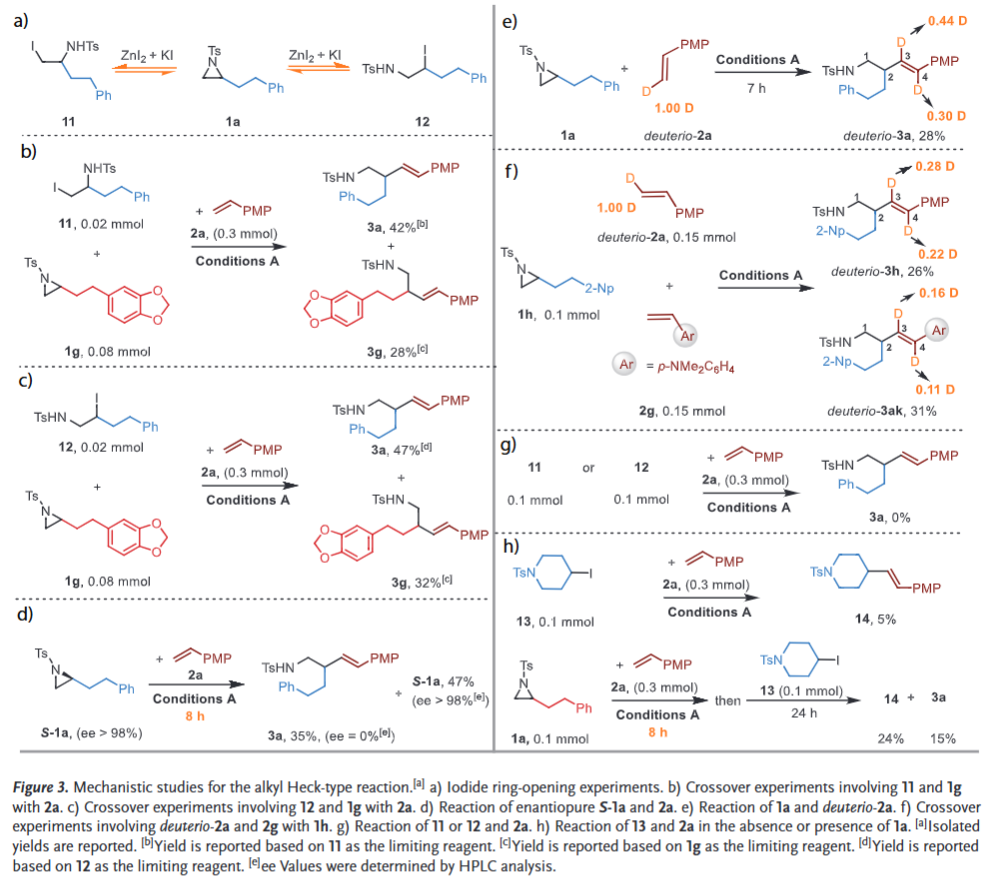
(图片来源 Angew. Chem. Int. Ed.)
本研究对远程去饱和反应机理进行了系统探究(Figure 4)。交叉实验(Figure 4a-b)证实该反应同样存在氮杂环丙烷的动态动力学活化过程。通过PBN(苯基叔丁基硝酮)自由基捕获剂进行的EPR实验(Figure 4c),成功通过高分辨质谱和EPR谱检测到烷基自由基加合物,确证了自由基中间体的存在。值得注意的是,底物1ax未能发生远程去饱和(Figure 4d),排除了1,n-氢原子转移(HAT)的反应路径。氘代实验深入揭示了远程烯烃结构的形成机制:不同位点氘代的底物deuterio-1a和deuterio-1h反应时(Figure 4e-f),产物deuterio-4a和deuterio-4m均在C-2、C-3和C-4位出现氘掺入,而C-1位未检测到氘信号。结合以上实验及反应过程监测(Figure 4h),作者得出以下结论: [Ni(n+2)]-烷基物种通过可逆的β-氢消除/迁移插入实现链行走过程,产物4或其NTs阴离子的形成是可逆的,以及在链行走过程中 [Ni(n+2)]-H物种会与烯烃配位,并发生可逆的解离-再插入。而本体系通过使用大位阻双齿膦配体Xantphos(区别于常规平面双齿吡啶型配体),协同氮杂环丙烷开环产生的NTs阴离子(作为碱),成功促进了[Ni(n+2)]-H物种的还原消除,打破了β-氢消除与烯烃再插入的平衡,实现了"自终止"的链行走过程。该机制同样适用于解释烷基Heck型反应中dppp配体的促进作用。这种新型远程去饱和策略不仅弥补了导向基团辅助方法的局限性(Figure 1c),还能灵活构建不同链长的烯基胺类化合物。
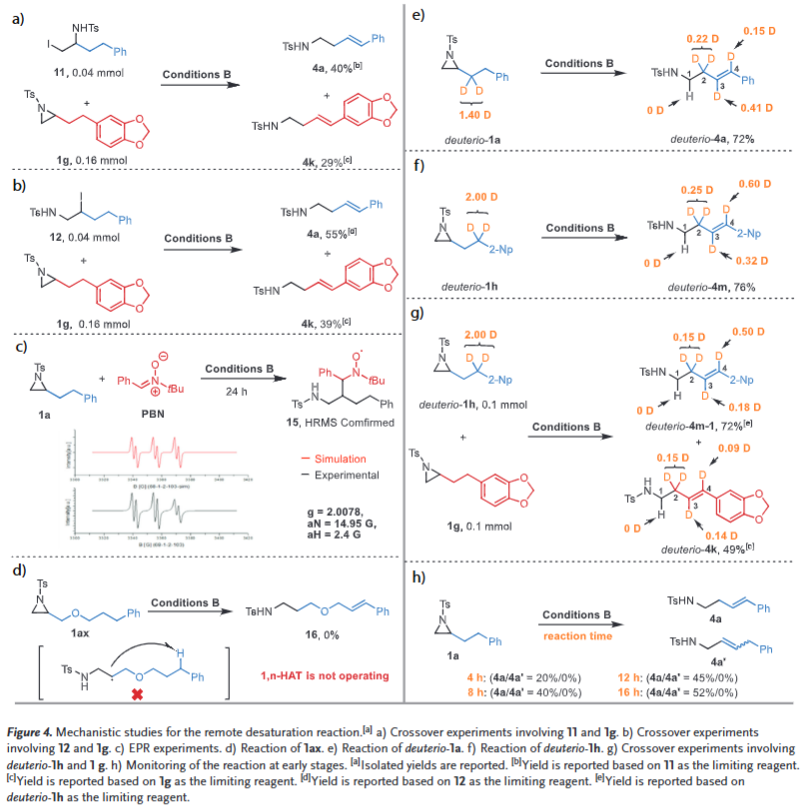
(图片来源 Angew. Chem. Int. Ed.)
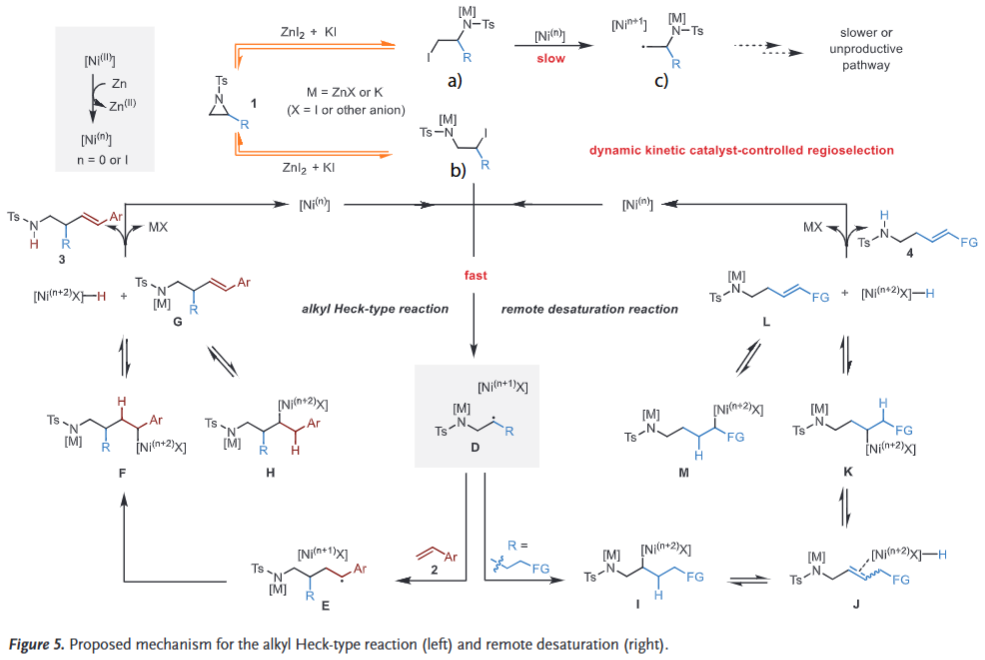
基于实验结果,作者提出了2-烷基氮杂环丙烷烷基Heck型偶联和远程去饱和反应的可能机理(Figure 5)。反应起始于锌粉还原[Ni(II)]生成低价[Ni(n)](n = 0或I),同时Zn(II)与KI协同促进氮杂环丙烷的可逆非选择性碘代开环,生成β-碘代胺A和B。随后[Ni(n)]优先与位阻较大的B发生单电子转移(SET),形成更稳定的仲碳自由基D,而伯碳自由基C因闭环速率快于SET而重新转化为B。
在Heck型反应中,自由基D与苯乙烯2加成得到E,进而与[Ni(n+1)X]结合形成F。F经历β-氢消除产生[Ni(n+2)X]-H和NTs阴离子G(对应产物3),后者通过[Ni(n+2)X]-H的可逆插入与F、H形成平衡。NTs阴离子作为碱促进[Ni(n+2)X]-H的还原消除,生成NHTs单元并再生[Ni(n)],完成催化循环。
对于远程去饱和过程,自由基D与[Ni(n+1)X]形成I,通过连续的β-氢消除/迁移插入实现链行走,最终建立K、M、[Ni(n+2)X]-H与NTs阴离子L的平衡体系。Xantphos配体和NTs阴离子协同促进[Ni(n+2)X]-H的不可逆还原消除,生成产物4并完成催化循环。
(图片来源 Angew. Chem. Int. Ed.)
总结
综上所述,兰州大学王刚伟团队通过动态动力学活化2-烷基氮杂环丙烷实现区域选择性烷基Heck偶联反应、脱氟烷基化反应以及通过链行走实现的远端去饱和化反应,为一系列烯基胺化合物的构建提供方法学基础。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn