

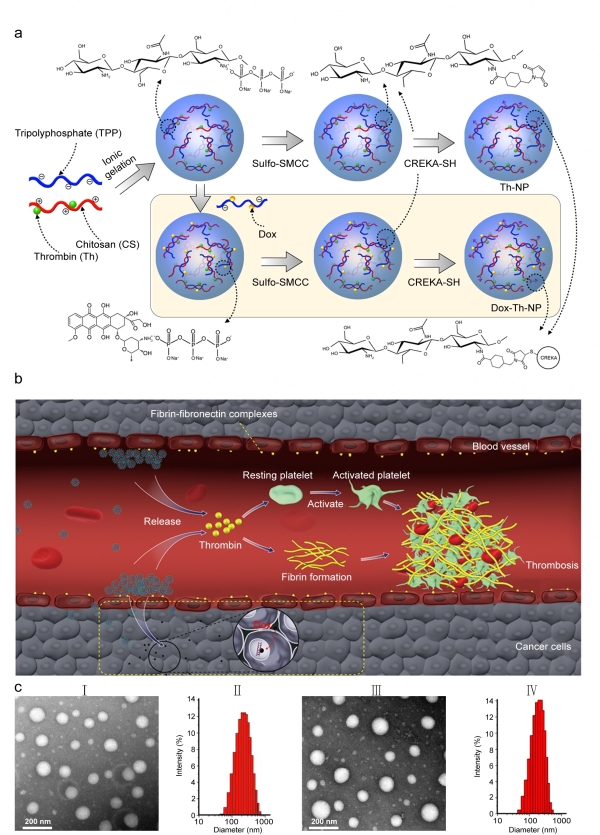
图 1. 负载促凝因子凝血酶和化疗药物的纳米载体设计及工作机理
2020年6月22日,国家纳米科学中心聂广军研究员、吴雁研究员和赵宇亮院士团队合作在Nature Biomedical Engineering 杂志上在线发表了研究论文Combination of tumour-infarction therapy and chemotherapy via the co-delivery of doxorubicin and thrombin encapsulated in tumour-targeted nanoparticles (https://doi.org/10.1038/s41551-020-0573-2)。通过智能纳米药物负载促凝因子和化疗药物,实现特异性靶向栓塞肿瘤血管的同时,促进化疗药物同步富集到无血供或不依赖血管生长的肿瘤边缘区域,有效提高血管栓塞疗法的治疗效果(图 1)。该研究为开发新型的抗肿瘤血管药物提供新思路,同时对提高临床已有栓塞疗法疗效的方案设计具有指导意义。本论文第一作者为李素萍研究员、张银龙博士。
肿瘤血管栓塞疗法是通过在已形成的肿瘤血管内形成血栓,阻断肿瘤血液供应,使肿瘤细胞因缺乏营养和氧气,而饥饿坏死的一种治疗方法。对于临床上大多数癌症患者而言,抗肿瘤治疗所针对的多是已经血管化的肿瘤。因此,肿瘤血管栓塞疗法呈现出广谱高效的临床应用前景。然而,迄今为止寻找安全而有效的血管栓塞疗法仍然是该研究领域的一个“瓶颈”问题。自2011年开始,聂广军研究员团队在智能纳米药物调控肿瘤微环境中血管系统方面开展了系列研究工作。
针对以上科学挑战,在赵宇亮院士的支持和指导下,李素萍、丁宝全和聂广军等合作发展了一种新型DNA纳米机器人,将凝血酶装载到其内部,实现了凝血酶在肿瘤组织中的精确定位、可控暴露,选择性诱导肿瘤血管栓塞,有效 “饿死”肿瘤的科学目的(Nature Biotechnology,2018, 3, 258-264)。该研究工作革新了肿瘤血管栓塞治疗手段。DNA纳米机器人代表了未来人类精准药物设计的全新模式,为恶性肿瘤等疾病的治疗提供全新的智能化策略。
另一方面,肿瘤血管内的血小板通过分泌颗粒内含物和/或直接粘附到血管内皮表面,保护血管的完整性,血小板这一特殊功能阻止了药物在瘤内的跨内皮渗透,限制了疗效。针对该科学问题,聂广军和李素萍等合作发展了一种靶向清除肿瘤局部血小板的聚合物纳米药物,定点清除肿瘤局部血小板,扩大血管内皮间隙,从而提高化疗药物的瘤内富集(Nature Biomedical Engineering,2017, 1, 667-679)。该工作提供了一种具有普适性的增加肿瘤血管内皮通透性的新技术,可用于化疗/小分子药物的增效减毒。
研究团队近期受邀,针对智能纳米药物调控肿瘤血管微环境,在Accounts of Chemical Research,2019, 52, 2703-2712; Medicinal Research Review, 2020, 40, 1084-1102和Trends in Biotechnology,2019, 6, 573-577等撰写了综述和评述文章,系统总结了肿瘤微环境血管系统的最新进展和挑战。
以上系列研究工作得到了科技部重点研发计划纳米科技专项、中科院先导专项B、国家自然科学基金重点项目和创新群体等项目支持。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn