

α-手性环状胺不仅是众多天然产物的基本结构单元,而且在合成化学、药物发现和催化剂设计等领域都有着广泛的应用。为此,人们发展了多种方法来构建此类骨架。然而,利用不对称碳氢键活化直接实现环状胺α-位的官能团化反应依然存在较大挑战。
中国科学院兰州化学物理研究所羰基合成与选择氧化国家重点实验室徐森苗团队一直致力于过渡金属催化的区域和立体选择性硼化反应研究(Org. Lett. 2017, 19, 3676; Chem. Sci. 2018, 9, 5855;J. Am. Chem. Soc. 2019, 141, 5334; Angew. Chem. Int. Ed. 2019, 58, 8187;J. Am. Chem. Soc. 2019, 141, 10599; Org. Lett. 2020, 22, 2861; Chin. J. Chem. 2020, doi.org/10.1002/cjoc.202000240)。尤其是在不对称碳氢键硼化方面,他们发展了一类新型的手性双齿硼基配体(CBL)并首次实现了配位基团导向的二芳基甲基胺的C(sp2)-H键(J. Am. Chem. Soc. 2019, 141, 5334)、环丙烷的C(sp2)-H键(J. Am. Chem. Soc. 2019, 141, 10599)和环丁烷的C(sp2)-H键的不对称硼化(Chin. J. Chem. 2020, doi.org/10.1002/cjoc.202000240)。
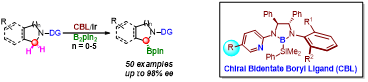
图一、CBL/Ir催化的环状胺的不对称碳氢键硼化反应
最近,他们通过改造的CBL,实现了环状胺类化合物的高区域和立体选择性的α-C(sp3)-H键硼化反应,产物的最高ee值可达98%(图一),并实现了生物活性分子(+)-Calycotomine的对映选择性合成。值得一提的是,在四氢异喹啉类底物的反应中,硼化反应专一性地发生在C1位,这与从文献已知的碳氢键活化方法形成互补。利用该方法,该团队也实现了一系列含有生物活性分子的环状胺类化合物的后期碳氢键硼化反应(图二)。
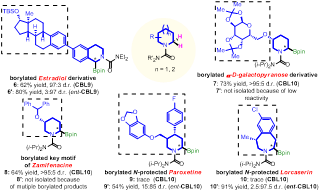
图二、CBL/Ir催化的连有生物活性分子结构的环状胺的后期碳氢键硼化
相关成果在线发表在J. Am. Chem. Soc. (论文链接:https://pubs.acs.org/doi/pdf/10.1021/jacs.0c06756)上。以上工作得到了国家自然科学院基金、江苏省自然科学基金、兰州化物所、羰基合成与选择氧化国家重点实验室和杭州师范大学有机硅化学及材料技术教育部重点实验室的支持。研究助理陈莉莉博士和博士研究生杨玉环为该工作的共同一作。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn