

(图片来源:J. Am. Chem. Soc.)
正文
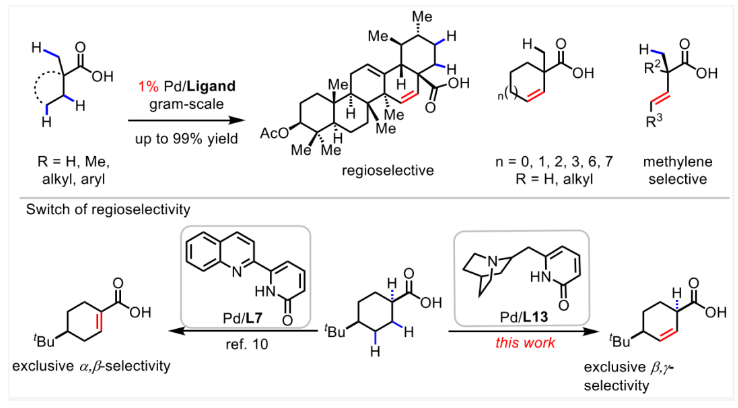
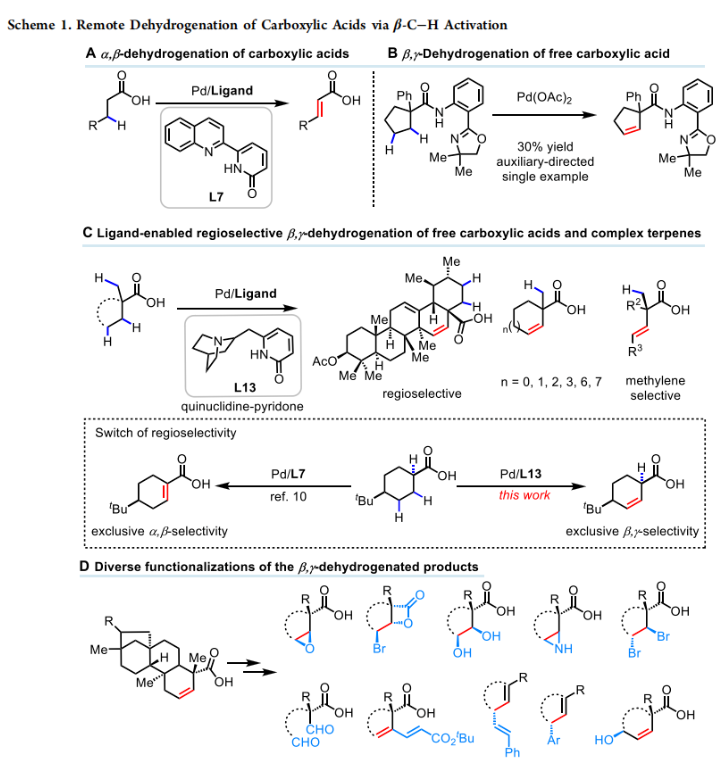
脂肪族化合物的去饱和是现代有机化学中一种广泛使用的合成转化。尽管目前化学家们在羰基化合物(如醛、酮、酯、酰胺以及羧酸等)的α,β-去饱和方面取得了重大进展,但实现羰基化合物的β,γ-去饱和仍是一个尚未解决的问题(Scheme 1A)。2008年,余金权课题组首次利用双噁唑啉酰胺导向,实现了环戊基羧酸的β,γ-去饱和,但仅有一个例子且产率仅为30%(Scheme 1B)。最近,美国斯克里普斯研究所余金权课题组利用最近发展的两类双齿配体(quinuclidine-pyridone和pyridine-pyridone),在钯催化下实现了游离羧酸的β,γ-脱氢烯基化(Scheme 1C)。值得注意的是,一系列具有重要生物学意义的天然产物也可以经历β,γ-脱氢生成远端烯烃,从而通过进一步的衍生化将环氧化物和β-内酯引入到复杂天然产物骨架中(Scheme 1D)。
(图片来源:J. Am. Chem. Soc.)
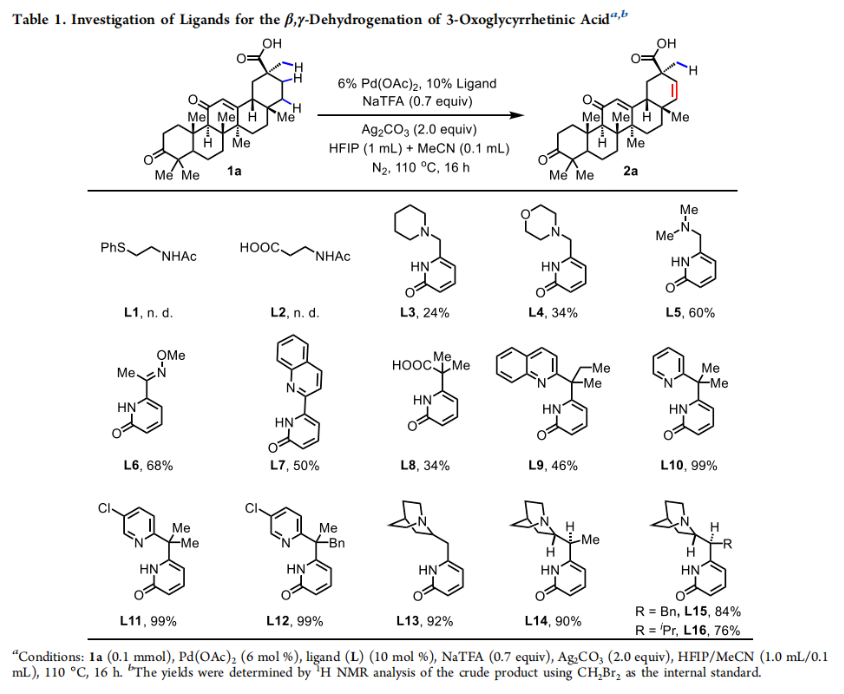
含有羧酸的萜烯类天然产物可用于预防和治疗多种疾病,并表现出多种生物活性,如抗病毒、抗癌和抗炎特性等。因此,在这些天然产物中引入β,γ-双键将为后续实现远端γ-位的官能团化提供多种可能性。作者选择三萜类化合物3-羰基甘草次酸(3-oxoglycyrrhetinic acid)1a作为模板底物对反应条件进行了优化(Table 1)。通过对一系列条件进行筛选,作者发现当使用1a (0.1 mmol), Pd(OAc)2 (6 mol%), L10 (10 mol%), NaTFA (0.7 equiv), Ag2CO3 (2.0 equiv), 在HFIP/MeCN (1 mL/0.1 mL)中N2氛围下110 °C反应16 h可以以99%的产率得到β,γ-去饱和产物2。其中,配体和混合溶剂(HFIP/MeCN)的使用是实现此过程的关键。
(图片来源:J. Am. Chem. Soc.)
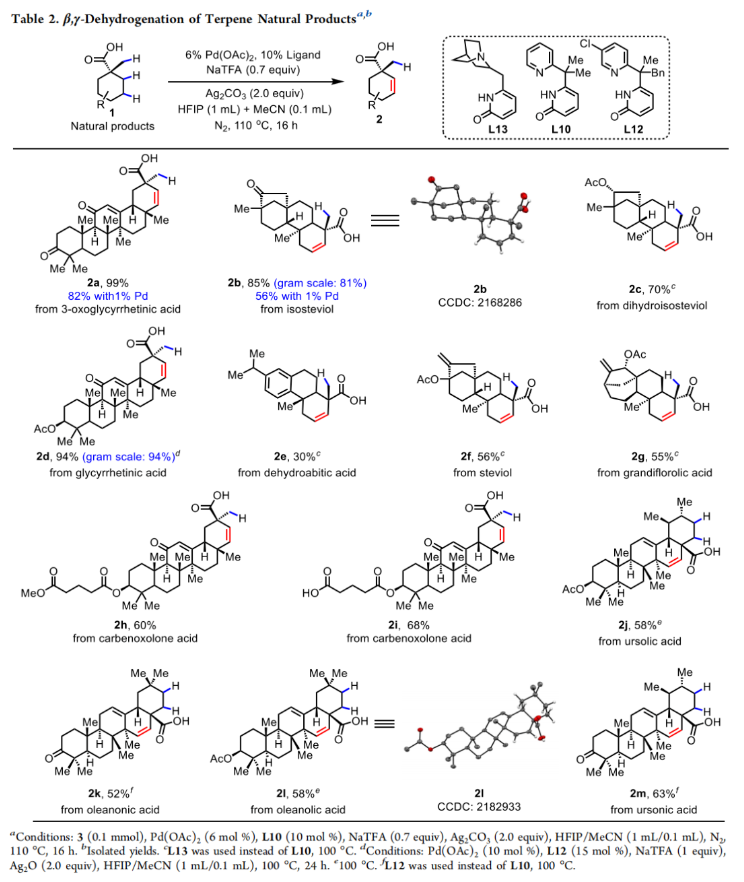
随后,作者探索了萜烯类天然产物利用此策略实现后期去饱和过程的底物范围(Table 2)。一系列具有重要生物学意义和合成意义的萜烯均可参与此β,γ-脱氢反应,以30-99%的产率得到相应的产物2a-2m,并与其他官能团展现出良好的相容性。其中包括isosteviol、steviol、grandiflorolic acid、carbenoxolone acid、ursolic acid、oleanolic acid、glycyrrhenic acid等一系列分子骨架均可兼容。值得注意的是,isosteviol和glycyrrhenic acid参与的反应均可以放大至克级规模,分别以81%和94%的产率得到2b和2d。此外,对于3-oxoglycyrrhetic acid参与的反应,当将钯催化剂的量降低至1%时,仍可以以82%的产率得到产物2a,这为此转化的大规模合成奠定了基础。
(图片来源:J. Am. Chem. Soc.)
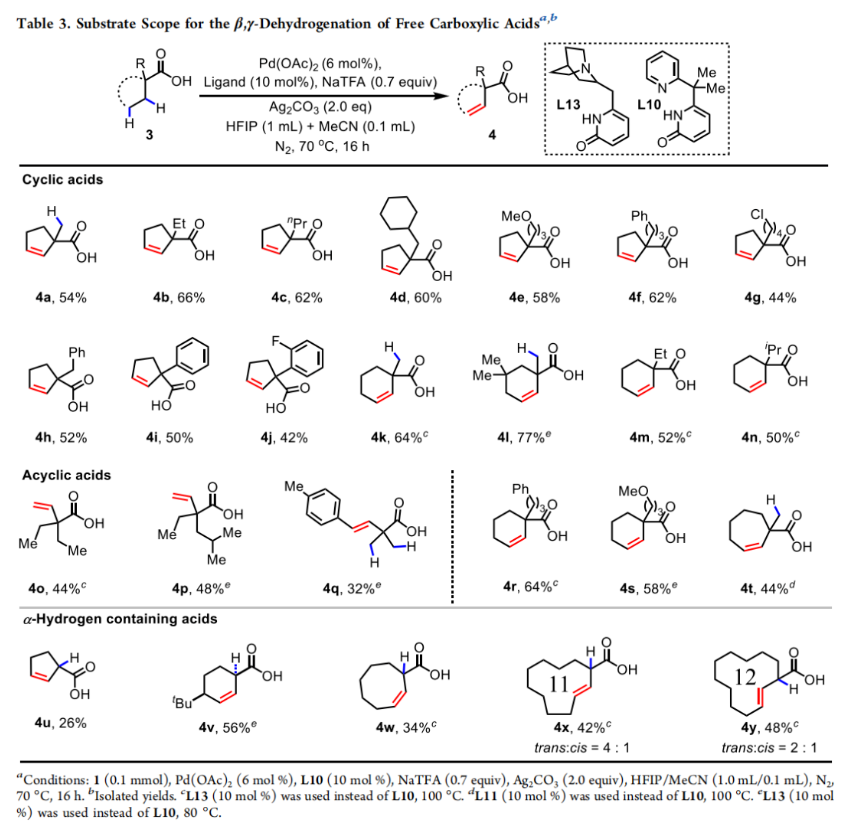
接下来,作者对一系列环状和非环状游离羧酸的兼容性进行了探索(Table 3)。具有多种不同α-取代的环戊基羧酸,如甲基、苄基、氯丁基和芳基等均可顺利实现此转化,以42-66%的产率得到相应的β,γ-脱氢产物4a-4j。值得注意的是,尽管在4b-4g中存在额外的β,γ-活化位点,但作者仅观察到了环戊烷环内的脱氢过程。非环链和环之间的区域选择性主要依赖于配体结构。在双齿吡啶酮配体的促进下,反应的有机金属中间体和过渡态是以钯为中心的螺环结构。因此,环戊基的构象与非环状链是截然不同的。除了环戊基羧酸外,含有6-(4k-4n, 4r, 4s),7-(4t)和8-(4w)元环的底物也均可以以单一的立体异构体生成顺式-β,γ-脱氢产物(32、34-77%)。有趣的是,含有11-(4x)和12-(4y) 元环的环状脂肪酸则倾向于得到反式烯烃的异构体混合物。此外,β,γ-非环羧酸也可发生脱氢,以32-48%的产率得到4o-4q。值得注意的是,与之前所报道的含α-氢脂肪酸(4u-4w)的α,β-脱氢反应相比,该策略将区域选择性转换为β,γ-脱氢。
(图片来源:J. Am. Chem. Soc.)
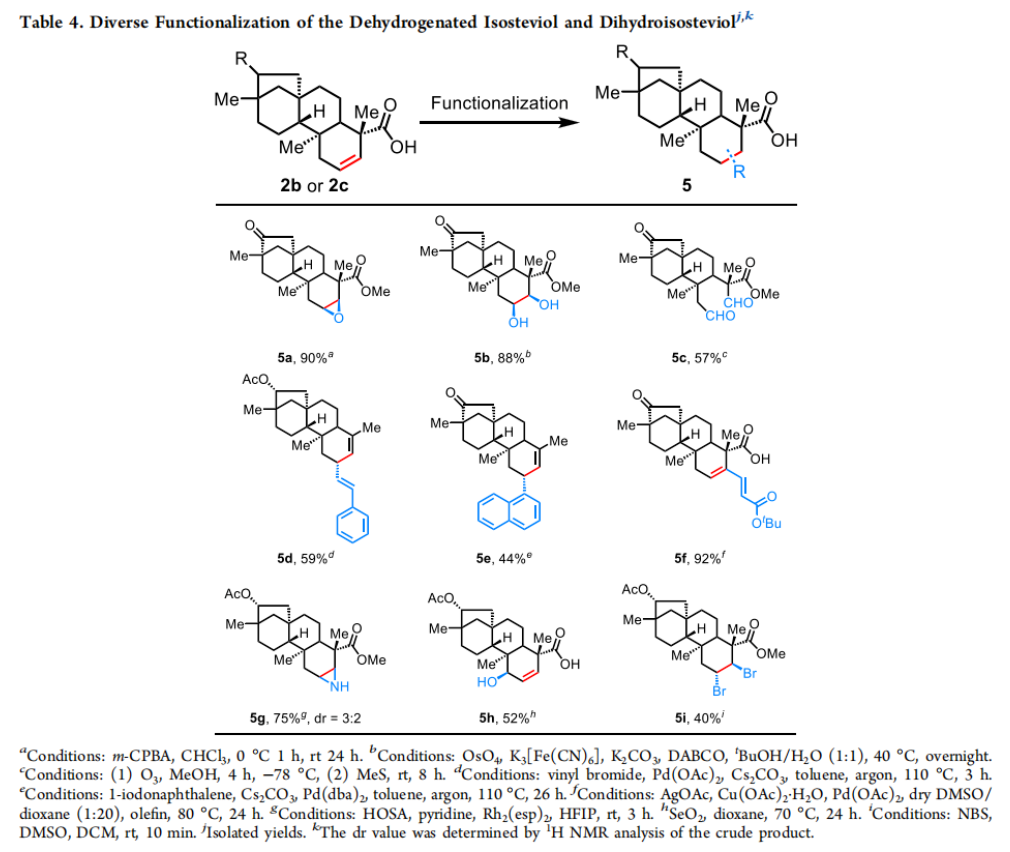
为了证明此转化的合成应用,作者利用isosteviol 2b和dihydroisosteviol 2c的β,γ-脱氢产物进行了后续衍生化(Table 4)。通过环氧化、双羟化、臭氧化、钯催化的脱羧烯基化和脱羧芳基化、钯催化羧基导向的C-H烯基化以及烯基的双溴化等过程实现了多种不同官能团化isosteviol产物5a-5i的合成(40-90%)。
(图片来源:J. Am. Chem. Soc.)
含有β-内酯的天然产物和衍生物具有较强的共价修饰蛋白质能力,因此,在天然产物上引入β-内酯骨架为基于活性的蛋白质分析提供了新的机会,这可以促进鉴定这些天然产物以前未知的细胞靶点。基于此,作者利用游离羧酸的β,γ-脱氢实现了一系列β-内酯的合成,并通过NBS溴化,构建了一系列溴代β-内酯(Table 5)。实验结果表明,无论五元或六元环羧酸、链状羧酸以及天然产物等均可兼容,以38-92%的产率得到相应的溴代β-内酯产物6a-6i。

(图片来源:J. Am. Chem. Soc.)
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn