

(图片来源:J. Am. Chem. Soc.)
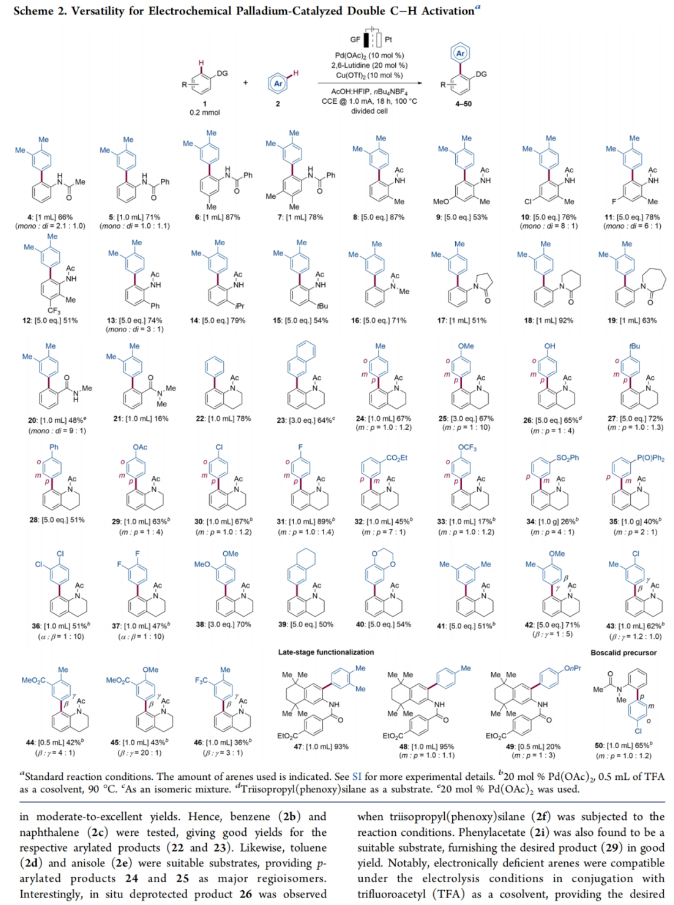
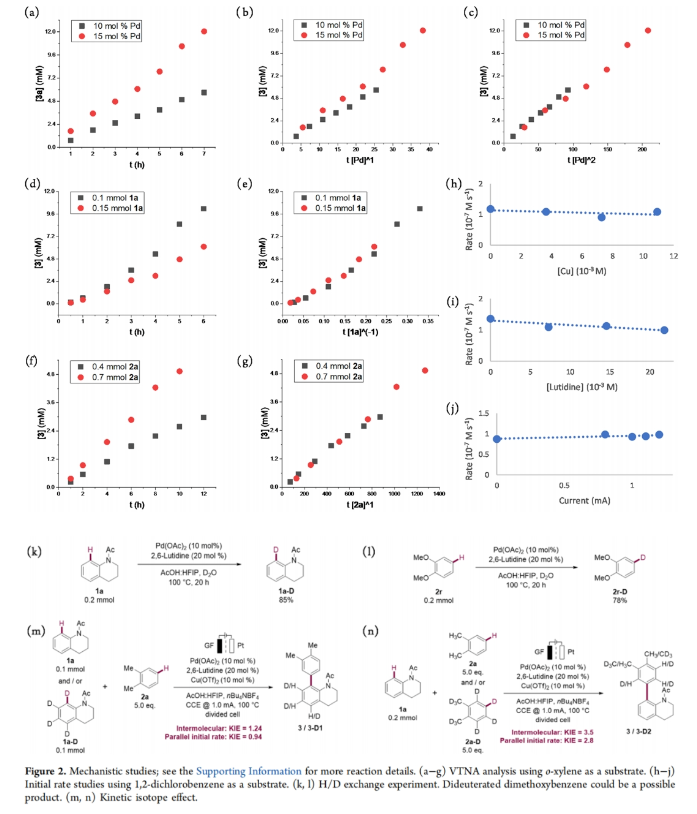
正文 联芳基骨架是一类重要的结构单元,传统的构建方法主要是卤化物与有机金属试剂的交叉偶联反应,但通常会产生超化学计量的化学废物。与之形成鲜明对比的是,钯催化简单芳烃的交叉脱氢偶联反应是一种符合原子经济和绿色合成的直接且快速的反应途径(Figure 1a)。然而,此类转化通常具有催化效率降低、底物范围有限和有副产物生成等问题。虽然早在1968年Davidson和Triggs就发现了钯络合物间的转金属化过程,但很少有报道能够为这种转化提供实验证据。2003年,Osakada课题组通过分子内的配体交换阐述了芳基的转金属化过程(Figure 1b)。此外,Hartwig和Stahl课题组分别对钯络合物转金属化过程的作用模式进行了详细的机理研究,分别实现了芳基卤化物和二甲苯直接芳基化。下载化学加APP到你手机,更加方便,更多收获。 近些年,过渡金属催化的C-H活化和电有机合成相结合已经成为一种独特且有效的可持续分子合成方法。其可以利用电来代替有毒的化学氧化剂。然而,通过电化学,钯催化的双C-H活化策略来构建联芳基化合物则少有报道。基于施章杰课题组多C-H键活化策略的启发(Figure 1c),最近,德国哥廷根大学Lutz Ackermann课题组报道了一种新颖的钯催化,电化学交叉脱氢转化,在不需要使用化学氧化剂以及对试剂进行预官能团化的条件下实现了联芳基化合物的构建。值得注意的是,作者提出了一种罕见的双金属机理,其以Pd-to-Pd的芳基转移过程作为决速步骤(Figure 1d)。 (图片来源:J. Am. Chem. Soc.) 首先,作者以N-乙酰基四氢喹啉1a和邻二甲苯2a作为模板底物进行反应探索(Scheme 1)。通过一系列反应参数优化,作者得出当使用阳极管:1a (0.20 mmol), 2a (1.0 mmol), Pd(OAc)2 (10 mol%), 2.6-lutidine (20 mol%), Cu(OTf)2 (10 mol%), nBu4NBF4 (40 mg), HFIP/AcOH (1.0 mL: 2.0 mL), 阴极管: 2a (1.0 mmol), nBu4NBF4 (40 mg), HFIP/AcOH (1.0 mL: 2.0 mL), 在1.0 mA电流下电解, 100 °C反应 18 h, 可以以72%的分离产率得到目标产物3。控制实验表明钯催化剂和电流在此双C-H芳基化过程中具有不可或缺的作用。 (图片来源:J. Am. Chem. Soc.) 在得到了最优反应条件后,作者对此转化的底物范围进行了探索(Scheme 2)。实验结果表明一系列不同取代的芳烃(尤其是缺电子芳烃)均具有良好的兼容性,以36-95%的产率得到相应的联芳基产物4-50。其中,一系列骨架和官能团包括卤素、潜在的Shono-类型氧化烷基化酰胺骨架等均可兼容。遗憾的是,羧酸和溴苯不能兼容此体系。值得注意的是,利用此策略还可以实现生物活性分子Tamibarotene酯的后期衍生化以及实现Boscalid前体的合成。 (图片来源:J. Am. Chem. Soc.) 随后,为了深入理解反应过程,作者进行了动力学研究(Figure 2),并得出如下结论:1)钯催化剂的动力学级数是二级而不是一级;铜、lutidine和电流的动力学级数为零;2)缺电子芳烃的反应途径与富电子芳烃的反应机理有关;3)2当量钯、1当量1a和1当量2a参与了速率决定步骤。基于上述结果,作者认为反应有两种可能的反应途径:1)Pd(II)到Pd(II)的转金属化机理;2)双金属Pd(IV)机理。而转金属化机理是更可能的反应路径。此外,作者通过H/D交换实验得出这两种同位素参与反应的产率均超过了Pd(OAc)2的量,这表明每种底物的金属化过程均是可逆的。此外,KIE研究显示底物1a存在二级KIE或不存在KIE,底物2a存在一级KIE,这表明1a的C-H键很容易断裂,而2a的C-H键断裂较难。 (图片来源:J. Am. Chem. Soc.) 为了进一步验证作者所提出的两个钯中心之间的协同芳基转移过程,作者探索了在决速步骤中静息态催化剂和活性催化剂之间的关系(Figure 3)。首先,作者通过HRMS分析,对在催化条件下可能的中间体进行了监测。从HRMS谱图得出,反应中存在三个中间体51-53(Figure 3a)。随后,作者使用非配位的二氯甲烷作为溶剂,合成了二聚体络合物54和55(Figure 3b)。络合物54和55在温和条件下即可获得与作者所观测到的1a的KIE值相一致。在室温下,用乙腈处理二聚钯络合物55,可以以接近定量的产率形成单体钯络合物56(Figure 3c)。55和2a之间的化学计量反应在1小时内可以以44%的产率得到产物8,在2小时内以55%的产率得到8(Figure 3d),这表明有机钯络合物55可能是反应的活性催化剂前体。这一假设通过55和二甲苯反应的原位核磁共振研究得到了证实,并观察到了预催化剂55的诱导期(Figure 3e)。作者通过55和56反应的非原位GC监测得出这两种中间体的反应速率相当(Figure 3f)。考虑到络合物56是由强配位的乙腈来稳定的,因此单体钯是动力学上更有利的活性催化剂。此外,DFT计算揭示了Pd(OAc)2在二甲苯上的C-H活化在能量上是有利的,且能垒为16.4 kcal mol−1。然而,当使用二聚体催化剂时,同样的步骤在能量上是不利的,且能垒为25.2 kcal mol−1。循环伏安法(CV)测试表明,络合物55在室温下,HFIP/AcOH中具有良好的稳定性(Figure 3g)。在室温下加入过量的2a时,作者并没有观察到催化电流,因此否定了Pd(III)或Pd(IV)中心发生二次C-H活化的可能性。将络合物54在用于催化的溶剂中加热至90 oC可以诱导络合物58的形成(Figure 3h)。根据上述实验观察和动力学研究,作者提出中间体52为静息态,单体51是循环活性催化剂。 (图片来源:J. Am. Chem. Soc.) 接下来,作者探索了Cu(OTf)2和2,6-lutidine在活性催化剂再生中的确切作用(Figure 4)。在1当量Cu(OTf)2作为化学氧化剂的情况下,增加2,6-lutidine的用量,产物3的产率从88%下降到20%,而以电为氧化剂的反应则保持了催化效率(Figure 4a)。这就导致了在lutidine存在下Cu2+的氧化能力降低,这一点通过CV研究得到了证实(Figure 4b)。此外,当作者将钯和铜混合时观察到了新的氧化过程,从而证实了不同金属之间的相互作用(Figure 4c)。因此,作者得出反应中铜盐是作为Pd(0)的稳定剂而非氧化还原催化剂。 (图片来源:J. Am. Chem. Soc.) 基于上述实验结果,作者提出了可能的催化循环(Figure 5):首先,1a和2a的C-H活化同时发生,分别产生络合物51和59。在这里,二聚体催化剂53是单体钯环51的预催化剂。根据底物1与Pd(OAc)2的比例,闭循环物种52可以以不同的浓度存在。随后,51与59通过分子间转金属化产生60,并通过还原消除得到所需产物3。两个有机钯络合物之间的转金属化为整个反应的决速步骤。产物形成过程中所生成的Pd(0)随后被Cu络合物稳定,而Cu络合物通过阳极氧化再生活性Pd(II)物种,从而结束催化循环。 总结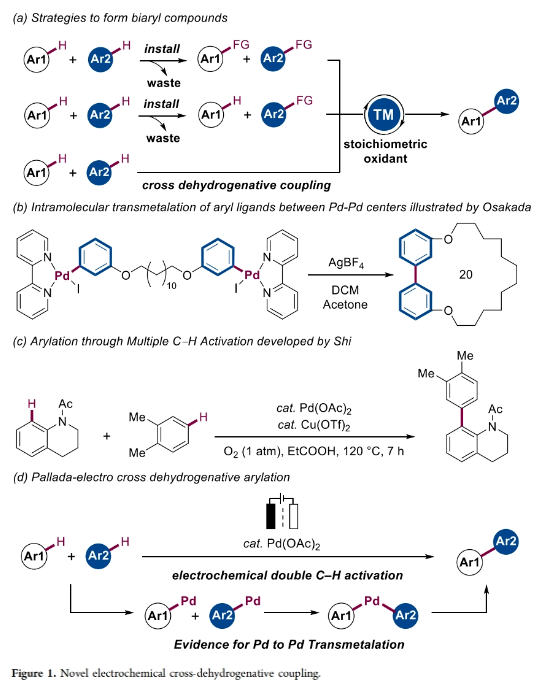




声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn