

为了解决这一问题,近日美国加州大学洛杉矶分校段镶锋教授和Philippe Sautet教授等人合作,以氮、硫、双掺杂多孔石墨烯框架(N, S-HGF)电催化剂和未掺杂的HGF作为对比研究对象。并通过多种表征手段建立了详细的反应网络,阐明了中心中间体Li2S4前后的主要反应途径,识别了关键中间相,如Li2S4和Li2S,并确定了非电化学比例在Li2S8和Li2S4之间的重要性。此外,通过对比N, S-HGF和HGF,作者验证了N, S-HGF催化剂能够加速LiPSs的转化,使其在较高电位下更快耗尽,从而缓解了多硫化物的穿梭效应,提高了电池的输出性能。这项研究为理解电催化SRR机理提供了重要的见解,并为设计更高效的催化剂提供了理论指导。

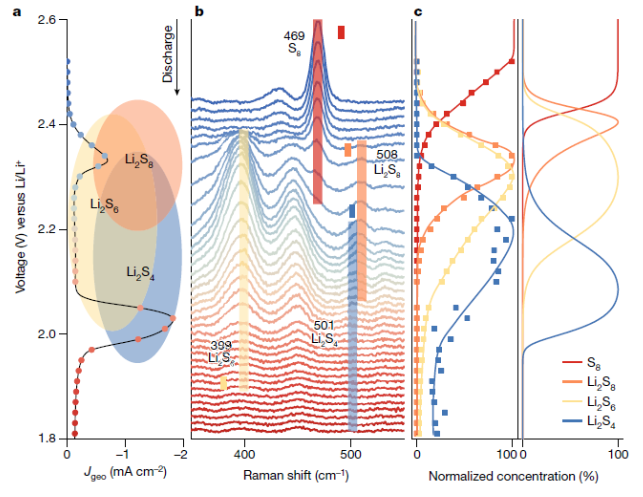
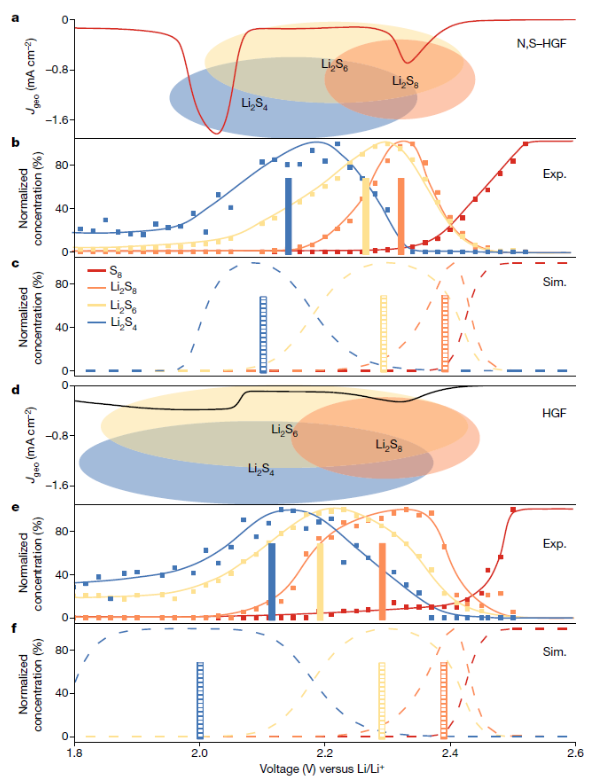
正文 为了让读者形象理解锂硫电池中涉及的多硫化物转化反应,作者在图1a展示了该电池中涉及的SRR的示意图。其中,SRR涉及从S8分子到Li2S固体的复杂的16电子转化过程。图1b显示了具有N,S–HGF催化剂的CV曲线。插图显示了在约2.11–2.25 V的近似电压范围内的平台,这是Li2S8转化为Li2S4的延迟引起的电压变化范围。图1c示意了本研究中使用的原位拉曼技术。总之,图1形象的给读者展示了一个微观化学原子反应的机理,有助于作者进一步采用一些表征手段去验证这个想法。下载化学加APP到你手机,收获更多商业合作机会。。 图片来源:Nature 为进一步揭示N,S–HGF对Li-S电池中多硫化物转化反应的显著影响(图2)。作者首先确认了N,S–HGF相较于未掺杂的HGF能够明显加速SRR动力学。比如通过对CV曲线进行积分,计算得到的电荷数被转换为完整的16电子过程中的电子转移数。在第二个峰值(2.11 V)开始处分离整体放电过程,得到了一个电荷转移比为4.08:11.92(约等于1:3),这一比例经过电流-放电测试进行验证。这表明Li2S4是主要中间体分隔了两个还原峰。为了探究这一反应的化学起源,作者使用第一性原理计算了不同多硫化物中间体之间的基本能量学。计算模拟显示,从S8到Li2S8的转化产生了2.41 V的最高计算输出电位。而Li2S8分子的进一步转化涉及多个可能的分支,计算表明形成两个Li2S4的路径是放热比较严重的,所以是最有可能产生2.24 V的输出电位。最后,考虑到实验中观察到的平台可能源于混合反应产物的延迟电化学转化,作者通过将DFT计算结果与电压效应结合,模拟得到不同多硫化物的浓度随电位的变化。计算显示,主导的LiPS相的顺序为S8、Li2S8、Li2S6、Li2S4和Li2S。从浓度导出的CV曲线得到的电荷比为2.82:1.20:11.98,与实验中观察到的比例相匹配。这一研究为理解Li-S电池中复杂的反应机制提供了重要的依据,为优化电池性能提供了理论指导。 图2. SRR的电荷分析和反应网络。 为了探究Li-S电池放电过程中的具体反应中间体,作者采用了原位拉曼光谱技术对放电CV扫描过程中的反应中间体进行了研究。图3a,b展示了在不同电位下反应中间体的变化。结果表明,在初始状态下存在典型的S8峰(469 cm−1),证实了元素硫的存在。随着电位的降低,S8信号逐渐减小,并在约2.36 V处消失,同时约2.44 V下出现了Li2S8信号(508 cm−1)并伴随着Li2S6峰(399 cm−1)的出现。随后,Li2S8峰值逐渐减小,而Li2S4峰(501 cm−1)在约2.18 V时达到最大值。随着电位的降低,Li2S4成为主要的多硫化物,而通过共晶反应形成的Li2S6也显著存在。通过比较实验和计算结果,发现了S8、Li2S8、Li2S6、Li2S4在不同电位下的浓度变化具有相似的序列。值得注意的是,Li2S6的出现电位与Li2S8相似,而其消耗电位与Li2S4相似,表明通过共晶/非共晶反应之间存在动态平衡。这些结果有助于更好地理解Li-S电池的放电机制,并为设计更高性能的电池提供了重要参考。 图片来源:Nature 为了进一步了解电催化剂对SRR的影响,作者对比研究了非掺杂的HGF与N,S–HGF的催化系统(图4)。结果显示,在高电位处这两种不同催化剂的放电第一步在某种程度上存在差异。具体是Li2S8的峰在HGF中稍有延迟。此外,Li2S6的转化对非掺杂的HGF更为敏感。这是因为在这种情况下Li2S4的转化动力学较慢,从而延迟了低价态的多硫化物消耗,使其出现在更低的电位区域(低于1.97 V),但是在该区域中电化学还原Li2S6也可能开始发生。所以结果说明Li2S4的转化主导了电催化过程,特别是在SRR的第二阶段开始时。这些CV和实时拉曼研究显示了HGF和N,S–HGF之间明显的SRR动力学差异,突显了高效催化剂带来的好处。 图4. SRR中不同催化剂的比较。 图5通过研究第二阶段的反应途径——即从Li2S4到Li2S的转化,以了解这两种电催化剂的不同电位范围。考虑从Li2S4开始的所有可能的电子转移步骤(见图5),他们在各种催化剂位点的存在下检查了总共12种不同的反应途径。结果发现了两个产生最高输出电位的途径(见图5c)。比如,在这两个途径中,相对于非掺杂位点为2.03 V ,N,S共掺杂位点表现出更高的输出电位(2.11 V),因此展示了N,S–HGF的卓越性能。有趣的是,内部缺陷位点在输出电位图中位于顶部的距离较近(图5b、c),与花边和锯齿边缘位点(分别为三角形和方形)相比,验证了石墨烯掺杂对电催化的有效性。这表明,最终从Li2S2到Li2S的转化是电位限制的步骤。HGF和N,S–HGF有效输出电位的模拟差异仅在第二阶段显著,与实验结果基本相符。实验证明和理论之间的这种密切关联进一步验证了改进Li-S电池的电催化策略。 总结


声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn