

正文
(图片来源:J. Am. Chem. Soc.)
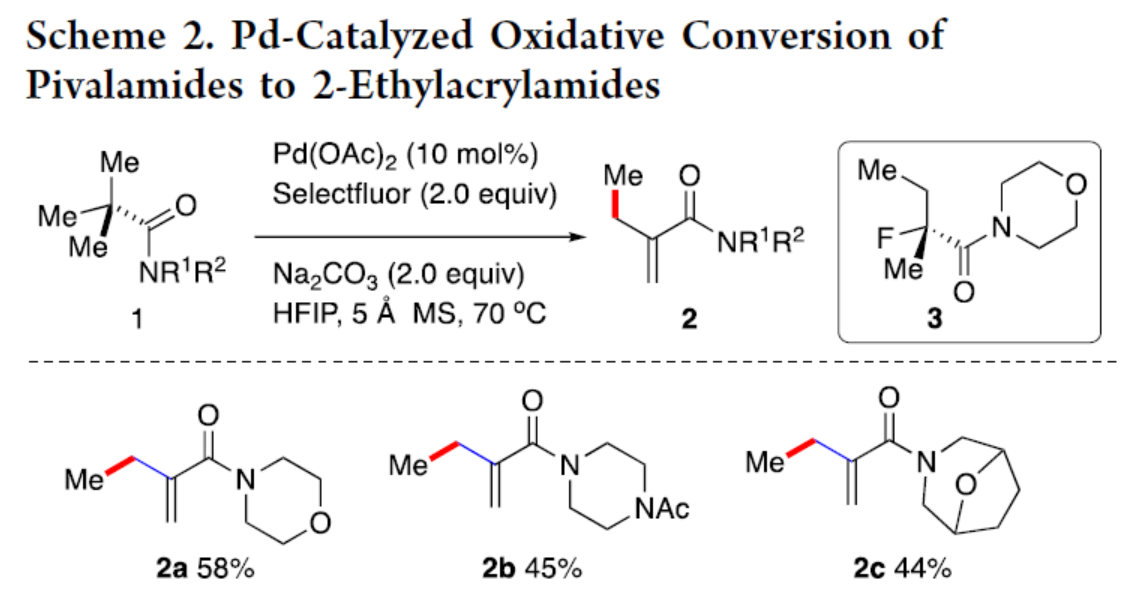
首先,作者以新戊酸的吗啉酰胺衍生物1a作为模型底物,进行了相关反应条件的筛选(见SI)。进而确认了最佳的反应条件(Scheme 2),以Pd(OAc)2(10 mol %)作为催化剂,Selecfluor(2.0 equiv)作为氧化剂,Na2CO3(3.0 equiv)作为碱,5 Å MS作为添加剂,在HFIP溶剂中70 oC反应,可以58%的收率得到产物2a。同时,通过相同的反应条件,还可合成产物2b(收率为45%)和2c(收率为44%)。
(图片来源:J. Am. Chem. Soc.)
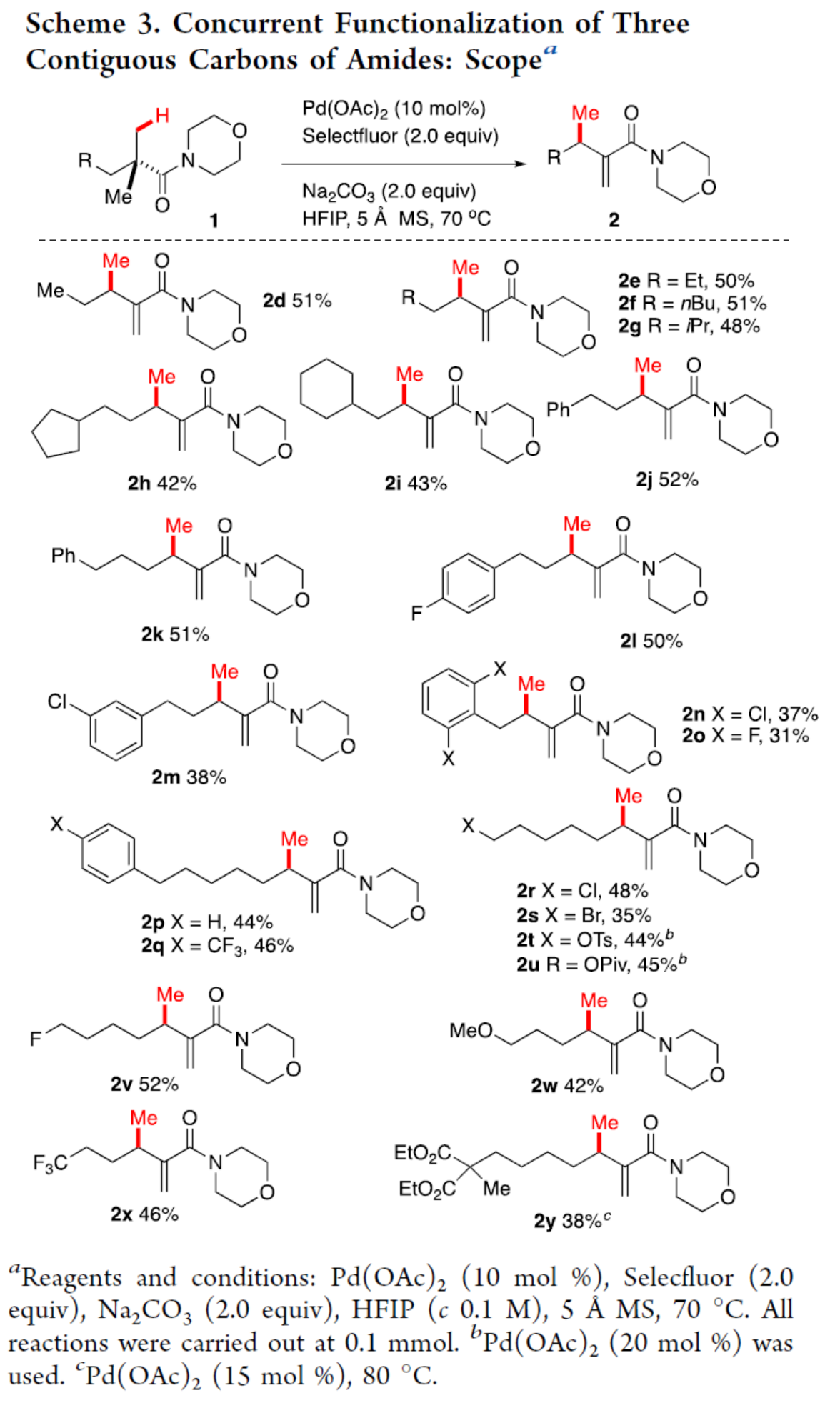
在获得上述最佳反应条件后,作者对底物范围进行了扩展(Scheme 3)。首先,具有不同链长度的直链和支链2,2-二甲基链烷酸的吗啉基酰胺衍生物,均可顺利反应,获得相应的产物2d-2k,收率为42-52%。其次,在邻位、间位和对位(2l-2o)带有氯和氟取代的芳基也与体系相容,并且可以容忍亲电烷基卤化物和甲苯磺酸烷基酯官能团的存在,从而为后期官能团化提供了机会,如获得相应的产物2l-2t,收率为31-50%。正如预期的那样,其他官能团如新戊酸酯和甲基醚也可以掺入至产物中,获得相应的产物2u(45%)和2w(42%)。值得注意的是,通过该策略还可以获得含有药用的含有氟和三氟甲基(2l,2o,2q,2v,2x)的化合物。此外,乙氧羰基的存在不会干扰反应过程(2y),这可能是由于酰胺的配位能力比烷氧羰基更强。然而,(1-甲基环戊基)-(吗啉基)甲酮在上述标准条件下仅生成复杂的反应混合物。
(图片来源:J. Am. Chem. Soc.)
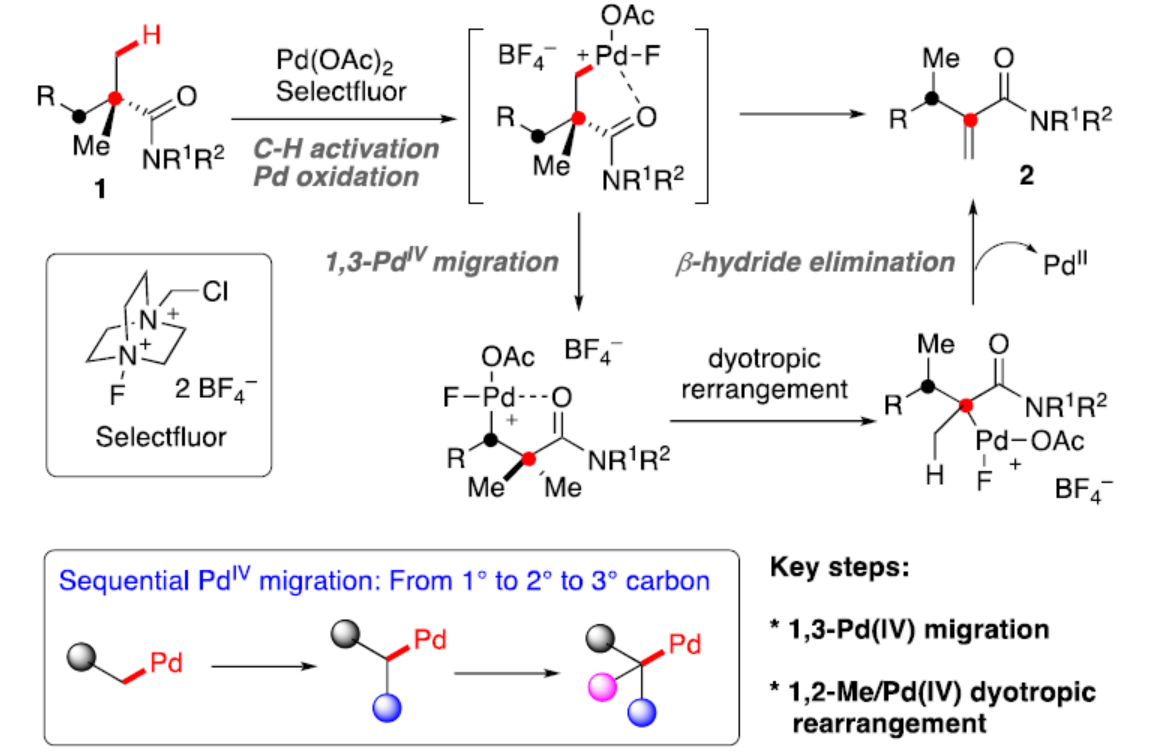
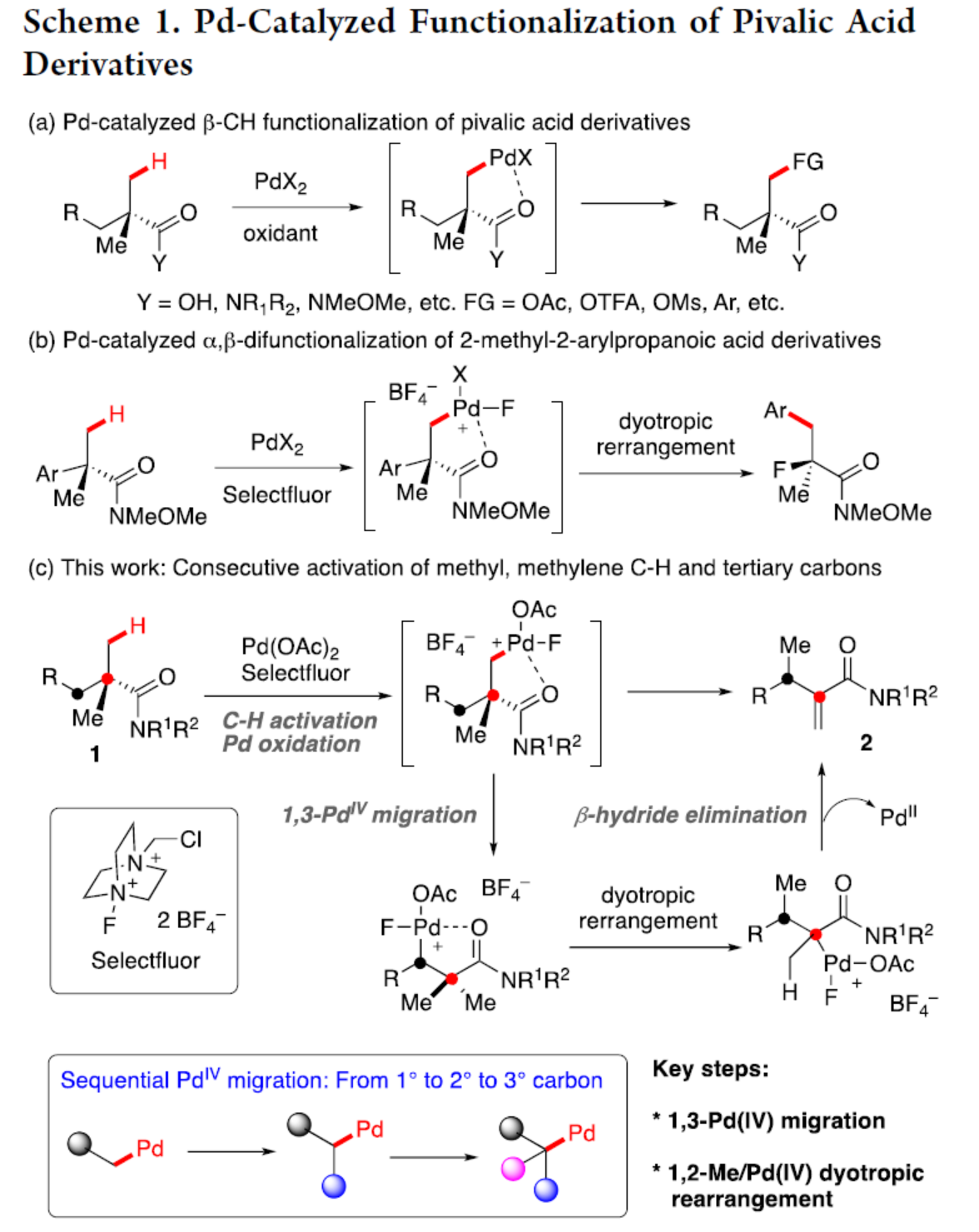
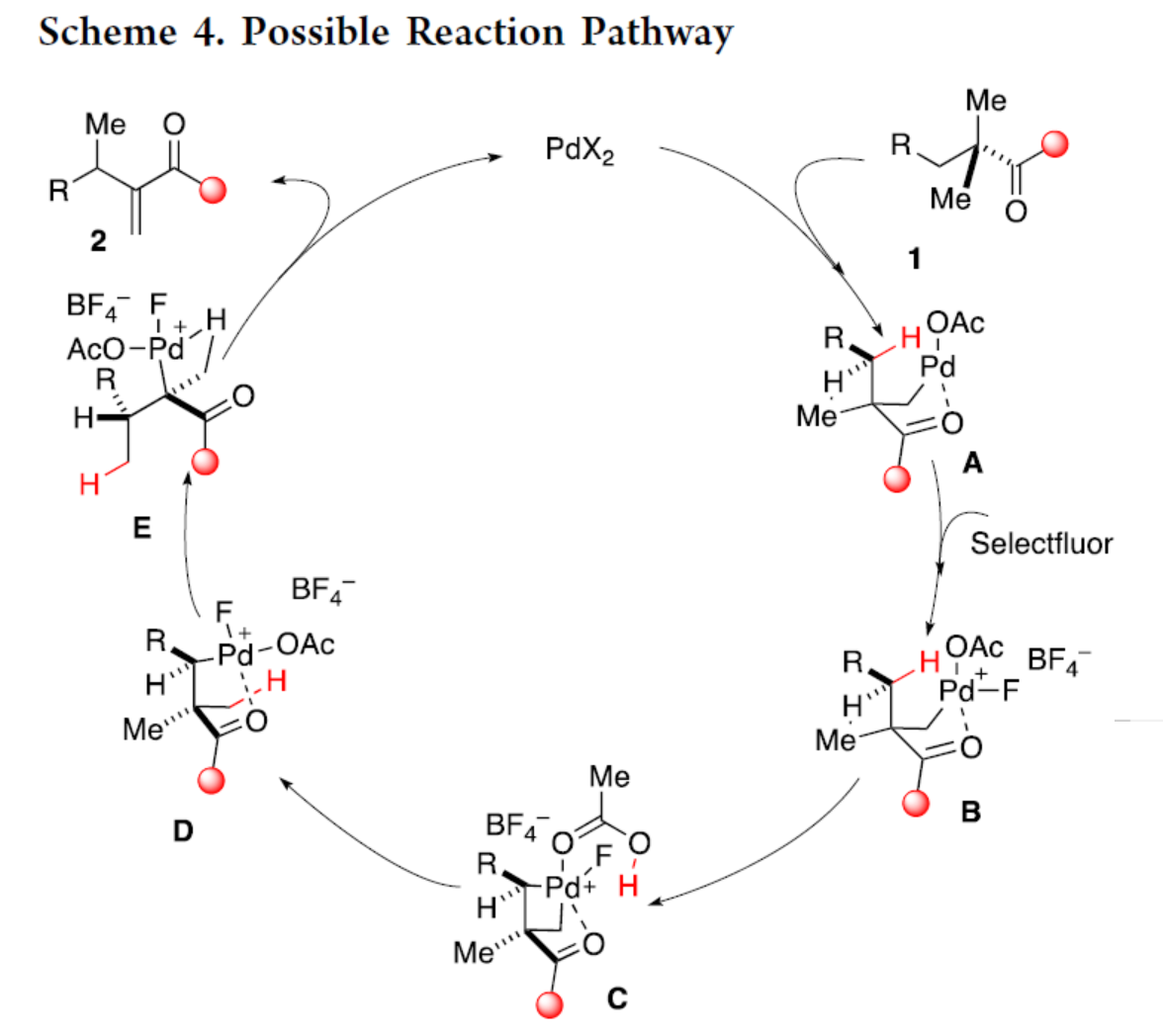
紧接着,作者提出了一种合理的催化循环过程(Scheme 4)。首先,酰胺化合物1中的一个甲基与PdX2经C(sp3)−H钯化,生成PdII配合物A。在Selecfluor存在下,配合物A经氧化生成PdIV配合物B。其次,通过1,3-PdIV迁移,可能实现配合物B向配合物D的转化,涉及四元钯环中间体C的形成。随后,配合物D经1,2-甲基/PdIV Dyotropic重排,生成配合物E。最后,配合物E经β-氢消除后,可生成目标产物2,同时再生PdII催化剂。作者认为,通过β-氢消除选择性形成末端烯烃是Pd与甲基中一个空间上更易接近的氢之间有利的激发相互作用的直接结果。
(图片来源:J. Am. Chem. Soc.)
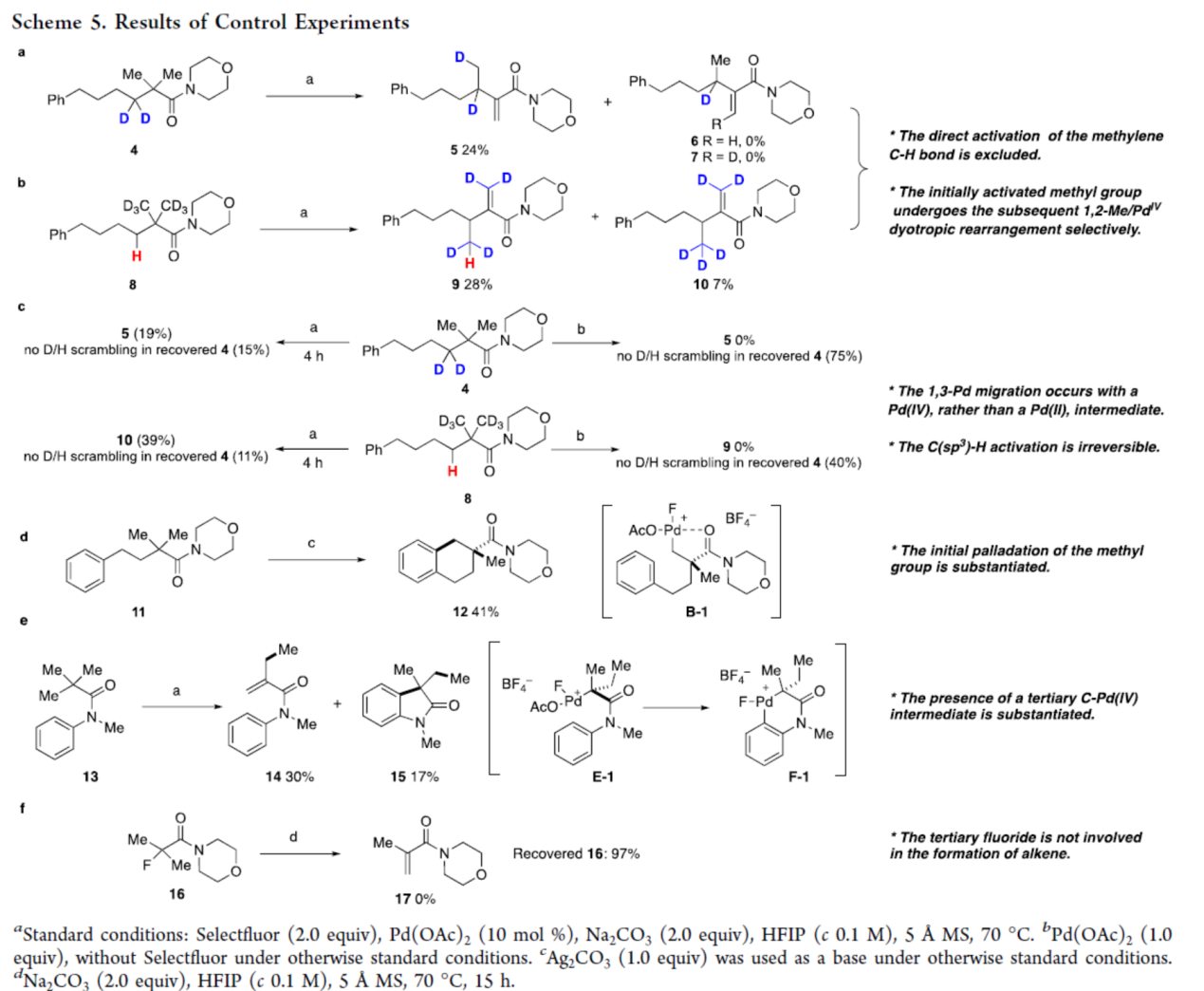
此外,作者还对反应机理进行了进一步的研究(Scheme 5)。首先,将双氘底物4置于标准反应条件下,得到重排产物5,作为唯一可分离的氘标记区域异构体,且没有观察到其他可能氘标记异构体6和7的形成(Scheme 5a)。同时,将底物8置于标准反应条件,分别以28%和7%的收率得到产物9和10(Scheme 5b)。在完全转化之前淬灭上述两个反应,可回收起始原料4和8,并且通过NMR分析证实了没有发生氘置换(deuterium scrambling)。其次,在无氧化剂的对照实验结果表明,反应可能是由酰胺的2-甲基基团活化引发的,然后在钯氧化后,生成的一级C(sp3)−PdIV发生1,3-迁移,转化为二级C(sp3)−PdIV,C-H活化是不可逆的。同时,最初被活化的甲基优先进行1,2-Me/PdIV Dyotropic重排。由于CH2D和CH3基团之间的迁移能力没有显著差异,中间体D的构象偏好和Dyotropic重排机理应该是观察到选择性的原因。紧接着,将酰胺11置于标准条件下,可以41%的收率得到2,2-二取代的四氢萘12(Scheme 5d)。邻近的PdIV活化苯基C(sp2)−H,然后还原消除产生的钯环,可以解释12的形成。此外,N-甲基和N-苯基新戊酰胺13除了得到预期的丙烯酰胺14外,还转化为羟吲哚15(Scheme 5e)。这两种化合物都可以衍生自PdIV中间体E-1。虽然E-1的β-氢消除会产生14,但侧苯基Csp2−H键的分子内活化,然后还原消除则生成钯环F-1,会导致15的形成。这些结果证实了PdIV中间体B和E的存在。最后,化合物16在碳酸钠的HFIP溶液中70 oC加热时,未发生反应,表明了叔氟化物16不是合成烯烃2的中间体(Scheme 5f)。
(图片来源:J. Am. Chem. Soc.)
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn