- 首页
- 资讯
上海交大商明课题组JACS:首例配体驱动的铜催化核苷类ProTide前药的不对称合成
来源:上海交通大学 2024-11-08
导读:近日,上海交通大学变革性分子前沿中心的商明课题组实现了首例配体驱动的廉价金属铜催化核苷类ProTide前药的不对称合成,相关研究成果在Journal of the American Chemical Society上发表。
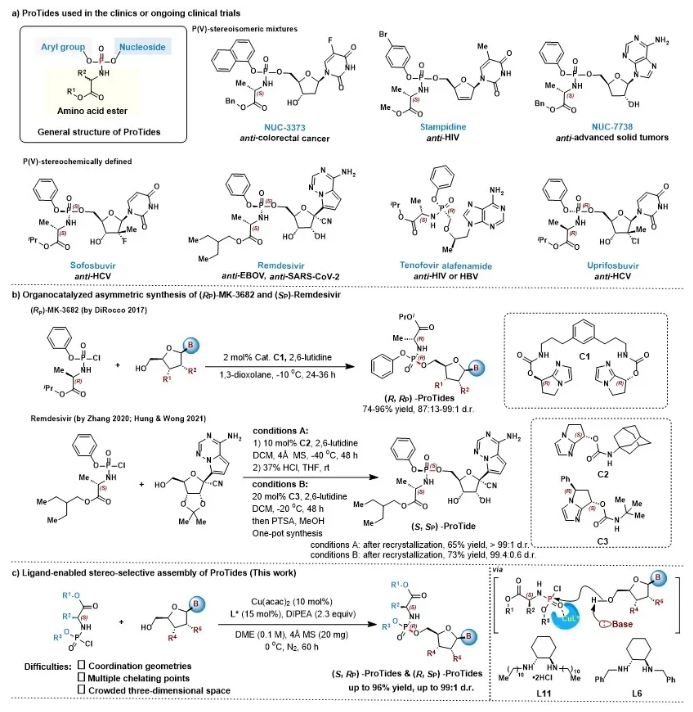
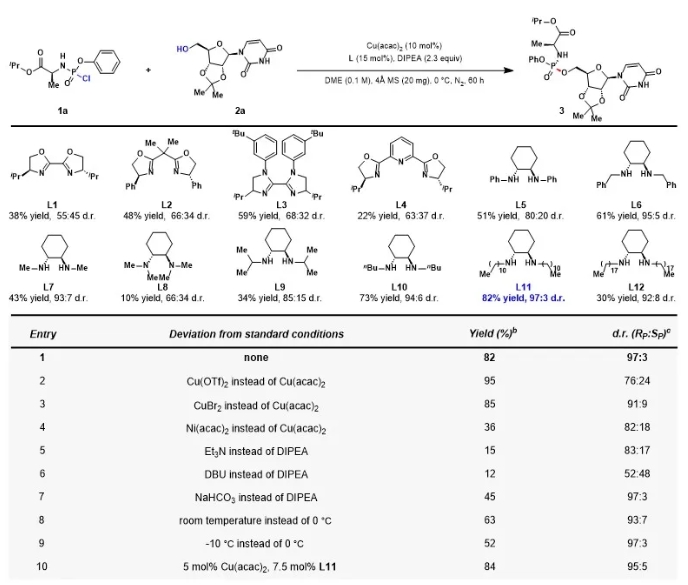
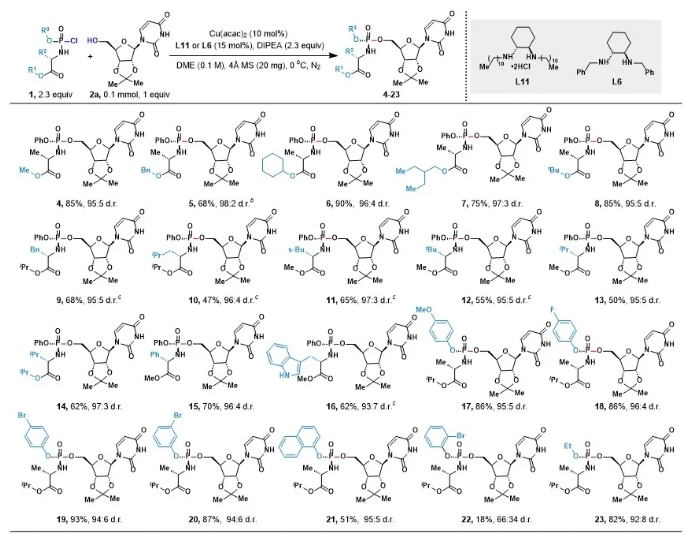
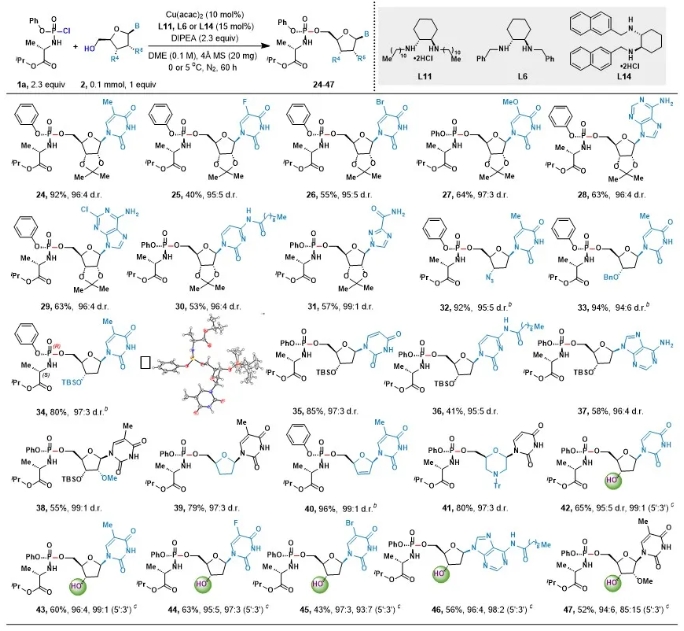
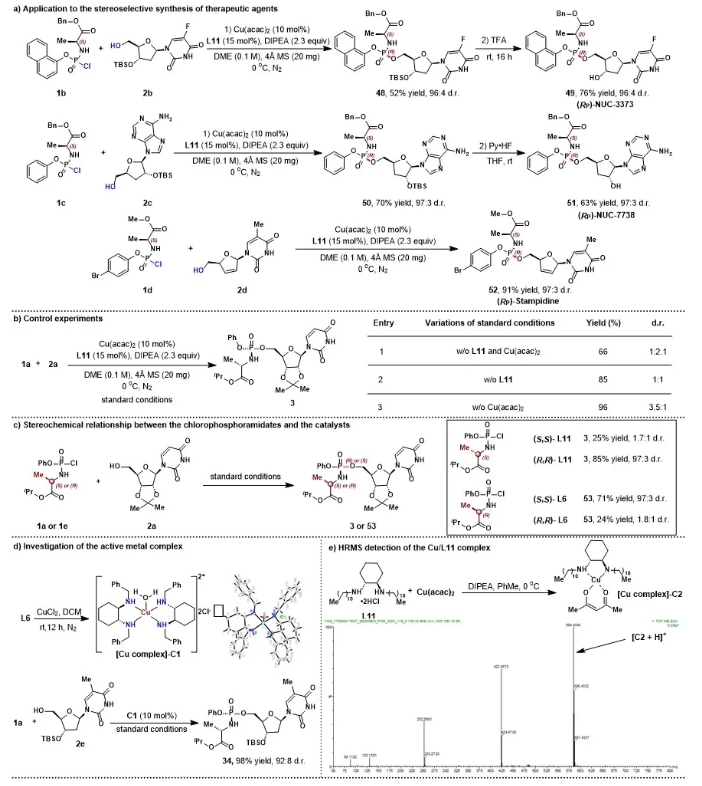
核苷类药物在抗病毒、抗肿瘤药物中占有相当比重,其在酶催化下可形成核苷三磷酸靶向并抑制DNA聚合酶或RNA逆转录酶活性,从而发挥治疗作用。由于磷酸基团极性大难以通过细胞膜,McGuigan等人发明了核苷前药(ProTide)策略。该技术通过将核苷磷酸根负离子掩蔽,从而更好地发挥生物活性。目前,前药策略已经被广泛用于药物的合成,已孕育出上市药物包括索非布韦、瑞德西韦、丙酚替诺福韦和临床候选药物Adafosbuvir、Uprifosbuvir、INX-08189等(图1a)。研究发现,ProTide前药分子中磷的绝对构型会改变代谢活化效率,极大影响药效发挥。因此立体选择性构建磷手性中心,是核苷类药物合成中的一个关键技术瓶颈。不对称催化是构建磷手性中心一种行之有效的方法。但是,截至目前,仅少数研究团队利用手性小分子催化剂,实现了为数不多的(R, RP)和(S, SP)-ProTides的催化不对称合成(图1b),从磷酰氯出发同时实现(R, SP)和(S, RP)-ProTides的催化不对称合成还未有报道。近日,上海交通大学变革性分子前沿中心的商明课题组实现了首例配体驱动的廉价金属铜催化核苷类ProTide前药的不对称合成(图1c)。 反应具有以下三个挑战:第一,金属催化立体选择性构建P-O键报道较少;第二,氨基磷酰氯底物具有独特的配位模式、多个螯合位点和拥挤的三维空间;第三,配体要求严格,不仅要能提高反应效率又要能控制手性。鉴于过渡金属催化的多种优势,作者使用市售可得的核苷2a与磷酰氯1a作为模板底物进行反应制备ProTide产物3,经过一系列条件优化(图2),作者以97:3 d.r.和82%的收率得到目标产物。反应成功的关键在于使用刚性较强的手性环己二胺配体,辅以长链烷基边臂效应,极大地改善了反应结果。值得一提的是,降低催化剂负载至5mol%几乎不会影响反应结果。 在获得最佳条件后,作者对底物范围进行了考察。首先考察了磷酰氯范围,如图3所示,各种L-丙氨酸磷酰胺都具有良好的耐受性(4-8, 68-90%, 95:5-98:2 d.r.),此外,L-苯丙氨酸、L-亮氨酸、L-异亮氨酸、L-叔亮氨酸、L-缬氨酸和L-苯甘氨酸等也能很好地适应反应条件(9-15、47-70%、95:5-97:3 d.r.),同样地,未保护的L-色氨酸磷酰胺也能顺利进行(16,62%,93:7 d.r.);该催化模式对多种芳氧基底物表现依然十分出色,包括4-OMe、4-F、4-Br、3-Br和萘基(17-21),大大促进芳氧基磷酰胺前药构效关系(SAR)研究。虽然2-Br磷酰胺(22)空间位阻大反应活性低,但是烷氧基取代磷酰胺却能以良好的收率和立体选择性顺利得到23。 接着,作者考察了核苷底物的适用范围。如图4所示,各种含有天然碱基和非天然碱基的核苷都具有强的反应活性和高的立体选择性(24-31, 40-92%, 95:5-99:1 d.r.),所开发的催化体系对含有敏感官能团如丙酮叉、酰亚胺、未保护的胺、酰胺和亲核性杂环底物都有很好的耐受性,包括抗HIV药物叠氮胸苷(32)在内的脱氧核苷底物也能高效转化为相应的ProTide前药(32-37,41-94%,94:6-97:3 d.r.)。X-射线单晶衍射确定了化合物34磷中心手性的绝对构型是R构型,鉴于吗啉寡核苷酸(PMOs)在治疗中的重要意义,作者进一步合成了吗啉类前药,获得了高达80%的产率和97:3 d.r.,将配体调整为L14,作者成功地将该方法应用于一系列无保护的脱氧核苷底物,并有着优异的5’:3’选择性及立体选择性。 随后,作者成功地将反应应用到临床抗肿瘤药物NUC-3373、NUC-7738和抗病毒药物司他夫定ProTide的合成中(图5a),说明此反应在ProTide前药研发领域具有较大潜力;最后,作者研究了反应机理,控制性实验表明,催化剂和配体两者缺一不可(图5b);调整配体的构型,可同时得到(R, SP)和(S, RP)两种构型产物(图5c);单晶衍射(图5d)和HRMS(图5f)实验进一步确定了反应过程中手性金属络合物的产生,验证了金属催化的反应机制。 商明课题组报道了首例铜催化核苷类ProTide前药的不对称合成,发展了一种长链烷基取代的手性环己二胺配体,提高了反应的效率和立体选择性,该方法具有反应条件温和、操作简单、适用范围广等优点。作者通过将其应用于临床ProTide前药的制备,证明了方法的实际效用,大大地推进了ProTide前药领域的发展。商明课题组隶属于上海交通大学变革性分子前沿科学中心,主要研究方向包括1.核苷酸高效合成方法开发,手性核酸合成;2.非天然核苷酸模块化合成方法开发;3.核酸药物开发。
因工作需要,拟招聘核酸化学/有机合成方向的博士后1-2名,待遇从优,年薪40万起(无任何附加条件),欢迎具有相关研究经历并有志于从事核酸合成化学研究的青年才俊加盟。
另外,课题组同时招收2025年入学申请考核制博士生,欢迎对本课题组研究方向感兴趣的同学联系申请。
请有意申请者将个人简历(包含学习经历、工作经历、发表论文等内容)发送至shangsjtu@sjtu.edu.cn。邮件标题注明:应聘岗位+本人姓名。申请截止时间2025年4月。文献详情:
Ligand-Enabled Cu-Catalyzed Stereoselective Synthesis of P-Stereogenic ProTidesShuai-Shuai Fang, XiangJun Hu, Ming-Hong Li, Shuang Qi, Tian Xie, Jia-Bao Wang, Hong-Qing Yao, Jian Zhang, Jun-Hua Zhang, Lijuan Zhu, and Ming Shang*https://doi.org/10.1021/jacs.4c12920
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn