

背景介绍
金纳米颗粒(AuNPs)因其独特的物理化学特性而备受关注,包括高消光系数、优异的生物相容性、尺寸依赖的光学特性以及高效的荧光共振能量转移(FRET)能力。基于这些特性,研究者们通常通过金-巯(Au-S)共价键将各类功能分子(如抗体、适配体、多肽和聚合物等)修饰到AuNPs表面,构建多功能纳米探针。这些功能化的AuNPs在生物传感、细胞成像、药物递送和疾病治疗等领域展现出巨大的应用潜力。然而,Au-S键固有的化学不稳定性限制了其实际应用:在复杂的生理环境中,特别是面对细胞内高浓度的生物硫醇(如谷胱甘肽,半胱氨酸等)时,Au-S键容易发生配体交换反应,导致探针结构破坏和功能丧失,最终造成检测信号失真,严重影响其在生物医学应用中的可靠性和准确性。这一局限性促使研究者们致力于开发更稳定的AuNPs表面修饰策略。
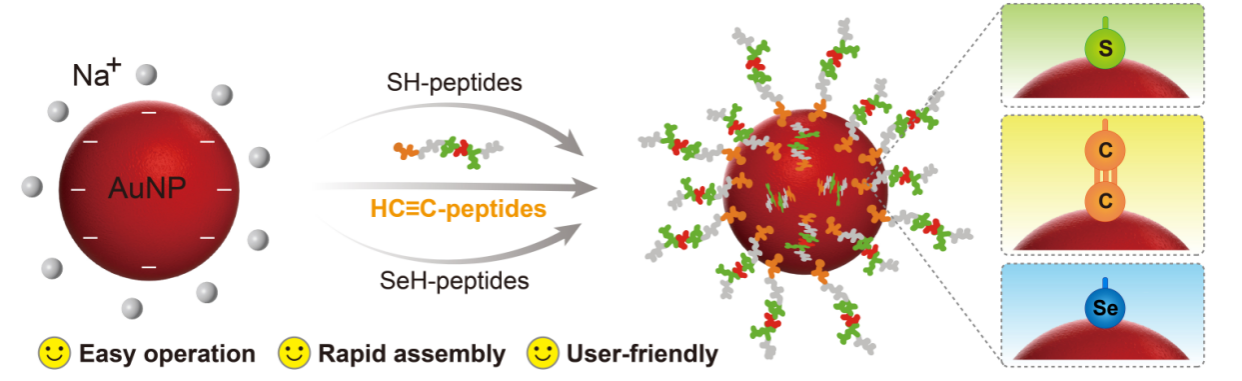
图1. 肽链纳米金探针构建
针对上述挑战,近日,湖南师范大学熊二虎教授课题组创新性地提出了基于炔基(-C≡C-)与金原子强相互作用的解决方案,开发了一种快速、稳健的肽链功能化AuNP偶联物(PFCs)构建新方法,整个偶联过程仅需两分钟即可完成(图1)。研究表明,与传统的Au-S键肽链偶联物相比,这种基于Au-C≡C键的偶联物具有显著优势:在生物硫醇抗性方面,即使在高浓度谷胱甘肽溶液中仍能保持结构完整性;在环境稳定性方面,可在高盐浓度、宽pH范围和高温条件下维持稳定性能,其稳定性与金硒(Au-Se)键肽链纳米金探针相当(图2)。值得注意的是,该探针在抗氧化性、肽链修饰成本和组装效率等方面均显著优于Au-Se键探针。
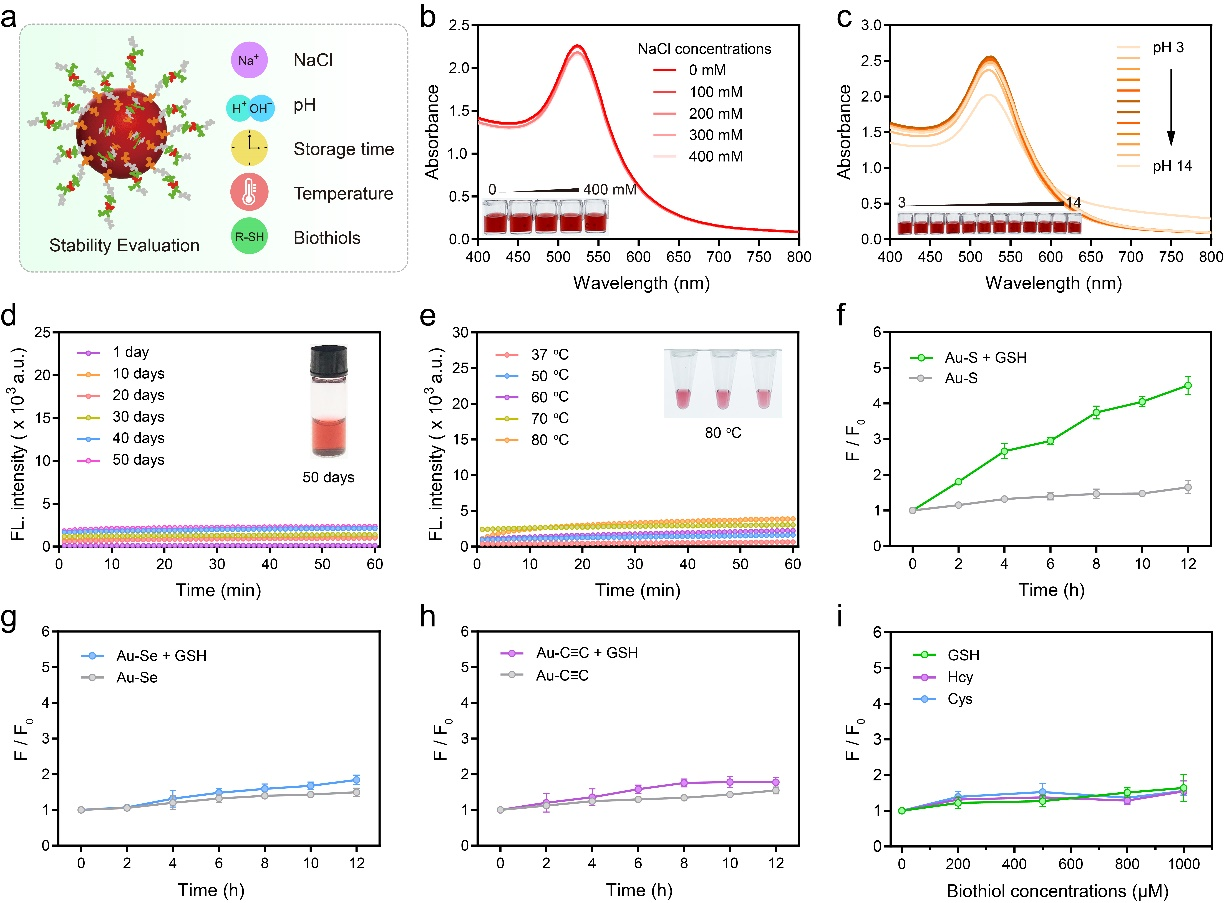
图2. 肽链纳米金探针稳定性考察
研究团队评估了基于Au-C≡C键的肽链纳米金探针在肿瘤细胞成像中的信号保真度(图3)。研究结果表明,细胞内的生物硫醇不会干扰该探针的信号输出,只有Caspase-3对探针上肽链的特异性切割才能产生有效的成像信号。这一特性显著提高了检测信号的保真度和特异性,为细胞成像分析提供了一种更为可靠的工具。
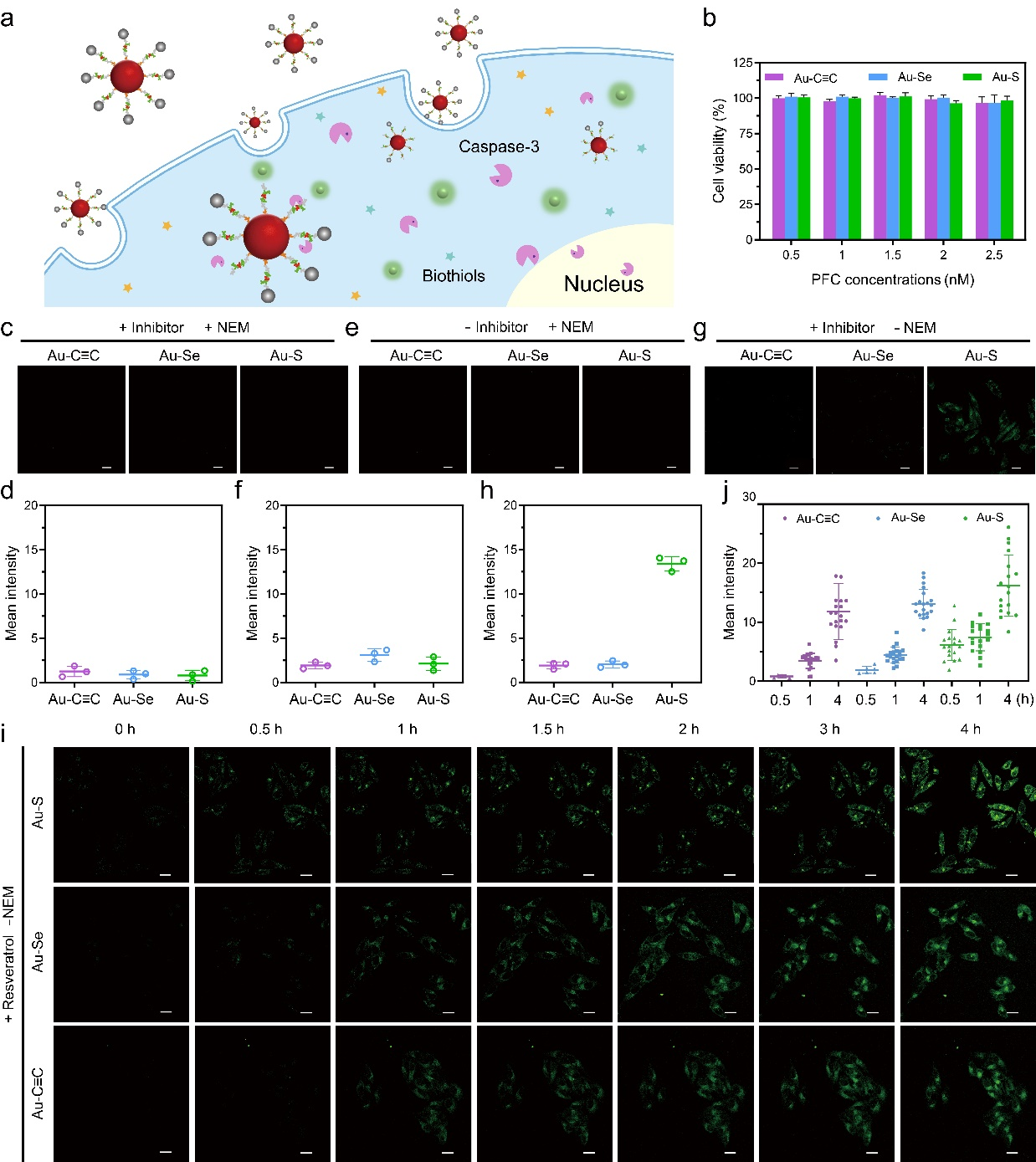
图3. 金炔键肽链纳米金探针细胞成像分析
总结与展望
该策略不仅成功解决了传统巯基肽链纳米金探针在生物硫醇环境中稳定性不足的问题,还为构建新型肽链纳米金探针开辟了全新途径,使其成为临床诊断、药物递送以及生物医学研究等生物应用领域中极具价值的重要工具。
该工作近期发表在Angew. Chem. Int. Ed.上,第一作者为湖南师范大学博士研究生都金莲和硕士研究生徐海丽,通讯作者为熊二虎教授,该工作得到了国家自然科学基金项目、湖南省杰出青年科学基金、湖南省青年科技人才计划等项目的支持。
通讯作者介绍
熊二虎,“潇湘学者”特聘教授,博士生导师,湖南大学/美国德克萨斯大学奥斯汀分校联合培养博士,湖南省杰青,湖南省青年科技人才-荷尖人才,湖南省化学化工学会第十九届青年化学化工奖,湖南省湘江新区青年科技工作者联合会理事,J. Anal. Test.和IMed期刊青年编委。目前主持国家自然科学基金面上和青年项目,以及省部级项目多项,授权中国和美国发明专利各1件,申请国家发明专利6件。近年来,共发表学术论文40余篇,其中以第一/通讯作者身份在Nat. Commun., J. Am. Chem. Soc., Angew. Chem. Int. Ed. (3篇), JACS Au, ACS Nano, Natl. Sci. Rev., CCS Chem., Sci. China Chem., Anal. Chem.(5篇)等国际权威期刊上发表论文30篇,5篇ESI高被引论文,2篇热点论文,论文总引用3260余次。研究成果发表后,受到国内外相关领域著名专家和学者的广泛关注,并在Chem. Rev., Chem. Soc. Rev., Nat. Biomed. Eng.等国际权威期刊上给予大篇幅引用和肯定性评价。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn