

通过一步操作在烯烃上引入两个官能团的反应称为烯烃的双官能团化,该反应在有机合成中具有重要用途。目前,基于自由基反应的化学选择性区域选择性实现烯烃的双官能团化反应取得了十足的进展,从机理上来讲,主要包括两种途径:一是烯烃和自由基反应后形成新的碳自由基,再和其它自由基发生连接;二是形成的碳自由基通过单电子过程被氧化形成碳正离子,再被亲核试剂捕获。带有苯基、羰基、杂原子等的双键由于p-Π共轭很容易发生双官能团化,而单独的双键即非活化烯烃的双官能团化依然面临着诸多挑战。
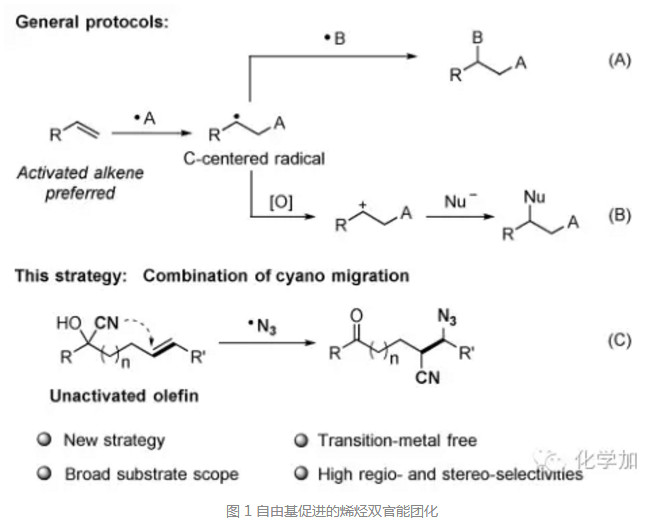
而朱晨团队则是希望通过烯烃先和叠氮自由基反应,接着氰基迁移捕获形成的碳自由基,实现双官能团化,这是一种全新的策略,没有用到过渡金属催化。

首先,作者通过条件筛选,选用了TMSN3和PIDA(醋酸碘苯)的组合来作为叠氮N3源,接着作者对底物的碳链进行了筛选,当碳链长度为1,2,3,4时,可以分别经四元环、五元环、六元环和七元环过渡态进行氰基迁移,可以看出,四元环和七元环过渡态是不利的。
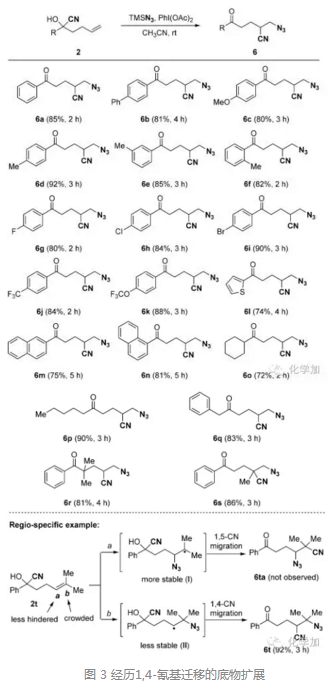
接着,作者在最佳反应条件:底物2 (0.20 mmol, 1.0 equiv), TMSN3 (0.80 mmol, 4.0 equiv), PhI(OAc)2 (0.40 mmol, 2.0 equiv) ,CH3CN (2.0 mL) 作溶剂,室温反应。十几个底物(n=2)都取得了优秀的收率,对于1,1-二取代的烯烃,也没有发现1,5-氰基迁移的产物,都得到了1,4-氰基迁移的产物,并且产率高达92%。

如图4所示,对于底物为两个非对映异构体的混合物,经由氰基迁移双官能团化后几乎得到单一产物(dr > 19 :1),而对于带有环状烯烃的非对映异构体的混合物底物,得到了单一构型的产物,这就说明该反应与底物中氰基构型无关,迁移后三级羟基都变成了羰基。
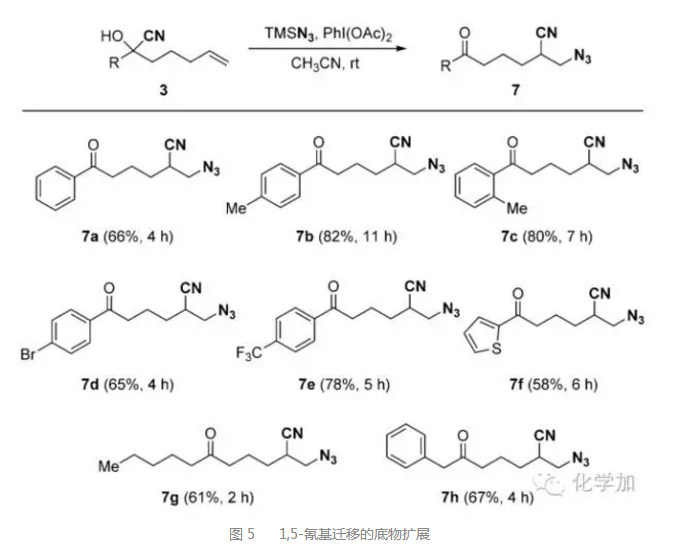
对于碳链长度为n=3的底物,经由六元环过渡态实现了烯烃的双官能团化,也是区域选择性地得到端基叠氮化合物,8个底物也都取得了中等到良好的收率。

基于实验结果,作者也提出了可能的反应机理,首先,TMSN3和PIDA生成二叠氮碘苯,失去碘苯后,生成叠氮自由基,对于双键进行加成,形成碳自由基I,接着发生氰基迁移形成新的碳自由基III,这时,有可能经PIDA氧化形成碳正离子进而形成酮羰基,也可能是III和叠氮自由基反应生成中间体V,再离去叠氮生成酮羰基。整体都是实现了对于非活化烯烃的双官能团化。
该反应的产物也是非常重要的有机合成子,产物中的叠氮可以经由Staudinger反应生成胺基,再和分子内酮羰基缩合形成环状亚胺10,也可以经由氢化后还原胺化形成取代的哌啶化合物9,这些都是有机合成中常见的骨架结构。

总结:苏州大学化学院的朱晨团队发展了一种全新的合成策略,通过叠氮化和氰基迁移实现了非活化烯烃的双官能团化,该反应条件温和,无金属参与,产率和选择性优良,底物适用性好,将在有机合成中具有重要应用。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn