

治疗性α-螺旋肽已逐渐成为治疗癌症和疾病的有吸引力的候选药物。然而,它们具有内在的弱点,包括构象稳定性差、半衰期短和体内清除快速。为了克服这些缺点,科学家提出了各种策略,包括通过共价键来固定α-螺旋肽结构的肽缝合方法。另一方面,分子伴侣在生命系统中发挥重要作用,以控制蛋白质折叠/展开并将其从部分折叠状态引导至天然结构。通过疏水片段或内部空间,分子伴侣不仅可以捕获未折叠的初始蛋白质或中间体,还可以防止蛋白质在重折叠过程中发生不可逆的聚集。在这方面,利用各种载体(如环糊精、聚合物、金属纳米颗粒、二氧化硅和自组装纳米结构)的纳米材料已被开发为人工分子伴侣。其中,多孔纳米粒子由于孔径可调、表面积大和灵活的表面修饰,在将质粒DNA、siRNA和蛋白质等生物大分子递送至靶细胞方面显示出巨大的潜力。因此,多孔纳米粒子被认为是生物医学应用中最有前途的递送载体之一,这些先前的研究启发作者开发一种基于多孔纳米粒子的肽的合成纳米伴侣系统(SNCP),作为一种纳米反应器用于辅助治疗性α-螺旋肽的正确折叠和细胞内肽递送(Fig. 1)。
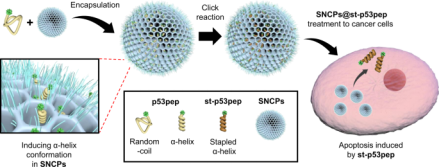
Fig. 1: 基于多孔纳米粒子的肽合成纳米伴侣(SNCP)的示意图(图片来源:Nat. Commun.)
为了应用人工伴侣系统,作者选择了一种合成的p53肽(p53pep)作为模型治疗肽。它来源于转录因子p53蛋白的15个残基α-螺旋反式激活结构域,该结构域可诱导细胞凋亡以响应细胞应激。这个α-螺旋结构域与MDM2癌蛋白的深疏水裂隙结合,作为细胞抑制剂调节p53蛋白水平。首先,作者根据先前报道的方法制备了介孔二氧化硅纳米粒子,并在此基础上进行改进构建了SNCP的纳米反应器(Fig. 2a)。
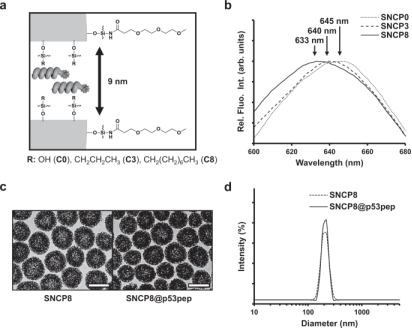
Fig. 2: SNCP的设计和表征(图片来源:Nat. Commun.)
为了使SNCP的内部环境更加疏水,作者在SNCP的内表面上引入脂肪链,并用尼罗红试验进行了验证(Fig. 2b)。结果表明,在SNCPs内表面引入脂肪链官能团增加了其内部环境的疏水性,这可能影响封装肽与SNCPs之间的相互作用,使具有脂肪链修饰的SNCP对p53pep表现出更高的负载能力。受成功的表面改性结果和SNCP特性的鼓舞,作者通过在水性条件下简单搅拌p53pep和SNCP的混合物,制备了p53pep封装的SNCP用于后续功能研究,并用TEM和DLS进行了一系列的证明(Fig. 2c, d)。
在SNCPs控制p53pep的α-螺旋构象和稳定性方面,作者应用圆二色(CD)光谱进行了表征,结果表明p53pep根据SNCPs的内表面环境形成不同的二级结构(Fig. 3a),且与SNCP0和SNCP3相比,SNCP8中的疏水环境更有利地促进封装的p53pep形成α-螺旋结构。封装在SNCPs内的α-螺旋肽p53pep的结构构象受到SNCP内表面疏水性的精细控制(Fig. 3c)。此外,α-螺旋肽与SNCPs内表面之间的疏水相互作用在提高α-螺旋肽的热稳定性方面起着关键作用(Fig. 3d)。
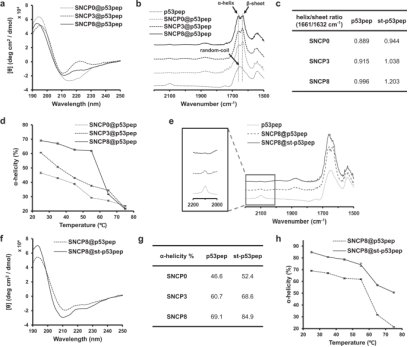
Fig. 3: 肽二级结构分析(图片来源:Nat. Commun.)
为了使p53pep在从SNCP释放后也保持不可逆的α-螺旋结构,作者使用铜(I)催化的叠氮化物-炔烃环加成(CuAAC)反应的点击肽装订方法合成了st-p53pep。CD光谱和FT-IR表征结果表明,三唑键形成降低的构象自由度增强了α-螺旋肽的二级结构(Fig. 3c, e, f, g)。SNCP8分子伴侣根据内孔表面的疏水性增加了肽的结构和热稳定性。最后,作者选择 SNCP8作为稳定p53pep的螺旋构象的最合适的分子纳米反应器,并将其用于体外和体内的进一步研究。
在SNCP作为抗癌肽递送载体的功效方面,数据表明目前的SNCP8@st-p53pep很容易被HepG2细胞吸收,并且随着时间的推移,负载的st-p53pep在细胞内从SNCP8释放,表明其作为肽的细胞内递送载体的潜力(Fig. 4)。
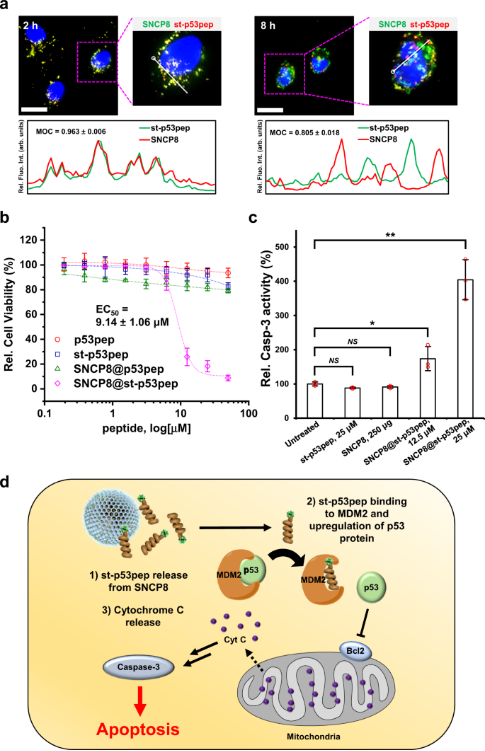
Fig. 4: 细胞实验和细胞凋亡研究(图片来源:Nat. Commun.)
在SNCP8@st-p53pep的细胞毒性方面,SNCP8@st-p53pep组表现出了较强的细胞毒性并呈现浓度依赖性,并且SNCP处理组也没有观察到细胞活力的显著降低。结果表明,st-p53pep和SNCP8的协同作用成功地诱导了细胞毒性,而不是单独使用SNCP8@p53pep或肽(Fig. 4)。细胞毒机制的研究表明SNCP8@st-p53pep通过p53依赖性途径诱导癌细胞的凋亡(Fig. 4d)。
最后,作者使用人肝癌(HepG2)异种移植小鼠模型评估了SNCP8@st-p53pep的体内治疗功效。SNCP8@st-p53pep治疗组的肿瘤生长被显著抑制,而单独的SNCP8或st-p53pep组与未治疗的对照组相比,肿瘤体积的生长没有显著差异(Fig. 5a)。这些结果表明SNCP8@st-p53pep对肿瘤生长具有抑制作用,并且SNCP8可以作为小鼠模型中治疗性抗肿瘤肽的有效递送载体。st-p53pep在体内进一步的可持续性分析研究表明,SNCP8不仅作为纳米反应器使p53pep的构象更稳定,而且还作为肽载体将st-p53pep递送至肿瘤组织和癌细胞,可持续释放st-p53pep并有效诱导p53介导的体内细胞凋亡(Fig. 5)。
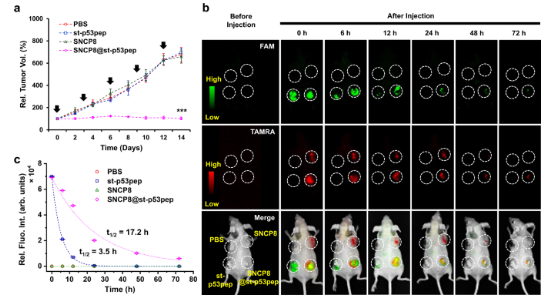
Fig. 5: SNCP8@st-p53pep在肿瘤小鼠模型和SNCP8@st-p53pep 治疗小鼠全身成像中的治疗效果研究(图片来源:Nat. Commun.)
总结:
综上所述,Dal-Hee Min等开发了一种基于多孔纳米颗粒SNCP的合成肽纳米伴侣,并证明了其在稳定和功能性递送治疗性α-螺旋肽以控制癌症生长方面的多种功能。SNCP的多功能性使其在目的肽的构象稳定性及其细胞内递送中表现出高度吸引力,该系统为未来各种肽疗法提供了比较有前景的应用平台。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn