- 首页
- 资讯
Angew:一锅法序贯立体选择性催化合成阻转异构酰肼
来源:化学加网原创 2022-09-13
导读:近日,意大利博洛尼亚大学Giorgio Bencivenni教授课题组实现了首例阻转异构酰肼的对映选择性和非对映选择性合成。该方法在一锅反应中实现了两个有机催化循环,其特征在于支链醛的烯胺胺化,然后在相转移条件下进行氮烷基化,得到了对映体富集的阻转异构体酰肼。同时该方法可以通过两种不同催化剂的组合以立体发散的方式得到全部四种立体异构体。
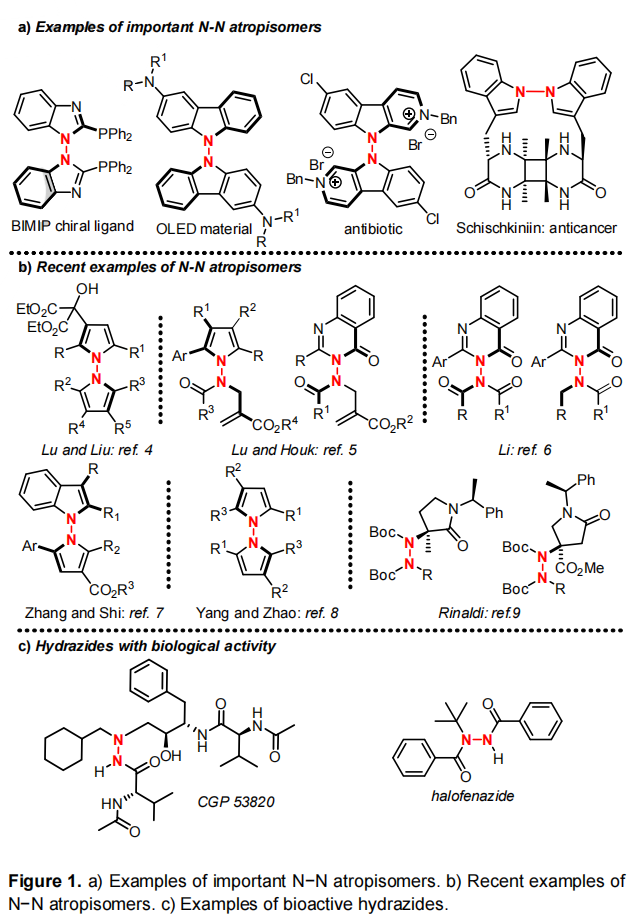
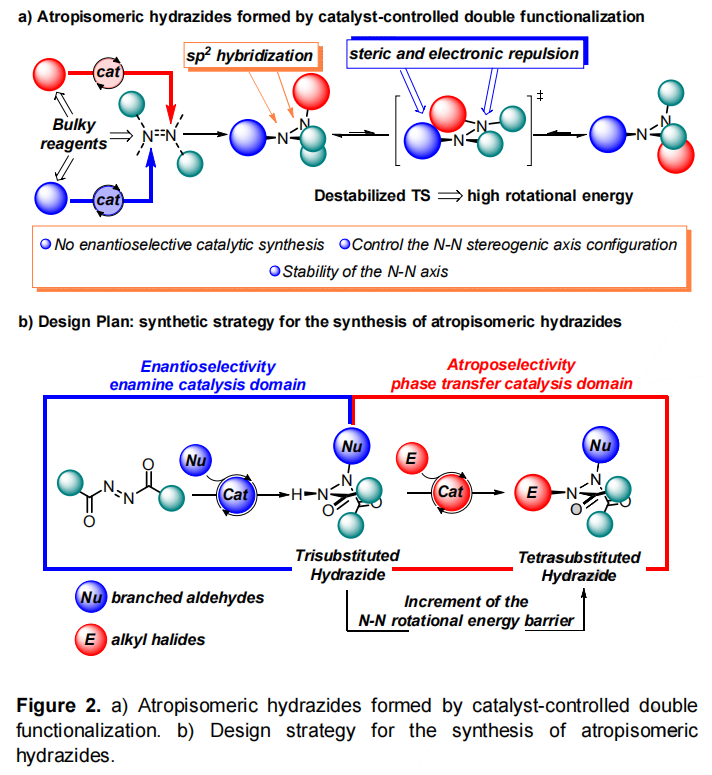
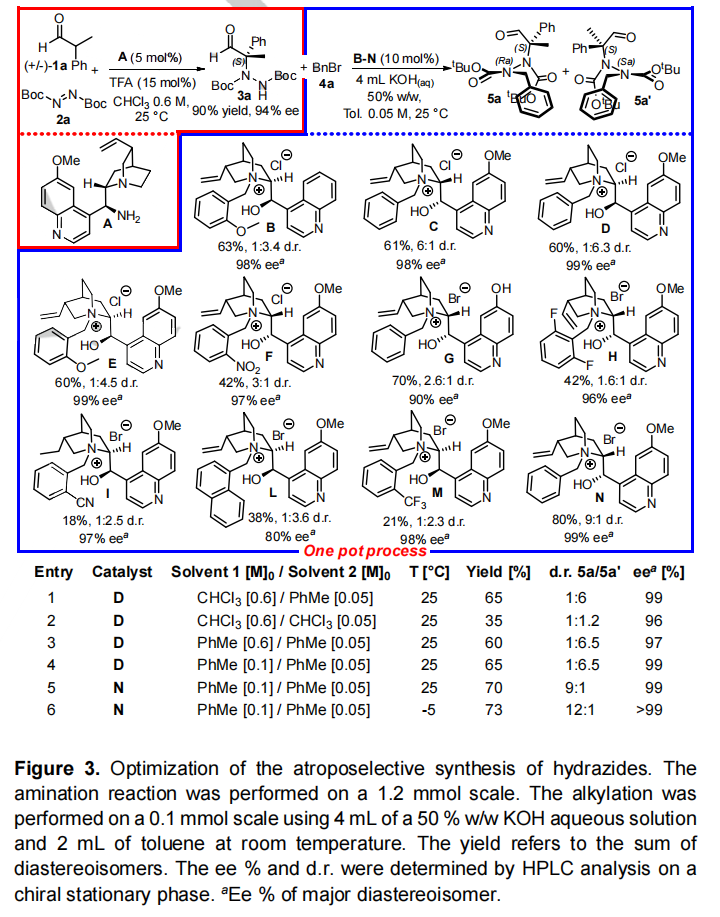
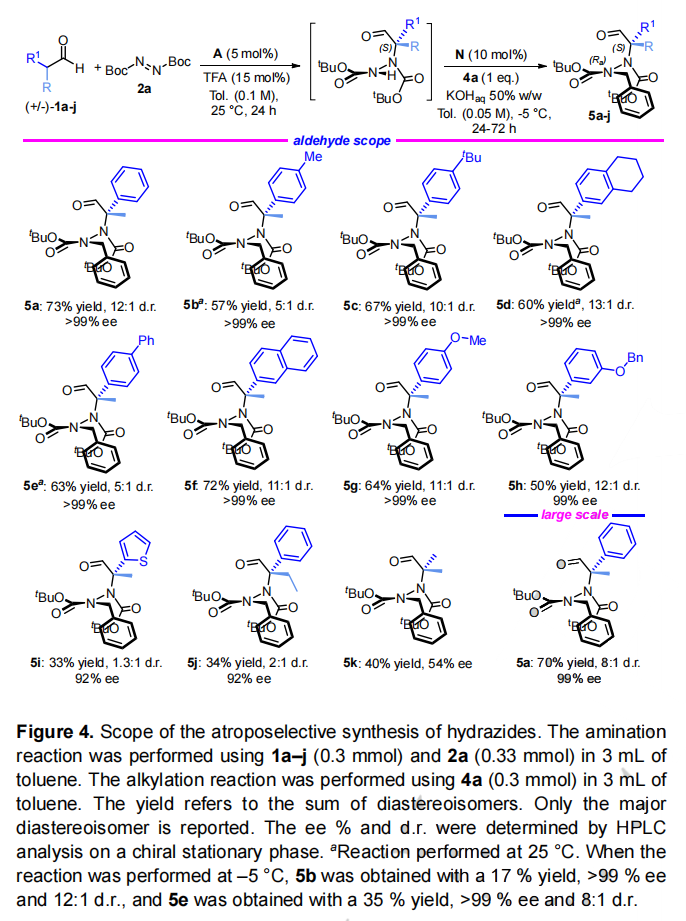
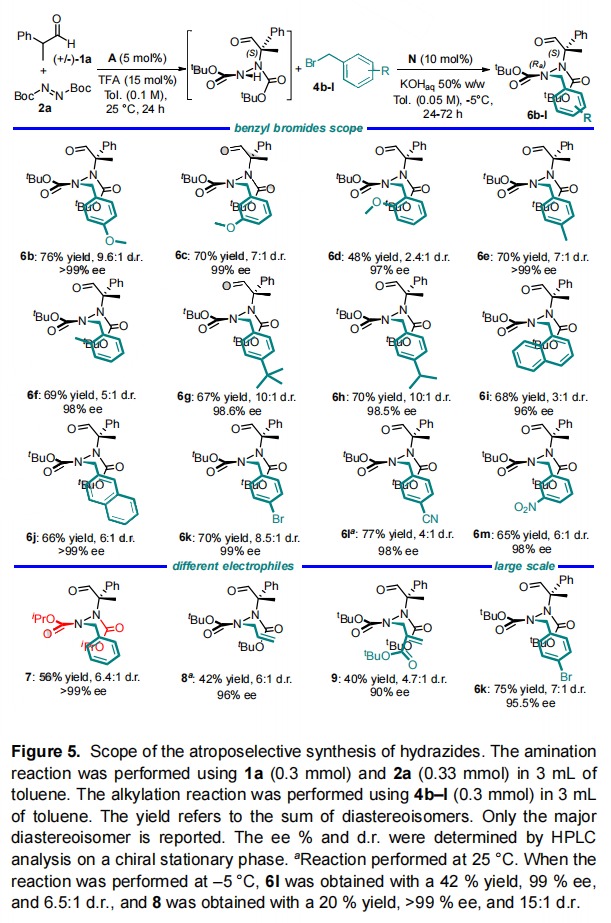
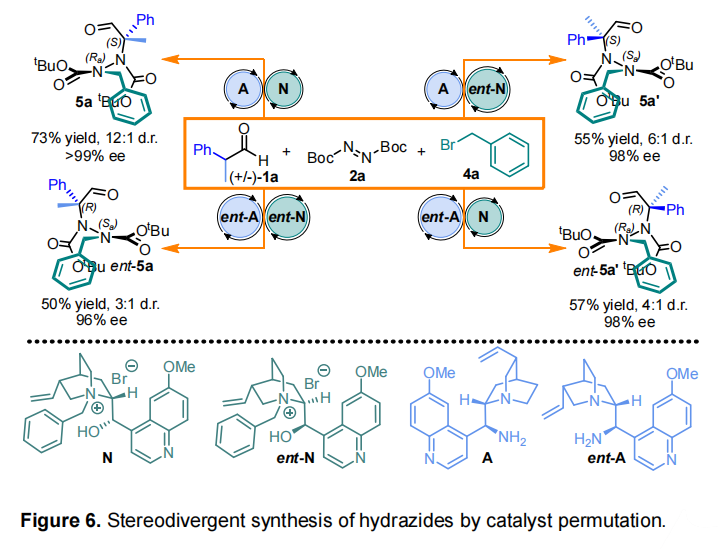
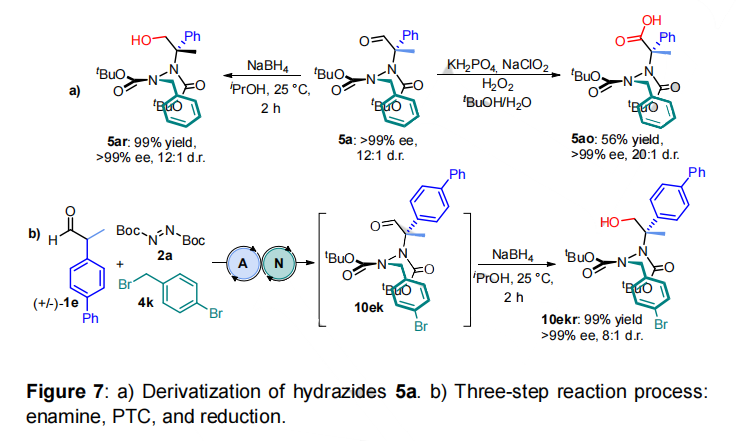
图片来源:Angew. Chem. Int. Ed.由于轴手性分子广泛存在于天然活性产物和功能材料中,近年来,对于阻旋异构体的不对称合成受到研究人员的广泛关注。然而,目前可行的催化方法主要是C-C 和C-X阻转异构体(X=N、S、O)的构建,这极大地限制了阻转异构体库的建立。虽然N−N阻转异构体在生物活性分子、功能材料和手性配体中有着较多的应用(Fig. 1a),但其不对称合成方法鲜有报道,仅有青岛大学刘人荣团队通过去对称化合成了双吡咯阻转异构体;新加坡国立大学卢一新课题组和南开大学李鑫团队利用动态动力学拆分策略合成氨基吡咯和氨基喹唑啉酮衍生物;新加坡国立大学赵宇课题组和江苏师范大学石枫课题组利用原位构环合成N-N轴手性吲哚和吡咯。最近,Rinaldi分离出一种稳定的阻转异构酰肼作为制备氨基酸等排体和构象受限的γ-内酰胺的中间体(Fig. 1b)。而酰肼是一类生物活性化合物,例如HIV-1和HIV-2蛋白酶抑制剂氮杂肽类似物CGP 53820、环境安全的杀虫剂卤虫酰肼 (Fig. 1c)。因此,Giorgio Bencivenni课题组将注意力集中在第一个有机催化合成轴向手性酰肼上。作者研究了阻转异构酰肼是否可以在温和反应条件下通过有机催化控制立体轴构型来制备,理想情况下,利用合适位阻和电性的试剂可以实现这种手性控制,即通过旋转过渡态(TS)的不稳定来保证N-N单键的高旋转稳定性(Fig. 2a)。图片来源:Angew. Chem. Int. Ed.作者提出了一种合理的催化策略包括使用偶氮二羧酸盐作为N-N单键的前体(Fig. 2b),该策略包括两个不同的催化步骤,依次增加N-N单键周围的空间位阻,最终产生旋转稳定的手性四取代酰肼。第一步,偶氮二羧酸盐发生亲核加成反应生成三取代酰肼;第二步,氮原子的烷基化得到旋转受阻酰肼。因此,作者提出了第一个对映选择性和非对映选择性合成阻转异构酰肼的方法,即结合两个立体选择性步骤:1)烯胺催化的支链醛的α-胺化,2)相转移(PT)条件下的氮烷基化。最终作者实现了多组分一锅法序列有机催化剂控制的立体发散多手性控制。图片来源:Angew. Chem. Int. Ed.作者首先通过外消旋2-苯基丙醛(1a)与偶氮二甲酸二叔丁酯 (DTBA)(2a)在氯仿中使用9-脱氧奎尼丁(A)作为催化剂,TFA 作为助催化剂反应得到3a,其具有90%的收率和94% ee。接着使用苄基溴4a作为烷基化剂对PT催化剂进行筛选,其中金鸡纳生物碱衍生物B-N催化效果最优(Fig. 3)。作者进而对两步反应进行一锅法测试,对反应条件进行筛选,最终得到最优反应条件:第一步以A作为催化剂,第二步以N作为催化剂,温度为-5 oC条件下,在甲苯溶液中在甲苯中反应,两步总收率为73%,ee值为 >99%, dr值为12:1(Fig. 3 entry 6)。接着,作者对底物的普适性进行了考察。首先对醛上的取代基进行改变来制备对应的酰肼(Fig. 4)。图片来源:Angew. Chem. Int. Ed.该方法适用于有不同芳基取代基的支链醛。当使用具有富电子烷基(5b-d)、芳基(5e-f) 和氧代烷基 (5g-h)基团的芳基时,具有良好的反应性。在大多数情况下,反应得到高产率、高对映选择性和非对映体控制。但是,使用带有杂芳族取代基的醛时,产率较低(5i),当甲基被乙基取代时产率也较低。为了将烷基化的产率提高,作者使用了过量的4a(5j)作为底物。令人意外的是,p-Cl-、o-Br-或o-NO2-取代芳环与具有两个烷基的支链醛一起反应时,酰肼中间体在烷基化步骤中会分解。作者还尝试在该过程的第一步中使用异丁醛1k对映选择性合成四取代酰肼,得到的阻转异构体5k的产率为 40%,ee值为 54%,结果表明,该方法的适用范围可以扩大到其它手性酰肼。该方法还可以放大到3.0 mmol规模。不仅如此,作者还对不同的苄基亲电试剂进行了普适性考察(Fig. 5)。图片来源:Angew. Chem. Int. Ed.作者通过该反应以高产率和优异的对映选择性获得了酰肼6b-l。供电子甲氧基作为苄基芳环上的邻位、间位和对位取代基具有良好的耐受(6b-d)。此外,不同大小的烷基具有良好的产率和高立体控制(6e-g)。不仅如此,1-和2-(溴甲基)萘以及具有吸电子取代基的苄基溴也具有良好的反应结果(6i-l)。为了扩大反应的一般范围,作者还探索了不同亲电试剂的反应性:偶氮二甲酸二异丙酯可代替DTBA (7),烯丙基碘(8)和Morita-Baylis-Hillman碳酸盐(9)可以作为烷基化反应底物。在放大反应中,可以做到2.5 mmol规模,得到相应的6k酰肼,具有良好的收率和对映选择性。图片来源:Angew. Chem. Int. Ed.作者还通过顺序接力催化得到了整套反应的立体异构体。如Fig. 6所示,可以通过催化剂置换获得所有四种立体异构体,得到良好的收率和立体异构体比率(Fig. 6)。图片来源:Angew. Chem. Int. Ed.不仅如此,作者通过还原和氧化5a来探索阻转异构酰肼的衍生化,得到相应的醇5ar(63%, > 99% ee)和酸5ao(56%, >99 % ee)。作者还尝试直接从粗混合物中衍生化,通过三步反应过程,以高收率和良好的立体选择性得到醇10ekr(Fig. 7)。
Giorgio Bencivenni课题组首次使用基于对映选择性和非对映选择性顺序有机催化的方法,高效且简单的一锅法合成了阻转异构酰肼。这种方法结合了两个催化步骤,每个步骤都致力于构建特定的手性元素,以立体发散的方式得到了所有可能的立体异构体。
文献详情:
Chiara Portolani, Giovanni Centonze, Sara Luciani, Andrea Pellegrini, Paolo Righi, Andrea Mazzanti, Alessia Ciogli, Andrea Sorato, Giorgio Bencivenni*. Synthesis of Atropisomeric Hydrazides by One-Pot Sequential Enantio- and Diastereoselective Catalysis. Angew. Chem. Int. Ed. 2022, https://doi.org/10.1002/anie.202209895
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn