

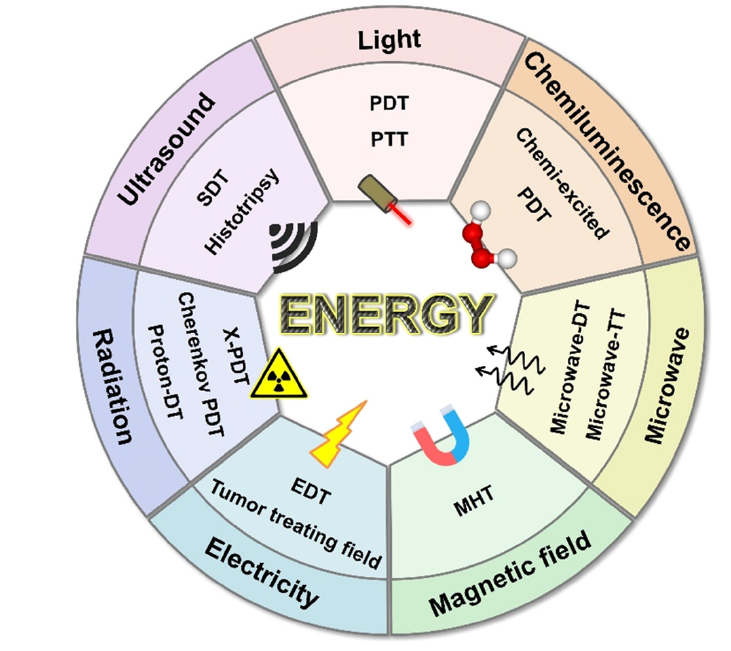
图1. 用于癌症治疗的不同激发策略(图片来源:Chem. Soc. Rev.)
1.PTT、PDT作用机制:
PDT是一种临床确立的肿瘤学干预措施,它依赖于光介导的光敏剂(PS)活化以产生活性氧(ROS)。在光照射下,激发的PS经历系统间穿越。由于三重态的寿命较长,因此系统间穿越速率高并产生活性氧。对于I型PDT,激发的PS将电子转移到周围的分子并产生自由基。相反,II型PDT涉及向三线态氧的能量转移,受激发的分子氧转化为单线态氧。PS在靶肿瘤中的蓄积以及充足的分子氧供应是PDT的先决条件。但光对组织的穿透力非常有限(仅有10 mm),对于深层组织处的肿瘤难以造成致命伤害,同时肿瘤微环境乏氧且渗透性低。
PTT是指光热剂通过非辐射弛豫释放热量,从而对癌症进行热消融。PTT治疗过程产生的副作用较小,全身系统毒性低,不会对正常组织造成损伤,具有很大的临床应用潜力。有效的PTT可通过阻断与热和修复相关的特定基因来提高光热转换效率以产生更多热量和降低癌症的热耐受性。但光热剂在人体内流通情况也并没有完全搞清楚,也没有进行长期的实验观察,对于其潜在毒性还得继续摸索。
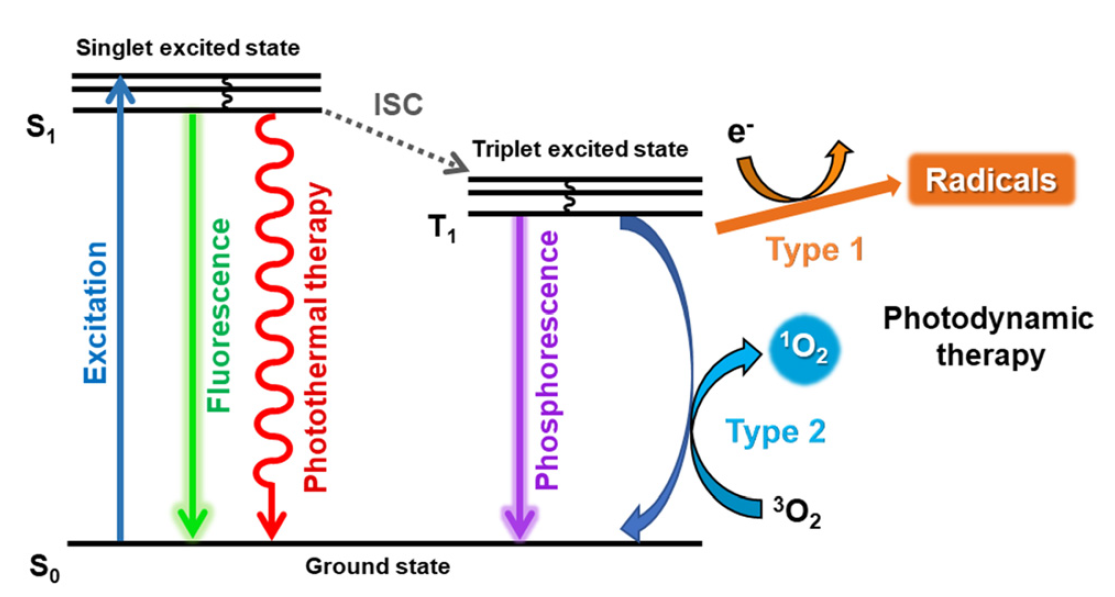
图2. PDT以及PTT机制示意图(图片来源:Chem. Soc. Rev.)
2.SDT及HIFU作用机制:
超声是一种频率>20 kHz的机械波,需要弹性介质传输能量,由于其非侵入性方式和深层组织穿透能力,已广泛应用于临床领域。SDT是基于超声发展起来的新兴无创治疗方法,尽管SDT产生活性氧的机制仍有争议,但目前主要认为超声与水介质相互作用,引发“空化”作用,空化气泡的连续坍缩产生声致发光,同时在周围的微环境中产生巨大的热量和压力,激活声敏剂,促使其产生活性氧杀伤细胞。然而,大多数声敏剂的生物安全性和ROS产生率较低,使其疗效还不足以取代传统的抗肿瘤治疗方法,因此SDT尚未在临床上得到广泛应用。此外,虽然SDT解决了光动力疗法低穿透的问题,但仍会导致肿瘤缺氧而阻碍其效率的提高,因此,保障肿瘤部位充足的氧气供应仍然是一个需要解决的问题。
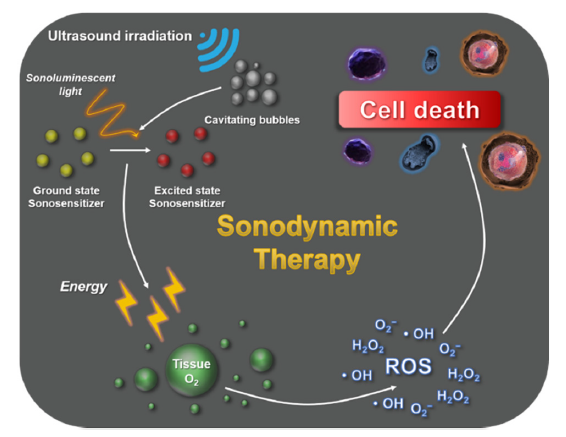
图3. SDT机制示意图(图片来源:Chem. Soc. Rev.)
HIFU原理是利用超声波能够无损伤的穿透人体组织,并且在体内聚焦,产生热效应(主要效应)、空化效应、机械效应等;焦点的温度可以达到60-100 ℃,从而导致焦点处的组织发生凝固性坏死,而不损伤焦点外的正常结构。近年来,HIFU在免疫治疗领域引起了极大的关注,尽管HIFU的免疫机制仍有争议,但主要认为超声导致的变性抗原蛋白的消失而引发免疫反应。
3.CL PDT机制
化学发光是一种在室温下将化学能转化为光能的化学现象,其反应体系多以草酸酯、过氧化氢(H2O2)以及荧光染料为主要组成部分,自发光波长通常由所采用的荧光染料的性质所决定。草酸酯受H2O2激发产生自发荧光,与荧光成像相比,其具有相对较深的穿透深度和较高的信噪比(S/N)。同时研究发现,其同时可产生化学能,诱导PS激发从而产生ROS。控制肿瘤区域附近CL的激活是取得更好治疗效果的关键点。如果化学反应在PS到达肿瘤之前开始,产生的ROS会影响正常组织。如果反应速度不足以产生足够量的ROS,则细胞内抗氧化成分会降低治疗效果。相比于直接激发,间接化学发光激发PS的PDT有以下几个优点:一、通过光转换纳米颗粒,PS可以被高效递送到肿瘤区域;二、多种激发光源增加了组织穿透能力;三、不管是常氧肿瘤还是乏氧肿瘤均能通过I型PDT来实现高效治疗。
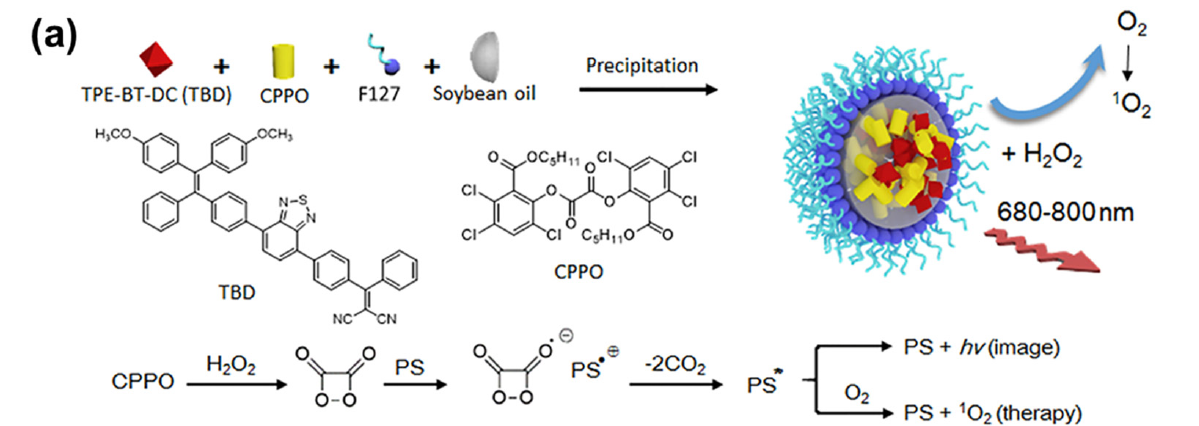
图4. CL PDT机制示意图(图片来源:Chem. Soc. Rev.)
4.X-PDT、CR PDT机制
基于X-射线直接激发PS或以X-射线激发纳米闪烁体作为能量传递介质间接激发PS的X射线激发的X-PDT成为深层肿瘤治疗领域的另一研究热点。X-射线激发发光纳米粒—PS耦合系统可提高ROS的产生率,从而有效提升了肿瘤的治疗效果。目前,用于X-PDT的纳米材料主要有基于稀土金属闪烁发光纳米粒和基于金属硫/氧化物(金属)半导体发光纳米粒。
CR PDT是一种不需要外界光激发的新型光动力疗法。通过放射性核素产生的切伦科夫辐射激活附近的PS,使其产生ROS以破坏靶细胞或组织,它克服了传统PDT存在的组织渗透受限、依赖外部光等缺点,是一个很有前景的新领域。切伦科夫辐射比较微弱、易被生物组织衰减、缺乏对应光谱的PS以及肿瘤靶向性不佳是限制其在临床进一步应用的关键因素。如何增强基于切伦科夫辐射的光动力治疗疗效是未来的研究重点。
5.MDTT机制
微波是指频率为300 MHz-3000 GHz的电磁波,MIPDT是一种新的癌症治疗方法,与传统PDT相比,其具有更快的消融时间和可忽略的副作用。相对磁导率、介电常数和阻抗匹配是定义微波吸收特性的主要参数。其中,离子限制效应影响金属有机框架(MOF)中的微波热效应。有限空间中离子碰撞比在自由空间中更频繁地发生;因此,MOF微孔中的多次碰撞有利于将微波电磁能转化为热能。MIPDT有两种不同的机制。在液态金属中,微波诱导液态金属中的电子转移,其中电子与不同分子的反应产生ROS。在掺杂有过渡金属的MOF中,由于在微波照射下电子-空穴对的发生分离,自由电子与分子氧发生作用产生1O2。
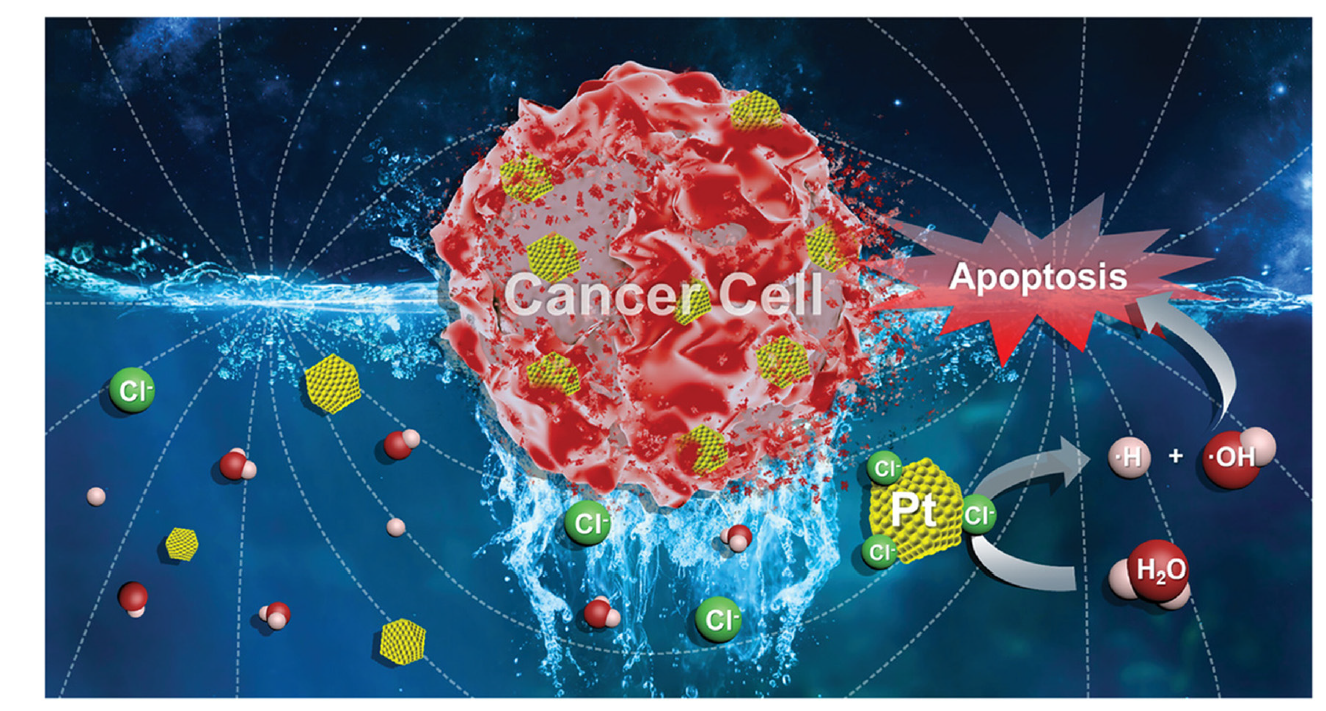
图5. MDTT机制示意图(图片来源:Chem. Soc. Rev.)
总结
近年来,已经开发了各种能量驱动的癌症治疗方法。然而,目前只有PDT、SDT和TTF少数能源用于临床试验。PDT广泛用于治疗浅表肿瘤。SDT虽然未获得FDA的批准,但它已在欧洲和日本得到应用。此外,医生在临床试验中并未使用单一疗法,而是使用鸡尾酒疗法,通过互补效应增强整体临床结果。
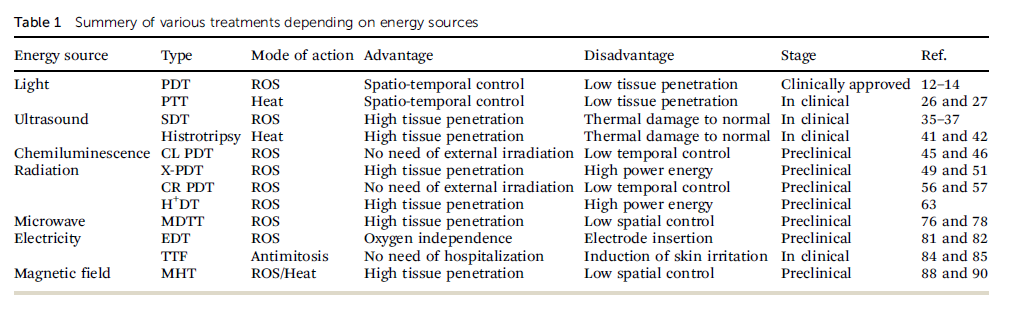
表1. 各种能量驱动的癌症治疗方法的临床进展(图片来源:Chem. Soc. Rev.)
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn