

(图片来源:J. Am. Chem. Soc.)
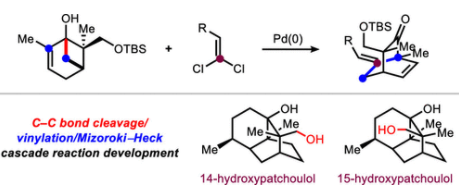
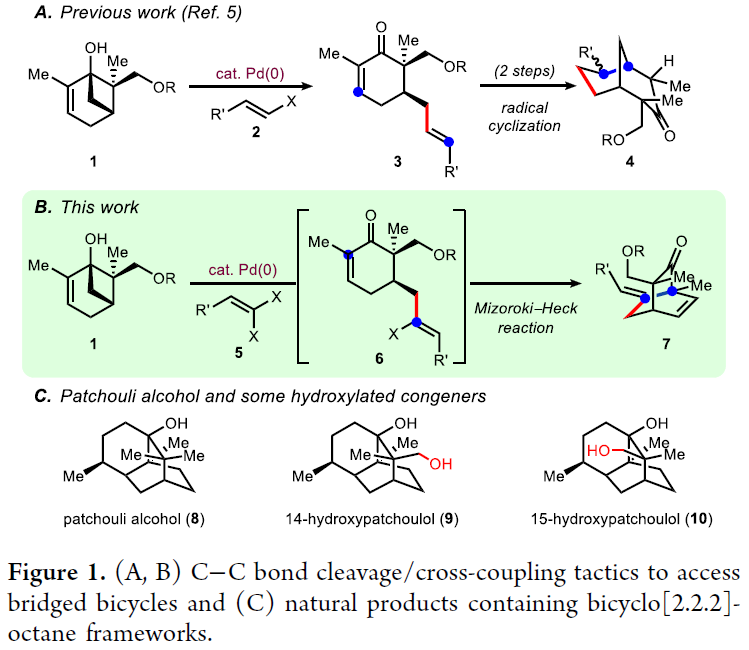
利用过渡金属催化C-C键的断裂与交叉偶联反应的结合被认为是一种从简单的合成砌块快速构建复杂分子强有力的手段。而如果将此策略应用于全合成中则可以高效的实现一系列复杂天然产物分子构建。Richmond Sarpong课题组曾发展了钯催化二羟基蒎烯衍生物(e.g., 1, Figure 1A)的C-C键的断裂/交叉偶联反应,实现了官能团化环己烯酮衍生物的制备(1→3)。而得到的环己烯酮可以通过自由基环化策略实现xishacorene B的全合成。总的来说,利用这种“手性源”重塑策略,使用现有对映体富集的小分子(如香芹酮)来实现复杂天然产物分子的合成具有重要意义。最近,美国加利福尼亚大学伯克利分校Richmond Sarpong课题组发展了钯催化环丁醇衍生物与偕二氯烯烃的C-C键断裂/烯基化/Mizoroki−Heck串联反应,实现了官能团化双环[2.2.2]辛烷骨架的构建。此外,作者利用此方法通过12步反应高效实现了具有重要应用价值的天然产物14-hydroxypatchoulol和15-hydroxypatchoulol的全合成(Figure 1B,1C)。
(图片来源:J. Am. Chem. Soc.)
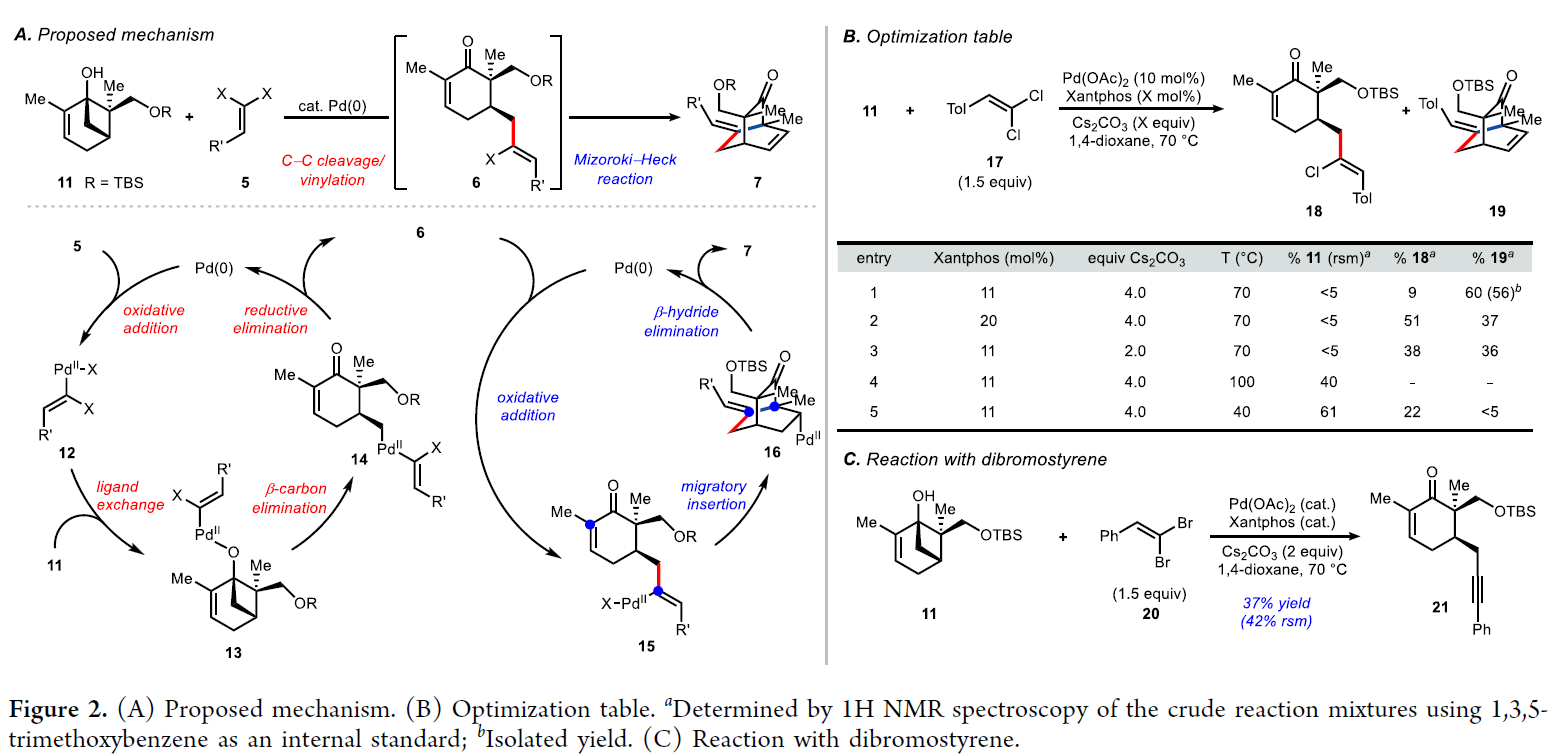
从机理上推测,作者认为此转化可能包含两个Pd(0)/(II)催化循环过程。首先,Pd(0)络合物与偕二氯化物5发生氧化加成得到Pd(II)物种12。随后,其与环丁醇衍生物11发生配体交换得到Pd(II)物种13,并经历β-C消除得到烷基取代的Pd(II)络合物14。接下来,14通过还原消除得到烯基氯产物6并再生Pd(0)物种完成第一个催化循环。另一个催化循环始于Pd(0)与6的氧化加成得到Pd(II)中间体15。随后15通过与烯酮部分发生分子内的迁移插入得到含有双环[2.2.2]辛烷骨架的Pd(II)物种16。最后,16通过β-H消除得到目标产物7并再生Pd(0)物种完成第二个催化循环(Figure 2A)。
作者首先以环丁醇衍生物11和偕二氯苯乙烯17作为模板底物进行了反应探索(Figure 2B)。经过一系列条件筛选后,作者发现当使用11(1.0 equiv),17(1.5 equiv),Pd(OAc)2 (10 mol%),Xantphos (11 mol%),Cs2CO3 (2.0 equiv),1,4-二氧六环,70 oC反应可以以60%的核磁产率(56%的分离产率)实现双环[2.2.2]辛烷产物19的合成(Figure 2B,entry 1)。此外,当作者尝试使用具有更高反应活性的偕二溴化物20参与反应时,仅以37%的产率得到了炔烃加合物21为主要产物(Figure 2C)。
(图片来源:J. Am. Chem. Soc.)
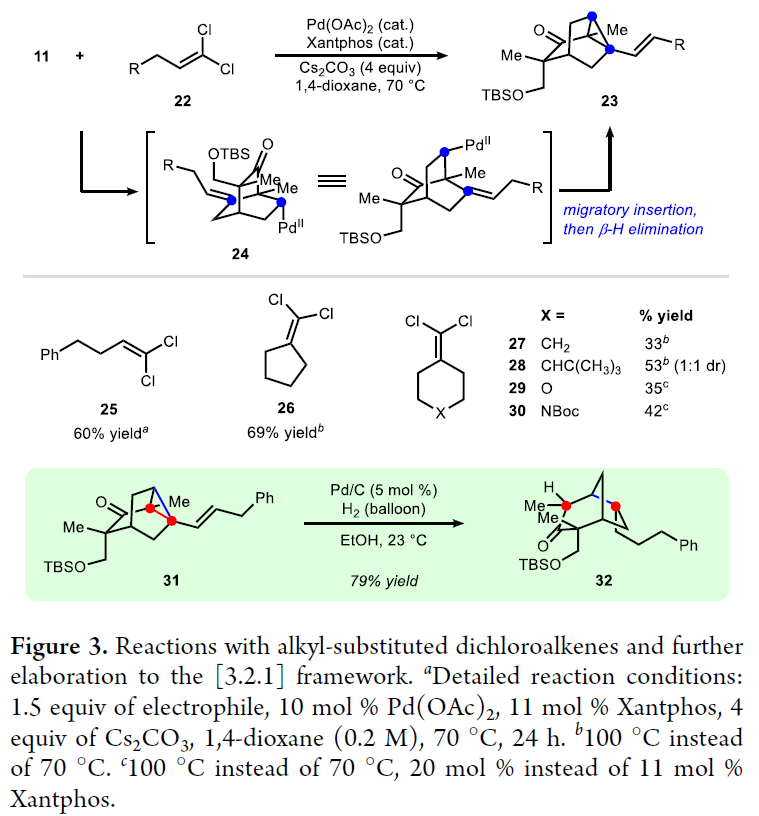
随后,作者探索了烷基偕二氯化物在此反应过程中的反应性。实验结果表明,烷基取代的偕二氯化物在此反应条件下可以以中等产率实现三环[3.2.1.0]辛烷25-30的合成。这主要是由于在烷基偕二氯烯烃参与的反应过程中,其在发生β-H消除过程之前会发生两次连续的碳-钯化反应,从而由24得到产物23。而对于前面讨论的芳基取代的偕二氯烯烃则不可能发生此类过程。此外,产物31中的烯基环丙烷部分可以经历氢化过程(Pd/C,H2)得到双环[3.2.1]辛烷产物32。尽管通常金属络合物会实现烯基环丙烷中取代较少C-C键的断裂,但在是此反应中却实现了烯基环丙烷中取代较多C-C键的断裂。这主要是由于钯在亲核进攻烯基环丙烷后得到的π-烯丙基钯物种会选择性的在更容易接近的凸面上发生质子化和氢化过程,因此会专一性的得到产物32(Figure 3)。
(图片来源:J. Am. Chem. Soc.)
接下来,作者希望利用发展出的方法实现15-hydroxypatchoulol 10的全合成。逆合成分析表明,patchoulol骨架可以通过33的分子内aldol反应来构建。而利用发展出的方法通过1和34的偶联则可以实现33的合成(Scheme 1A)。于是,作者首先利用缩酮保护的35与环丁醇衍生物11偶联以53%的产率实现了双环[2.2.2]辛烷骨架36的合成(Scheme 1B),并利用36来实现15-hydroxypatchoulol 10的全合成(Scheme 2A)。

(图片来源:J. Am. Chem. Soc.)
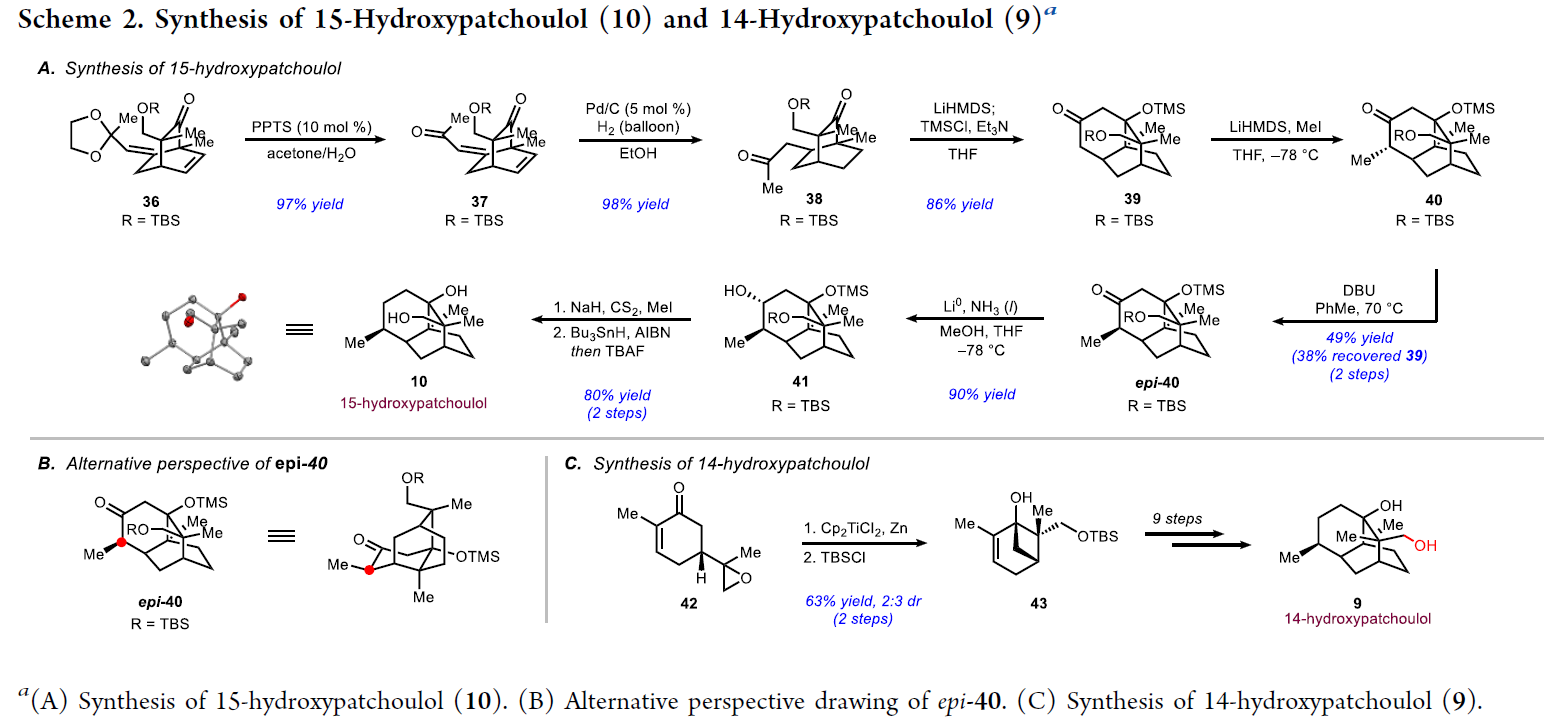
首先,36中的羰基保护基可以在PPTS作用下实现脱除得到烯酮37。随后,37通过氢化(Pd/C,H2)过程以良好的非对映选择性得到全饱和产物38(98%)。接下来,38在过量LiHMDS存在下发生环化得到aldol产物后通过与TMSCl反应得到相应的硅醚产物39。在此过程中,作者发现反应中羟基的保护至关重要,其可以有效避免碱性条件下的逆aldol反应的发生。随后,39选择性的在凸面实现了羰基的α-甲基化过程,得到了40为主要产物(非目标中间产物)。接着作者在70°C下,通过DBU介导的热力学差向异构化过程得到了甲基构型翻转的产物epi-40(目标中间产物)(Scheme 2B)。然而,最后一步脱羰基过程则具有一定的挑战性,作者分别尝试了Wolff−Kishner还原以及Caglioti和Myers的改进方法均未成功。此外,作者尝试将羰基转化为硫羰基或缩硫酮后再还原也未取得成功。最终,作者通过将epi-40中的羰基还原为羟基得到产物41,并通过Barton-McCombie脱氧反应实现了形式上的脱羰基过程得到了产物15-hydroxypatchoulol 10,并且产物10的结构通过单晶衍射得到进一步证实(Scheme 2A)。此外,作者还利用类似的方法实现了14-hydroxypatchoulol 9的合成(Scheme 2C)。
(图片来源:J. Am. Chem. Soc.)
总结 美国加利福尼亚大学伯克利分校Richmond Sarpong课题组发展了钯催化环丁醇衍生物与偕二氯烯烃的C-C键断裂/烯基化/Mizoroki−Heck串联反应,高效实现了官能团化双环[2.2.2]辛烷骨架的构建。当使用烷基偕二氯烯烃作为偶联配偶体时,此过程还可以实现三环[3.2.1.0]辛烷产物的合成。此外,作者还利用此方法通过12步反应高效实现了具有重要应用价值的天然产物14-hydroxypatchoulol和15-hydroxypatchoulol的全合成。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn