


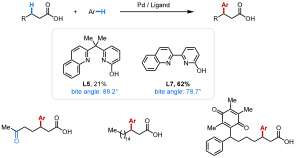
近些年来,过渡金属催化的C-H键活化已经逐渐成为构建碳-碳键的常见策略。在这一领域中,美国斯克利普斯研究所(The Scripps Research Institute)的余金权教授课题组一直专注于通过借助于天然官能团(如游离羧酸、游离脂肪胺和天然酰胺)导向的配体控制的碳氢键活化反应来构建新的碳-碳键。在过去十多年的研究中,该课题组开发了一系列的高效配体来加速C-H 键的活化。例如:他们先后实现了配体促进的Pd(II)-催化的游离羧酸导向的 β-甲基碳氢键活化(芳基化、烯基化、氧乙酰基化等)及Pd(II)-催化的游离羧酸导向的 β-亚甲基碳氢键活化(α, β-脱氢反应和二羧酸的位点选择性β-和γ-亚甲基内酯化反应)。尽管如此,仍有很多问题亟需解决。例如:在前者(β-甲基)通过C-H键活化在分子中引入含氮杂环;在后者(β-亚甲基)通过C-H键活化实现分子间官能团化。在最新刊登的这两篇文章中,该课题组报道了他们在解决上述问题上的最新研究成果。两篇文章由Liang Hu博士和Guangrong Meng博士共同完成。
(一):配体促进的Pd(II)-催化的游离羧酸导向的 β-甲基碳氢键杂芳基化
Pd(II)-催化的游离脂肪酸导向的 β-甲基碳氢键活化此前已有诸多报道。通过配体的设计及反应条件的优化,一系列碳-碳键与碳-杂原子键都可以被顺利构建。然而,对于在此位置引入药物结构中广泛存在的含氮杂环,化学家们仍然没有找到很好的策略。现有的解决方法仍然依赖于预先安装外加导向基,但这限制了目标分子合成的效率。余金权课题组长期深耕于Pd(II)-催化的游离脂肪酸导向的碳氢键活化,为了解决这一问题,他们首先分析了向此位置直接引入含氮杂环的困难(图1):相对于具有弱配位能力的羧酸导向基,含氮杂环(如吡啶)具有较强的与过渡金属中心配位的能力,可能会在反应体系中与Pd(II)配位导致催化剂失活。对此,他们提出,解决这一问题最有效的方法依然是通过配体设计来促进反应体系中有活性Pd络合物的生成。
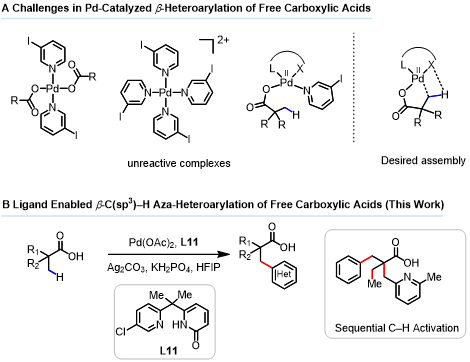
图1:β-甲基碳氢键杂芳基化研究背景(图片来源:Angew. Chem. Int. Ed.)
在初始的条件优化中,作者重点研究了配体对反应的影响(图2)。在没有配体或使用有代表性的单齿吡啶类配体(L2)、单齿吡啶酮类配体(L3)的情况下没有获得所需的产物。随后作者将注意力转向之前帮助他们实现亚甲基碳氢键活化的基于吡啶酮的双齿配体。在对该类配体进行一系列优化之后,他们发现当使用六元双齿螯合配体(L11)时,该反应可以得到71%的β-亚甲基杂芳基化产物。而当作者使用五元双齿配体 (L4-L5)时,反应产率则只有5%。作者基于六元双齿螯合配体(L11)探索了这一反应的底物适用范围。作者探索了近50个底物,都取得了良好的收率,产率33%-86%。醚类,芳基卤素等官能团都能良好的兼容。

图2:反应配体研究(图片来源:Angew. Chem. Int. Ed.)
(二):配体促进的Pd(II)-催化的游离羧酸导向的 β-亚甲基碳氢键芳基化
上面提到,余金权课题组通过使用六元双齿螯合配体(吡啶-吡啶酮类)成果实现了游离羧酸导向的β-甲基杂芳基化。而在同时,他们也实现了游离羧酸导向的β-位非环状底物的亚甲基碳氢键芳基化。此前,为了实现这一位置的亚甲基碳氢键官能团化,化学家们通常需要预先安装强配位属性的双齿导向基来加速碳氢键活化进程(图3A)。在稍早之前,该课题组成功实现了Pd(II)-催化的游离羧酸导向的 β-亚甲基碳氢键活化(α, β-脱氢反应和二羧酸的位点选择性β-和γ-亚甲基内酯化反应)。但是这些进展仍然局限于亚甲基 C-H 键的分子内官能团化。通过实现 β-亚甲基 C-H 键分子间官能团化可以迅速扩大分子的多样性。该课题组最新研究成果显示,通过配体设计与优化,无需安装导向基,游离羧酸导向的β-亚甲基芳基化依然可以高效进行。
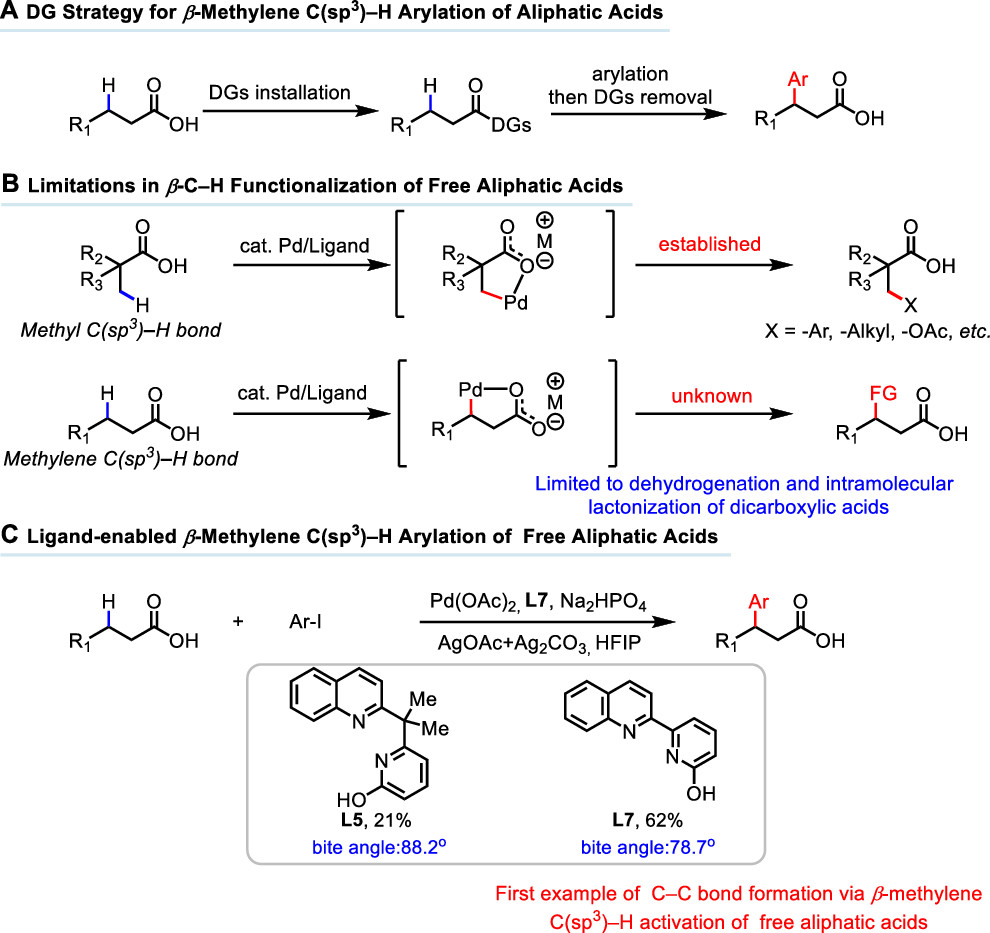
图3: β-亚甲基芳基化研究背景(图片来源: J. Am. Chem. Soc.)
在条件优化中,作者依然是首先考察了配体对反应的影响(图 4)。在没有配体的情况下没有获得所需的产物。类似地,使用此前报道过的单齿吡啶类配体(L2)、单齿吡啶酮类配体(L3)和双齿MPAA配体(L4)也未能得到任何产物。而当使用他们最近发展出的六元双齿螯合配体L5时,作者成功观察到了21%的β-亚甲基芳基化产物。接下来作者筛选了一系列其它基于吡啶酮的六元双齿配体,但是反应产率都很低。当作者将注意力转为使用五元双齿螯合配体 (L7)时,反应产率被顺利提高到了62%。随后作者使用最优配体(L7)对反应底物进行了探索。近50个底物都取得了良好的产率,产率37%-72%。酮类,酯类,烷基胺等官能团都能良好的兼容。
值得一提的是,在β-亚甲基芳基化的配体优化中,作者发现五元双齿螯合配体(L7)相对于六元双齿螯合配体(L5)有着更高的催化效率;而在上文提到的β-甲基杂芳基化的反应中,作者却观察到了相反的实验结果。这些实验数据进一步证明了该课题组在此前文章中报道的配体螯合角对反应活性有着重要的影响,应当成为此后配体设计中不可或缺的考量因素(Science 2021, 374,1281-1285.)。
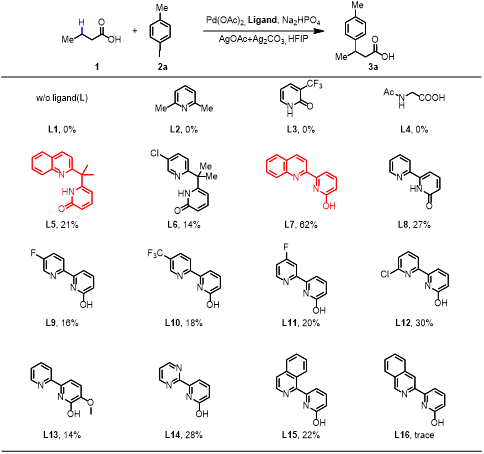
图4:反应配体研究(图片来源: J. Am. Chem. Soc.)
总结 余金权课题组近日在著名化学期刊JACS和Angew上连续报道了他们在Pd(II)-催化的游离脂肪酸导向的 β-亚甲基芳基化和β-甲基杂芳基化领域中的研究成果。这些研究成功的关键在于使用他们之前开发的五元环和六元环的双齿吡啶-吡啶酮配体。这些研究成果进一步促进了碳氢键活化在药物研发中的应用。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn