

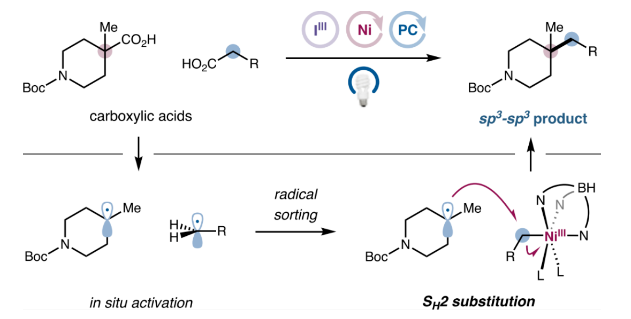
图1. 光/镍催化双分子均裂取代(SH2)交叉脱羧偶(图片来源:J. Am. Chem. Soc.)
过渡金属催化的交叉偶联反应使得人们可以通过简单分子砌块的组装实现复杂化合物的构建。传统的交叉偶联反应主要涉及经典有机亲电试剂和有机金属亲核试剂之间的偶联,近年来光氧化还原催化的出现,使得偶联策略可以扩展至更多含普通天然官能团的底物片段,如氯代物、醇、羧酸、以及C-H键等。在这些偶联砌块中,羧酸由于商业易得、结构多样以及稳定无毒等优点得到了广泛关注。目前已有众多涉及脂肪族羧酸脱羧的光氧化还原反应被报道,包括烷基化、芳基化、胺化和三氟甲基化等。然而对于两种不同羧酸之间的高选择性交叉脱羧C(sp3)-C(sp3)偶联依然难以实现。
传统的过渡金属催化C(sp3)-C(sp3)偶联主要通过形成二烷基金属络合物来实现,然而这种双烷基金属中间体还原消除的速率通常较慢且易发生β-H消除、碳-金属键断裂以及富电子烷基被氧化为碳正离子等副反应。自由基交叉偶联作为传统金属催化偶联反应的理想替代方法,近年来逐渐被人们关注。然而由于自由基之间的反应一般是由扩散控制的,当两种自由基具有相似的寿命且能以相近速率生成时,会得到自偶联和交叉偶联的混合物(图2A)。基于上述问题,作者提出了一种双分子均裂取代(SH2)策略,通过金属与自由基选择性结合生成金属烷基物种再与另一自由基反应实现交叉偶联,其中金属与自由基的选择性结合可以由烷基自由基本身的取代度和反应活性来控制(图2B)。根据此设计原理,作者成功开发了一种铁卟啉催化烷基溴代物与氧化还原活性酯之间的交叉偶联反应,在此基础上,作者期望开发一种两种羧酸底物间的选择性交叉偶联(图2C)。
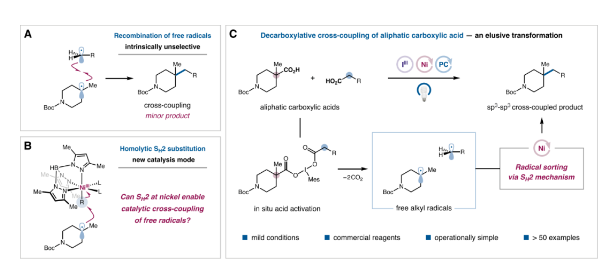
图2. 研究背景与反应设计思路(图片来源:J. Am. Chem. Soc.)
首先,作者提出了该双脱羧交叉偶联反应的设计思路与相应的机理(图3B)。羧酸1首先与高价碘2上的羧酸配体发生交换,生成相应的三价碘物种3。随后激发态光敏剂(4CzIPN或TXO)与高价碘物种发生能量转移,断裂两个I-O键后发生脱羧得到烷基自由基4和5,在此阶段,Ni(II)配合物6可能会选择性地捕获较少取代的烷基4,生成Ni(III)烷基配合物7。最后与自由基5发生SH2反应得到交叉偶联产物8并完成催化循环。
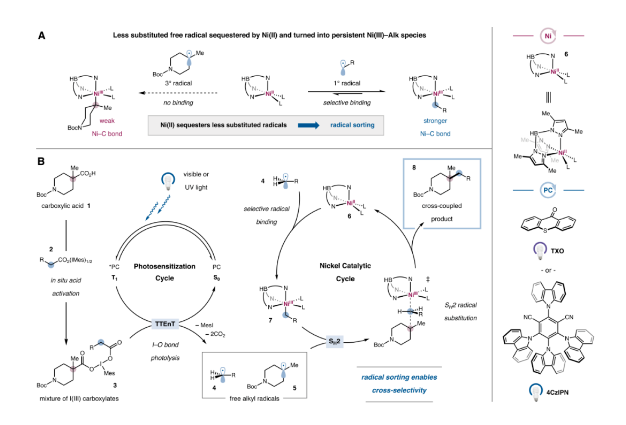
图3. 双脱羧交叉偶联反应体系设计(图片来源:J. Am. Chem. Soc.)
随后作者以N-对甲苯磺酰基哌啶酸和2,4,6-三甲基碘苯二乙酸MesI(OAc)2为模板底物对反应条件进行了详细筛选(图4)。使用Ni(acac)2为金属源,三(3,5-二甲基-1-吡唑基)硼氢化钾(K[Tp*])为配体的组合能有效催化该反应。对于光催化条件,作者探索出了两种催化方案,即365 nm紫外光与TXO组合以及450 nm蓝光与4CzIPN组合,相对于前者,可见光条件对于一些在紫外光下稳定性差的底物更加适用。最后,通过优化溶剂、温度以及反应时间等条件,最终能以85%收率获得目标脱羧偶联产物。
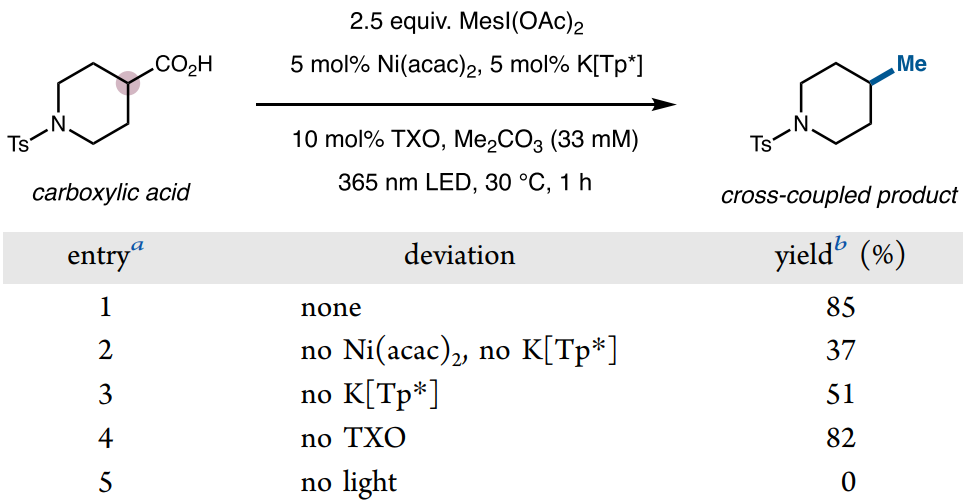
图4. 反应条件优化(图片来源:J. Am. Chem. Soc.)
在最优反应条件下,作者考察了该脱羧甲基化反应的底物适用范围。如图5所示,该反应表现出优异的官能团兼容性。含杂环的伯烷基羧酸,如吡啶、苯并三唑和1,2,4-噁二唑,能以良好的产率得到甲基化产物9和10。众多仲烷基羧酸均能顺利完成该反应(11-20),其中β-内酰胺以及受保护和未保护的醇羟基具有良好的耐受性(11, 12, 18),证明其在药物化学中具有一定的应用潜力。对于环状羧酸,包括氮杂螺[3.3]庚烷(14),、环戊烷(15)、吡咯烷(16)、哌啶(17-19)以及去甲托烷(20)均表现出优异的反应性。对于具有挑战性的叔烷基羧酸,该催化体系表现出了强大的适用性,成功实现了一系列含季碳中心产物的构建(21-29)。随后,作者又考察了生物活性分子中广泛存在的α-氨基酸和α-氧酸结构单元的反应性,将这类底物置于标准反应条件下,能以良好的收率得到脱羧甲基化产物30-33,这表明富电子的亲核型自由基也能与该体系兼容。最后,作者考察了复杂药物和天然产物的适用性,含过氧键和缩酮骨架的青蒿琥酯和含两个未保护烯丙醇基团的赤霉素A3能以中等至良好的收率得到甲基化产物(34, 38)。含α-二苯基片段的药物分子安立生坦能顺利完成脱羧甲基化,表明该反应能适用于高度空间拥挤的底物环境(36)。

图5. 脱羧甲基化反应底物拓展(图片来源:J. Am. Chem. Soc.)
在完成以碘苯二乙酸作为甲基源的脱羧甲基化反应后,作者考察了其它双羧酸碘苯的反应性,这些三价碘底物可以由MesIO与相应羧酸反应获得(图6)。结果表明,同位素标记的CD3、13C-甲基均能适用于该脱羧偶联反应(40, 41)。多取代乙酸(42-44)和丙酸(45-46)能以中等至良好的收率完成相应烷基化反应。最后作者利用此反应也成功实现了一些季碳中心产物的构建(47-49)。
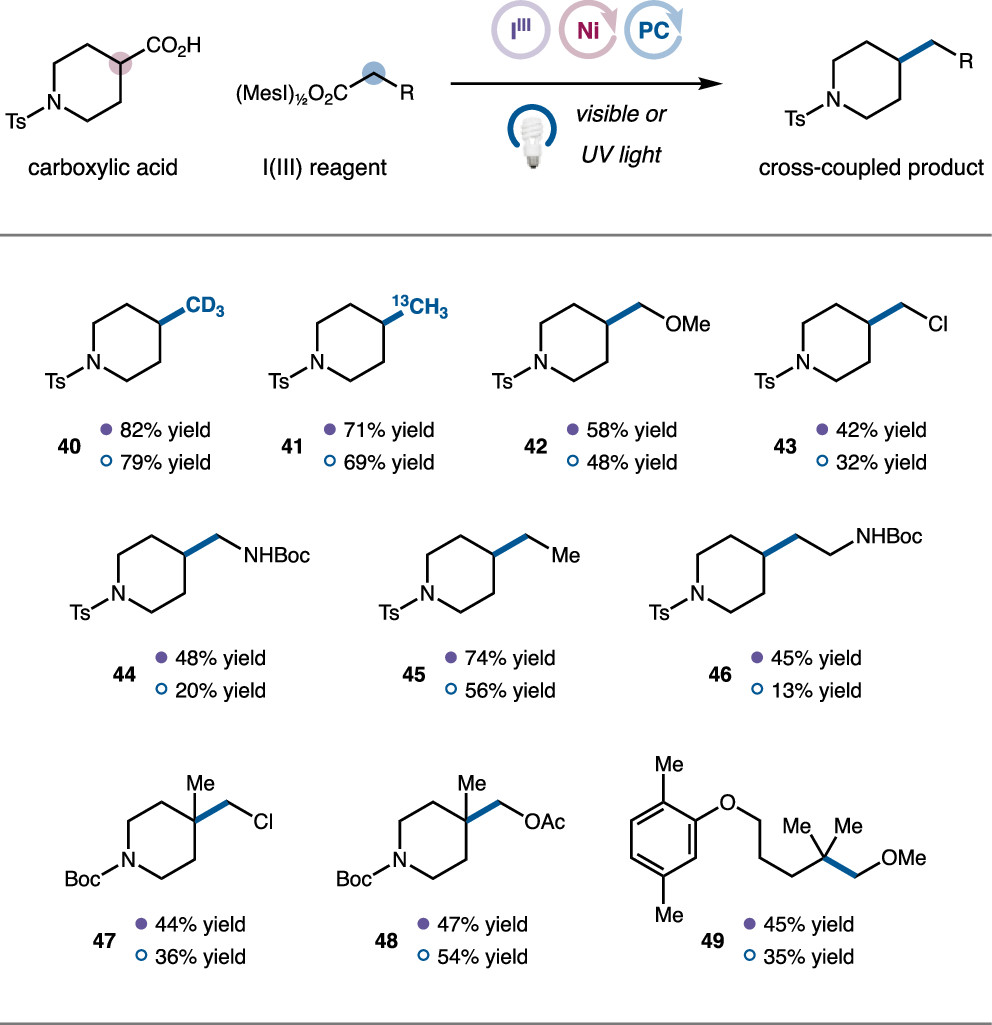
图6. 羧酸底物拓展(图片来源:J. Am. Chem. Soc.)
随后,作者研究了该体系中镍催化循环的机理。首先通过动力学分析表明在紫外光条件下,高价碘物种的光敏化为该反应的决速步,且反应速率与镍催化剂的浓度无关。对于该转化的立体化学过程,作者将底物β-氨基酸50置于各种甲基化反应条件下,研究其反式与顺式产物15的比例规律(图7A)。结果表明在不添加镍催化剂时能以34%的产率和1.5:1的d.r.值得到交叉偶联产物,这可能是通过受扩散控制的经典自由基偶联生成。通过添加Ni(acac)2和配体K[Tp]能将产率和d.r.值分别提高至63%和2.4:1。使用最优配体K[Tp*]最终能以81%的产率和3.0:1的d.r.值得到产物。这些结果都表明Ni物种直接参与了该C-C键的形成过程。一般而言,镍参与的金属有机反应通常涉及低价Ni(0)或Ni(I)物种,然而循环伏安实验表明在该体系下,过量的MesI(OAc)2能有效地将Ni(I)物种氧化为Ni(II)。为了进一步证实该催化转化中不涉及活性低价镍物种,作者还通过添加易与低价镍氧化加成的芳基卤代物进行控制实验,结果表明卤代物的添加没有抑制该双脱羧偶联反应且芳基卤代物可以定量回收(图7B)。作者进一步利用EPR实验表征该体系中Ni物种的存在形式(图7C)。对于MesI(OAc)2、Tp*Ni(OAc)络合物55和TXO的混合溶液,在无光照条件下未监测到EPR信号,表明在热化学条件下高价碘无法氧化Ni(II)络合物。当使用365 nm的紫外光照射时,出现了g值为2.17的EPR信号,其来源于以过渡金属原子为中心的自旋体系。对照实验表明在无TXO的条件下也能检测到一定强度的该信号,且关闭光源后该信号会在几秒钟内消失。这些结果表明MesI(OAc)2会在365 nm光照下生成甲基自由基,其被Tp*Ni(OAc)捕获得到低自旋d7Ni(III)-Me络合物56a。最后,作者对一系列碘苯二羧酸进行了相同的光激发EPR实验(图7D)。除MesI(OAc)2外,只有MesI(O2CEt)2能产生显著的EPR信号(g=2.19),异丙基和叔丁基无法得到相应Ni-烷基物种,这与DFT计算出的Ni-C键解离能顺序相一致。
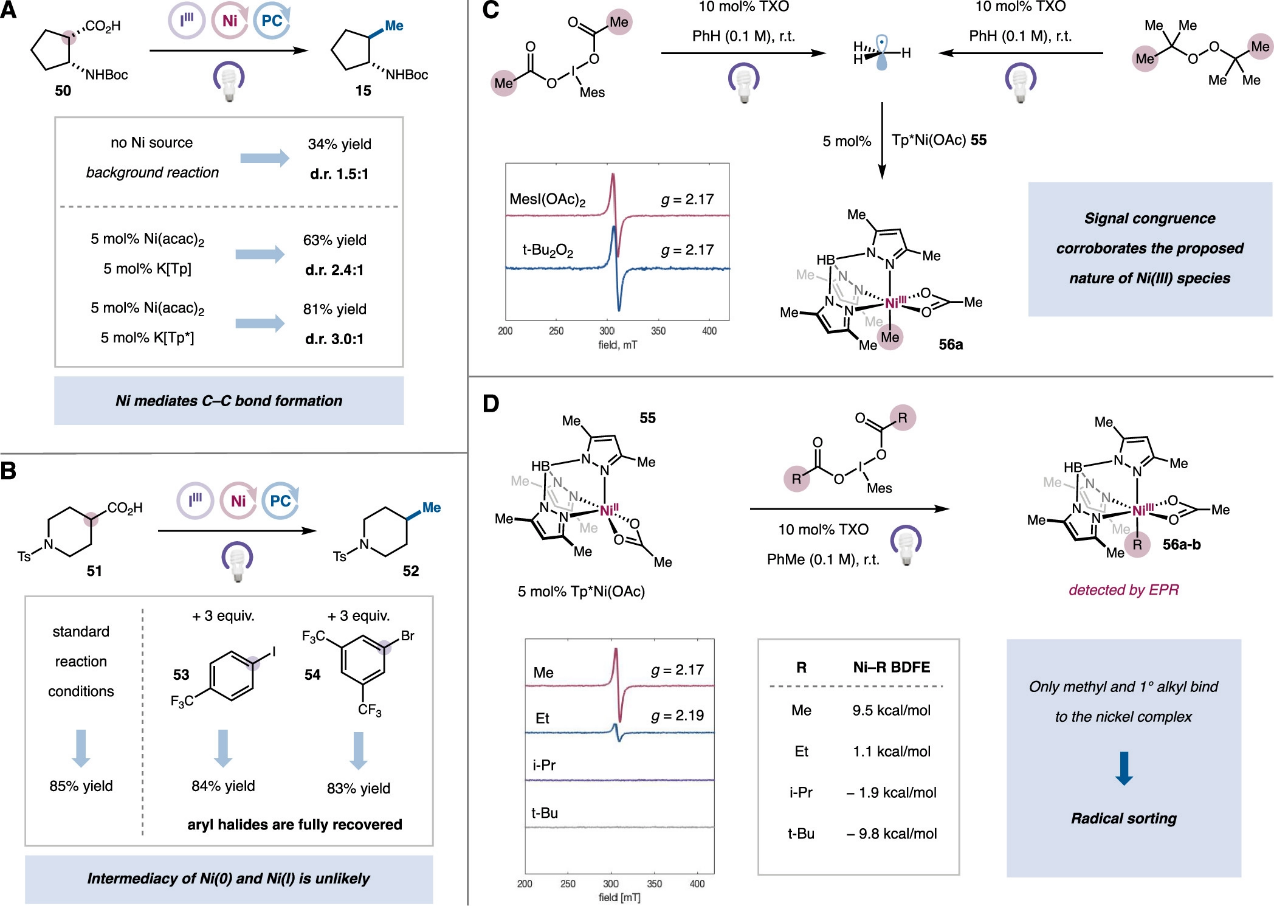
图7. 反应机理研究(图片来源:J. Am. Chem. Soc.)
总结 David W. C. MacMillan课题组报道了一种基于双分子均裂取代(SH2)策略的脂肪族羧酸双脱羧交叉偶联反应。在该反应中,高价碘光敏化产生的烷基自由基首先被Ni(II)物种捕获,进一步与另一自由基发生SH2反应,实现该脱羧偶联的选择性。该催化体系具有优异的官能团兼容性且能用于传统金属有机反应难以得到的季碳中心化合物的构建。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn