

不饱和键的较高的反应性与原子经济性(一次反应可以构造两个新的σ键)使得π体系的区域选择性双官能团化反应受到关注。小分子催化剂的介入大大丰富这一领域,减轻了传统反应性的限制,显著提升效率。在简单烯烃亲核/亲电反应物的位点选择性上的持续创新证明了这一策略的成功,并激发了科学家们对双烯等更大π体系的兴趣。
由于在功能性小分子中氟无处不在,而且此前I(I)/I(III)催化的[1,n]-二氟化反应仅限于n=3,因此作者希望实现双烯的直接1,4-二氟化反应。这一根本性的进展不仅将扩大现有的氟化反应范围,还将促进现代药物化学的发展。为了使反应效果更佳,-CF3取代1,3-双烯被认为是有前途的底物。反应得到的1,4-二氟化产物的一个吸引人的特征是稳定的叔氟,其中C(sp3)-CF3取代基对其稳定做出了突出贡献。结合之前的经验,该反应将采取分步机理进行。在由I(I)/I(III)催化的二氟化条件下,原位生成的ArIF2将活化双烯(I)中空间位阻较小的末端烯烃。烯丙基/苄基对碳正离子的稳定作用将抵消-CF3基团的Iπ效应。热力学上有利的E-双键的形成和亲核试剂对碘离子中间体的取代将同时发生得到产物(IV)。从机理角度考虑,其它亲核试剂同样可以完成最后一步取代反应,因此该反应还可以得到δ-氟醇和对应的胺衍生物。
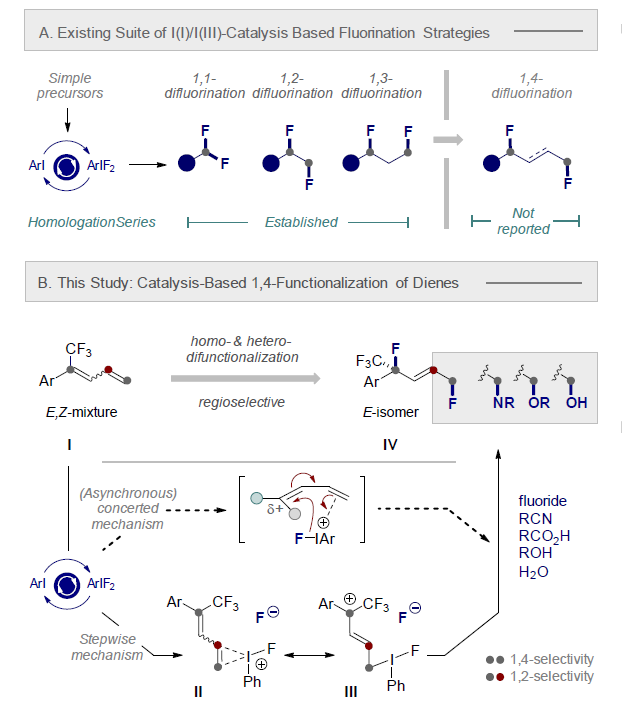
图1. 研究背景及反应机理(图片来源:Angew. Chem. Int. Ed.)
随后,作者以双烯1a为模型底物进行条件筛选。首先,作者以CHCl3为溶剂,在胺•HF络合物和Selectfluor®的存在下筛选了芳基碘化物催化剂,并发现5 (p-H)作为催化剂时效果最佳。最终,作者确定添加5 (20 mol%)和胺:HF的比例为1:7.5时效果最佳,可以92%的收率得到2a,且1,4-产物与1,2-产物的比例>20:1。作者还发现增加或减少胺与HF的比例对反应结果影响不大,Selectfluor®替代Oxone®或m-CPBA导致收率降低。
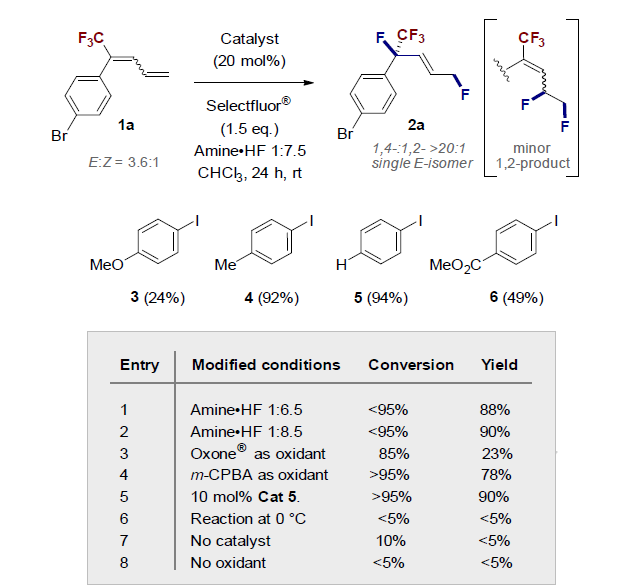
图2. 条件筛选(图片来源:Angew. Chem. Int. Ed.)
为了研究二烯构型对结果的影响,并确定烯烃部分的立体收敛性,作者将E-1a和Z-1a分别在催化条件下反应。作者发现在所有情况下,E-烯烃2a的收率在89-94%之间(为了操作简单,作者使用E/Z混合物进行底物范围研究)。用-H和-Me代替-CF3的对照实验并不成功,可以体现-CF3起到的活化作用。
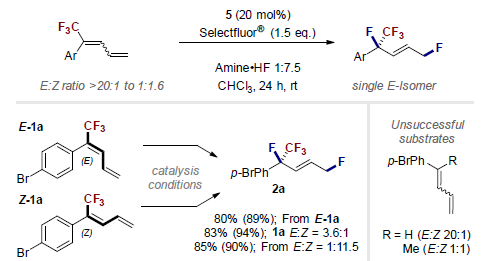
图3. Z、E-构型的探索(图片来源:Angew. Chem. Int. Ed.)
在确定最佳反应条件后,作者进行了底物拓展。反应可以兼容多种卤代芳基(2b-2f),产率范围为70-90%。含吸电子基团p-CF3的2h产率为76%,而含给电子基团p-Me的2i的产率为41%。未取代芳环的2j收率为74%。硝基、酯基、氰基等官能团(2k-2r)同样适用于该反应,收率高达52-91%,且得到的均为单一的E-构型产物。另外,该反应同样适用于非芳香族二烯:环己基衍生物对应的产物2s收率为54%。最后,作者利用苯酞酰亚胺衍生物2t(收率为90%)得到了单晶结构,不仅展示了相关基团的位置关系,还证实了产物单一的E-构型结构。
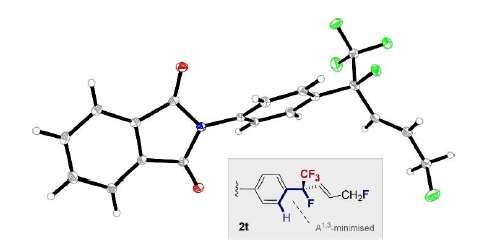
图4. 2t的X-射线晶体结构图(图片来源:Angew. Chem. Int. Ed.)
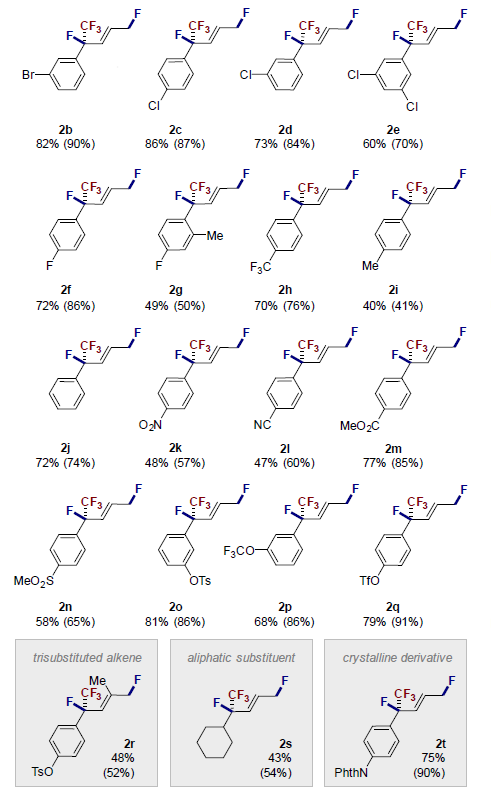
图5. 底物拓展一(图片来源:Angew. Chem. Int. Ed.)
为了合理解释反应的区域选择性,并证明反应过程中阳离子中间体的存在,作者对上图中所选底物的本位13C-NMR位移与log10(1,4-/1,2-区域选择性)作图,揭示了取代基的电子性质与实验观察到的区域选择性之间的关系:有更多富电子芳基取代基使苄基阳离子稳定的底物显示出更好的1,4-区域选择性。这支持了图1所描述的机理。
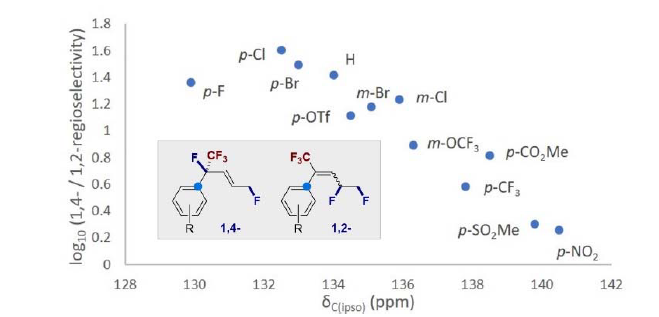
图6. 区域选择性的影响因素(图片来源:Angew. Chem. Int. Ed.)
为了进一步扩展该方法适用范围,作者引入了其它亲核试剂以直接获得高度修饰的1,4-双官能团化产物。受到Ritter反应与高价碘催化相容性的启发,作者选择腈作为反应的另一部分。乙腈对应的1,4-氨基氟化产物3a(65%)的形成。证明了这一想法的成功。3b (Et)、3c (i-Pr)、3d (t-Bu)、3e(-Ph)和3f (-CD3)的收率高达71%。羧酸同样可以实现双烯的区域选择性1,4-氧氟化。3g-k最高以72%的收率得到产物。尽管产率一般,但醇甚至是水也可参与反应,这大大拓宽了反应的适用范围。
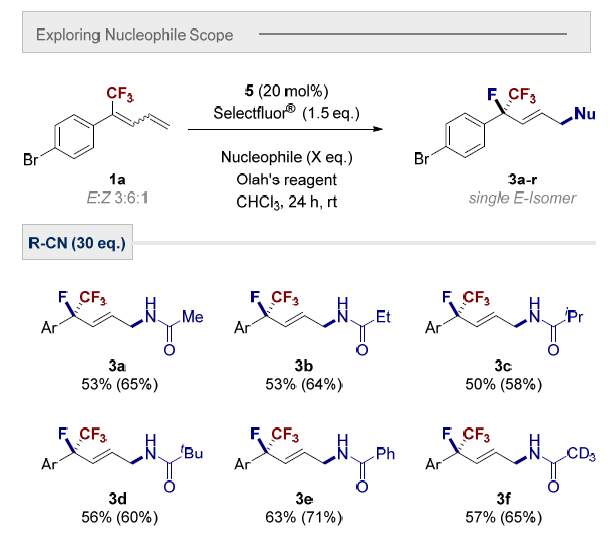
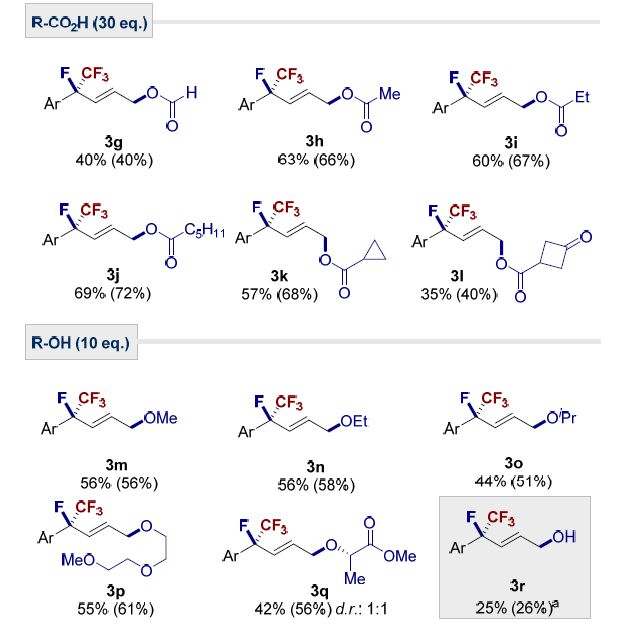
图7. 底物拓展二(图片来源:Angew. Chem. Int. Ed.)
在不损失催化效率(85%收率)的情况下,反应规模可被扩大到3 mmol。为了证明反应的应用价值,作者进行了进一步衍生化反应。在回流CH2Cl2的过程中用溴处理2a,可生成烯丙基溴4a(收率61%)。2a的烯烃部分经过臭氧化反应后还原可以58%的收率得到4b;也可在m-CPBA作用下得到4c。化合物3h经过皂化反应和Appel反应可得烯丙基溴化物4d (两步收率98%)。3r经过Pinnick氧化可生成α,β-不饱和羧酸(收率98%)。综上,该反应具有令人满意的应用价值和前景。
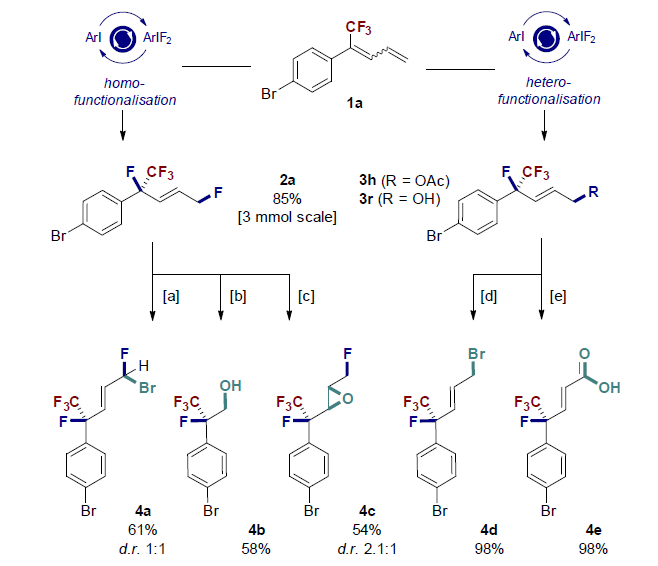
图8. 反应应用(图片来源:Angew. Chem. Int. Ed.)
总结 Ryan Gilmour课题组通过I(I)/I(III)催化首次实现了双烯的区域选择性1,4-二氟化反应。该策略经过进一步改进,可通过一步反应直接得到δ-氟醇和胺衍生物。该反应具有极高的区域选择性(1,4-:1,2->20:1),并可得到高度官能团化的三级C(sp3)-F。该方法不仅提供了一种新的氟化策略,还将在有机氟化学领域发挥重要作用。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn