

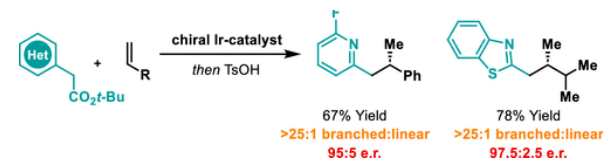
(图片来源:J. Am. Chem. Soc.)
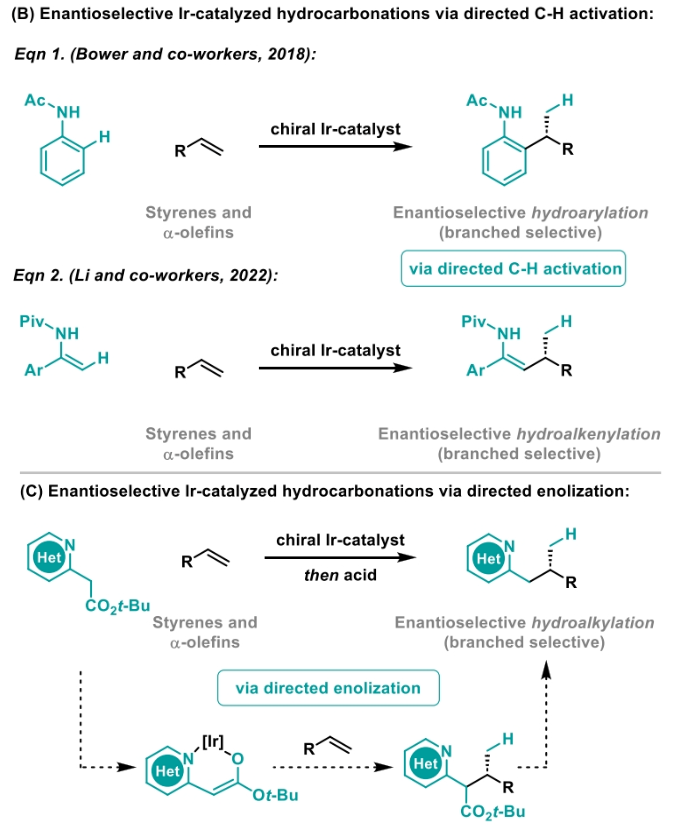
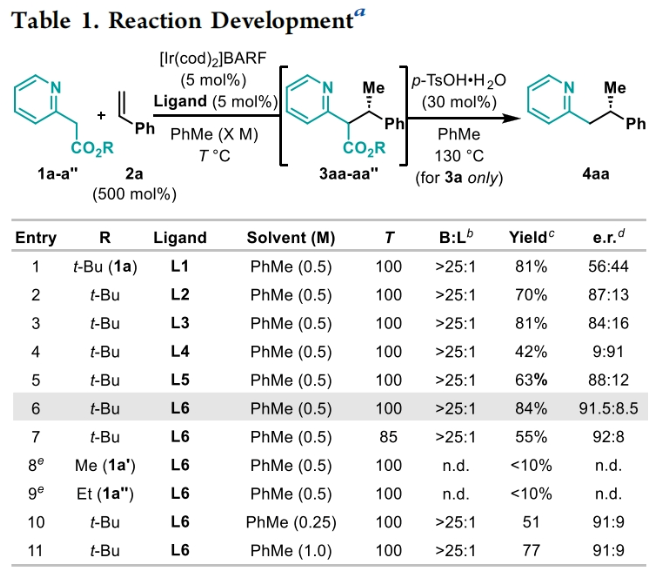
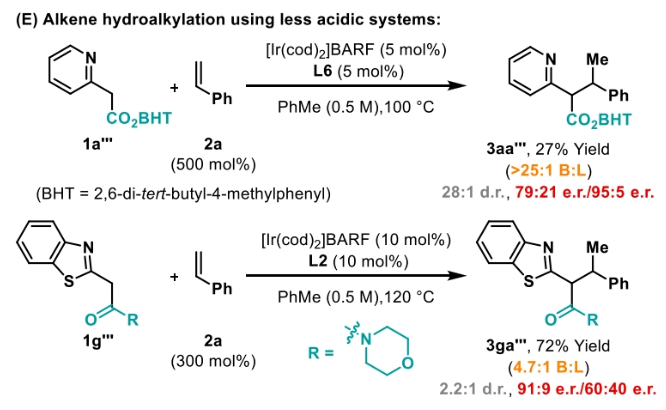
正文 包含对映选择性分子间C-H键与烯烃加成的交叉偶联是极具吸引力的,主要是由于:(a)可以减少起始原料的预官团化过程;(b)具有较高的步骤和原子经济性;(c)可以使用简单易得的起始原料作为偶联配偶体(Scheme 1A)。而实现这一过程的最有效途径就是导向金属插入到C-H键中,例如C-H活化。此方法通常需要使用极化的烯烃,主要是由于:(a)可以增强反应性;(b)通过电子效应来控制反应的区域选择性。事实上,目前仅有少数的对映选择性策略可以适用于最低活化的单取代烯烃(如苯乙烯和α-烯烃),其中基于铱催化剂转化被证明是特别有希望实现氢-芳基化和氢-烯基化反应过程(Scheme 1B)。最近,英国利物浦大学John F. Bower课题组发展了铱催化烯烃的对映选择性氢-烷基化反应。反应中使用手性双膦配体DuanPhos修饰的阳离子Ir(I)络合物,以完全的分枝选择性和良好的对映选择性实现了苯乙烯和α-烯烃的氢-烷基化(Scheme 1C)。下载化学加APP到你手机,更加方便,更多收获。 (图片来源:J. Am. Chem. Soc.) 首先,作者选用2-吡啶基乙酸叔丁酯1a和苯乙烯2a作为模板底物对此转化进行了探索(Table 1)。通过一系列条件筛选,作者发现当使用[Ir(cod)2]BARF (5 mol%), L6 (5 mol%), 在甲苯中 (0.5 mL)中100 °C反应,随后加入p-TsOH (30 mol%)在130 °C反应可以一锅法以84%的产率,良好的区域选择性(B:L > 25:1),91.5:8.5的er得到目标脱酸氢-烷基化产物4aa(entry 6)。 (图片来源:J. Am. Chem. Soc.) 在得到了最优反应条件后,作者首先对杂芳基骨架兼容性进行了考察(Table 2)。实验结果表明此转化对于一系列不同杂芳基,如取代吡啶(4aa-4fa)、苯并噻唑(4ga, 4pa-4sa),噻唑(4ha-4ia),苯并噁唑(4ja),苯并咪唑(4ka),吡嗪(4la)、三嗪(4ma)、异喹啉(4na)和喹啉(4oa)等均具有良好的兼容性,以39-97%的产率,良好的区域选择性(B:L > 25:1),75:25-99:1的er得到相应的脱羧氢-烷基化产物4aa-4sa。遗憾的是,嘧啶类起始原料1t和1u不能兼容此转化。 (图片来源:J. Am. Chem. Soc.) 接下来,作者对烯烃的兼容性进行了探索(Table 3)。实验结果表明不同取代的苯乙烯、萘乙烯、二茂铁取代的烯烃甚至是烷基烯烃均可兼容,以59-98%的产率,良好的区域选择性(B:L > 25:1),60.5:39.5-98:2的er得到相应的脱酸氢-烷基化产物4gb-4gp。值得注意的是,在4gn的合成过程中,作者并未观察到由烯丙基苯2n向β-甲基苯乙烯的潜在异构化竞争过程。 (图片来源:J. Am. Chem. Soc.) 有趣的是,反应中的脱羧步骤可用于触发进一步的C-C键形成(Scheme 2)。例如,连有乙酰基的烯烃2q可以与1g经历氢-烷基化反应得到3gq。而在加入p-TsOH (30 mol%)后120 °C反应可以以49%的产率,良好的区域选择性(B:L > 25:1),91:9的er得到手性环戊烯产物5(Scheme 2A)。此外,产物3ga还可以通过烯醇化官能团化,立体选择性的实现氟取代和甲基取代的产物6 (82%, 4:1 dr, 99:1 er)和7(68%, 9:1 dr, 99:1 er)(Scheme 2B)。 (图片来源:J. Am. Chem. Soc.) 最后,为了深入理解反应机理,作者进行了一系列控制实验(Scheme 3)。首先,当作者使用消旋的BINAP作配体时,分别尝试利用2a与2-,3-或4-号位取代的吡啶参与反应时,仅2-号位取代的吡啶能够实现转化,由此表明氮中心合适位置的重要性(Scheme 3A)。此外,氘交换实验表明在反应中固有的烯醇化和铱催化的烯醇化途径都可能存在。且C2位的氘交换发生在C-C键形成之前或之后。而甲基和次甲基位点的氘交换则发生在烯烃2c阶段,最有可能是通过可逆的氢金属化过程发生的(Scheme 3B)。动力学分析表明,催化剂([Ir(cod)2]BARF/L6)的级数近似为1。目前,作者倾向于认为碳金属化途径形成Int-II。这一反应可能经历由Ir-烯醇Int-I进行的内球烯烃碳金属化过程,也可能经历通过外球烯醇Int-III进攻Ir-π-络合物Int-IV。如果后者是有效的,那么其它可烯醇化的前亲核试剂将会以高水平的对映体选择性参与反应。然而,实际情况并非如此。例如,作者利用β-酮酯反应得到的基本上是外消旋氢-烷基化产物。因此,在Scheme 3C中展示的两种C-C键形成途径中,支链选择性可以归因于电子效应和/或铱中心倾向于加成到位阻较小的末端烯烃。在Table 1中,作者发现含有叔丁酯的底物最适合此转化。为了验证这一点,作者分别选择连有乙酯、叔丁酯以及叔戊酯的底物1g’, 1g, 和1g’’分别与苯乙烯2a反应。实验结果表明,1g在最温和的条件下(70 oC)反应,可以以最高的产率(98%)得到产物3ga。有趣的是,产物3ga-3ga’’的对映体富集程度接近,由此表明酯基的结构对反应性至关重要,但对对映选择性诱导过程影响很小(Scheme 3D)。而当作者使用相对弱酸性的前亲核试剂反应时,则会对对映诱导过程产生影响(Scheme 3E)。 (图片来源:J. Am. Chem. Soc.) 总结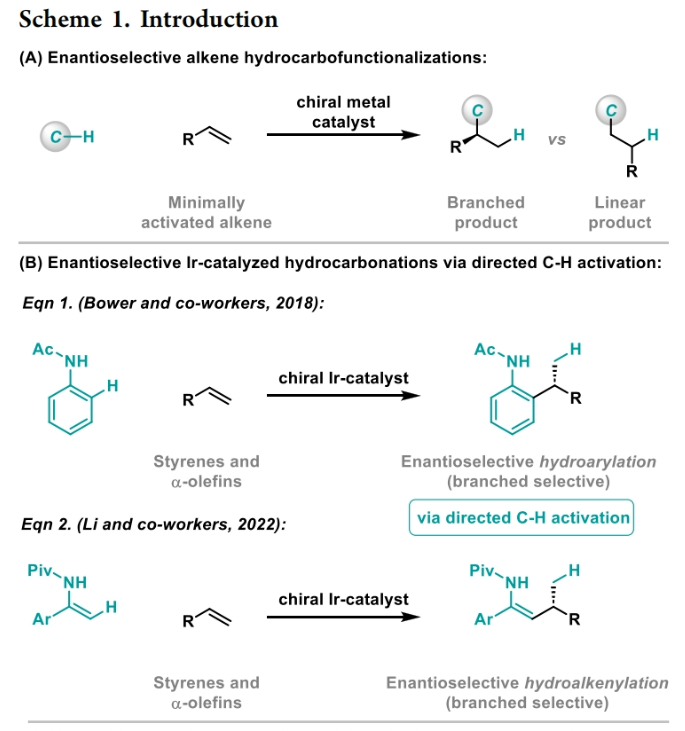
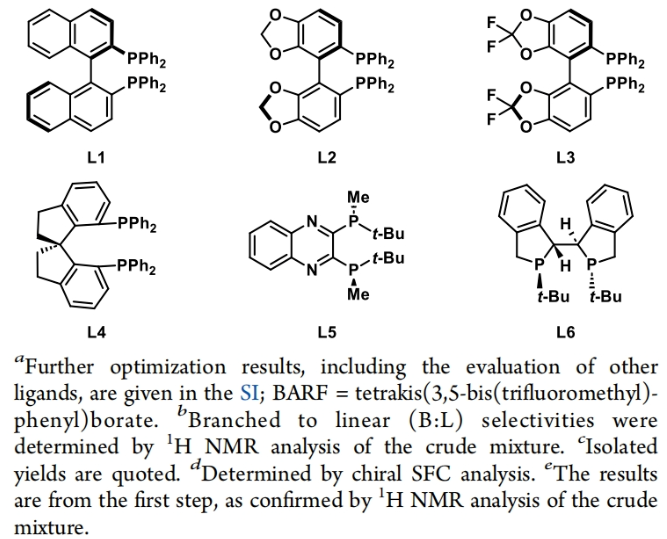
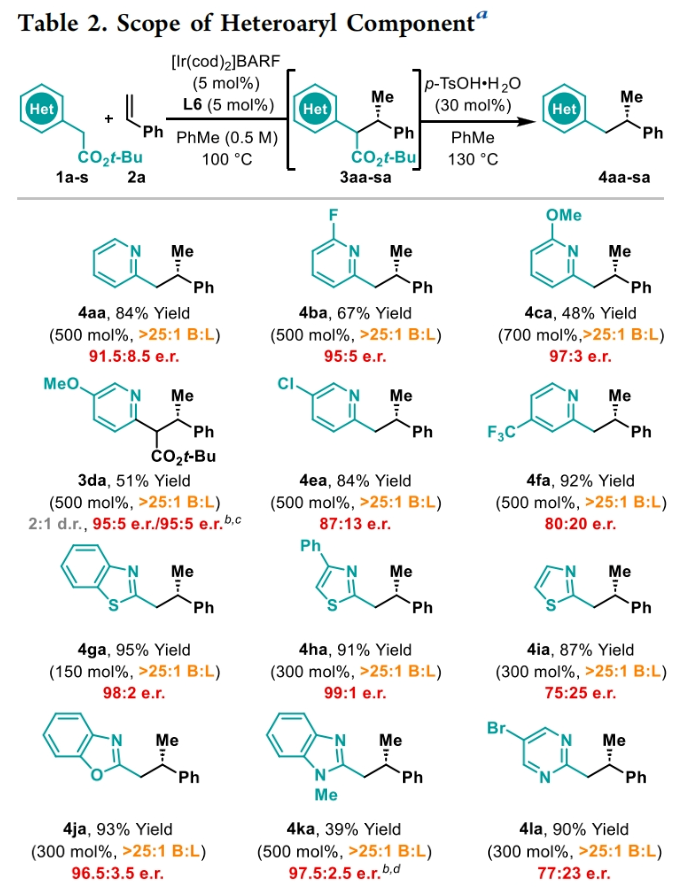
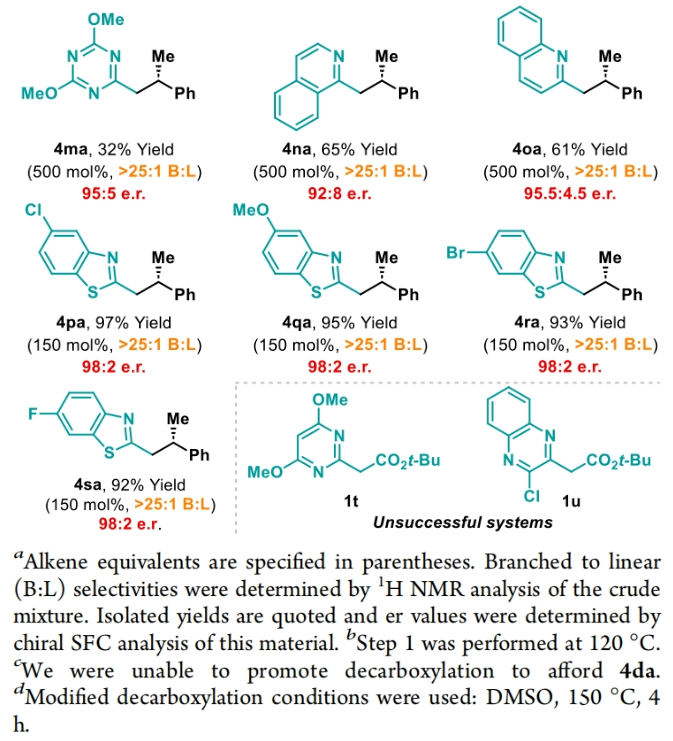
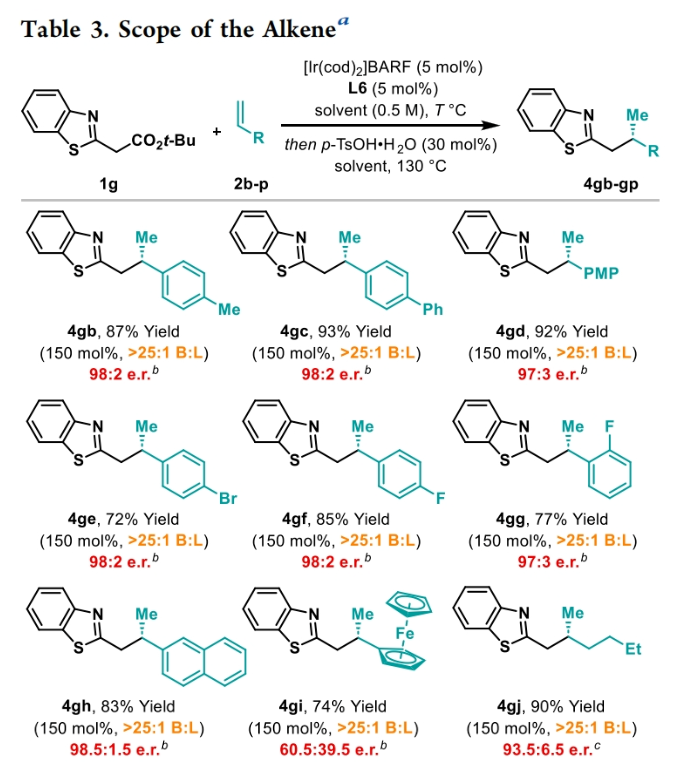
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn