

(图片来源:Angew. Chem. Int. Ed.)
正文
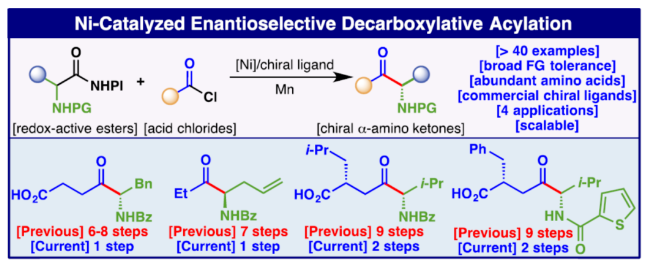
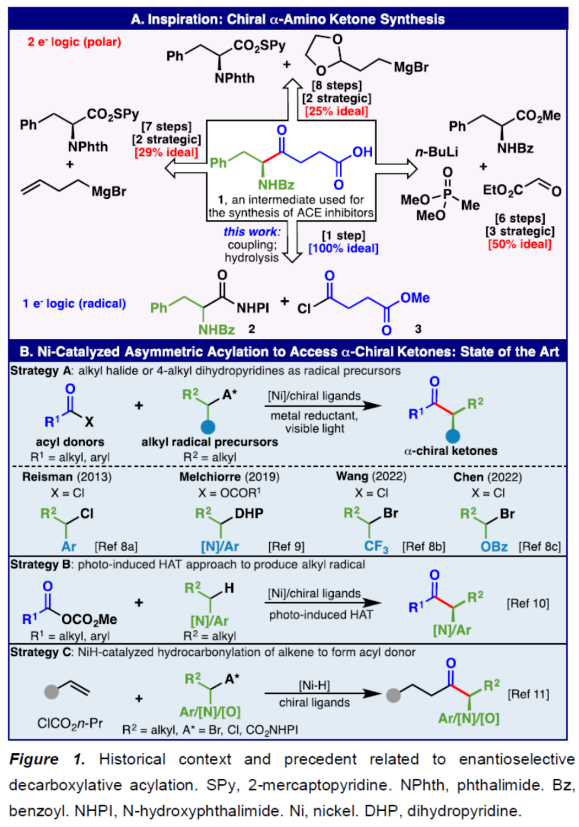
手性α-氨基酮是一种具有价值的砌块,并可作为合成大量天然产物和药物的关键中间体。到目前为止,最常见的逆向合成断裂策略涉及依赖于α-胺化策略或手性池衍生α-氨基酸的同系化反应。例如,砌块1(Figure 1A),一种用于合成ACE抑制剂的中间体,已通过后一种策略从L-苯丙氨酸通过6-8步构建,其中大多数反应步骤不会形成策略键,导致低理想性。原则上,利用自由基逆合成策略是合成1更为直接的方法,其中苯丙氨酸(2,外消旋或对映体纯)衍生的氧化还原活性酯(RAE)可与简单的琥珀酸衍生物3进行对映选择性脱羧酰化反应。目前,化学家们已开发三种通过镍催化构建α-手性酮的策略(Figure 1B)。在策略A中,在进入镍催化循环并与活化的酰基反应之前,烷基卤化物或二氢吡啶(DHP)单元用作还原(化学或光化学)活化的自由基前体。在策略 B中,光诱导不稳定C-H键(苄基或邻苯甲酰胺)的HAT形成相应的自由基供体。在策略C中,主要涉及氯甲酸酯、末端烯烃与合适的自由基供体的三组分偶联反应。近日,美国Scripps研究所Phil S. Baran课题组开发了一种高度对映选择性和普适性的镍催化脱羧酰化反应,该反应可简洁高效地以68%的收率与92%ee得到产物4。下载化学加APP到你手机,更加方便,更多收获。
(图片来源:Angew. Chem. Int. Ed.)
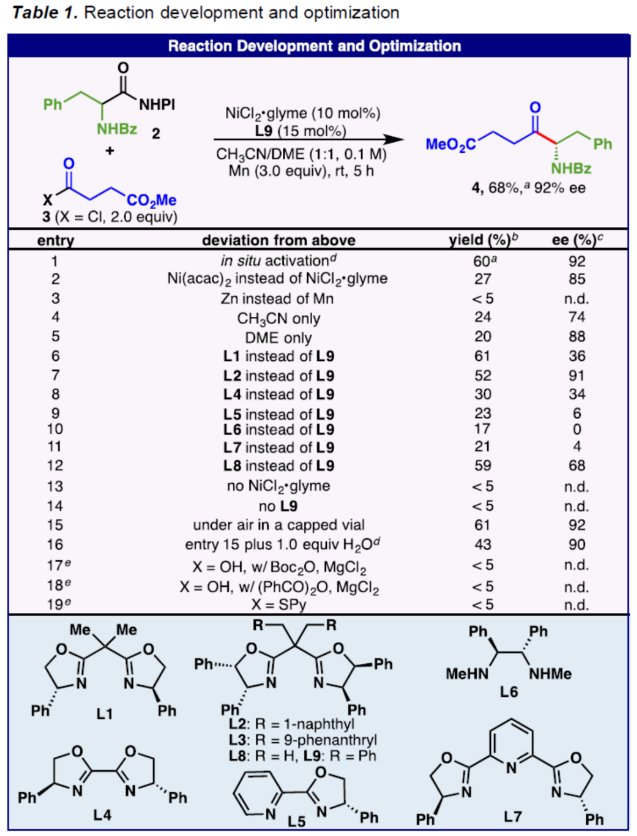
首先,作者以RAE 2与酰氯衍生物3作为模型底物,进行了相关还原脱羧酰化反应条件的筛选(Table 1)。当以NiCl2•glyme(10 mol %)作为催化剂,L9(15 mol %)作为配体,Mn粉(3.0 equiv)作为还原剂,在CH3CN/DME溶剂中室温反应5 h,可以68%的收率得到产物4,ee为92%。

(图片来源:Angew. Chem. Int. Ed.)
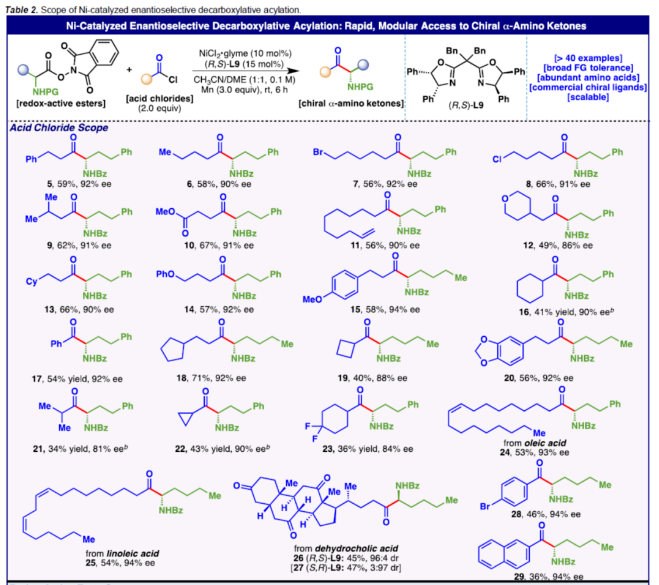
在获得上述最佳反应条件后,作者对底物范围进行了扩展(Table 2)。首先,一系列一级与二级羧酸衍生的酰氯或芳香族羧酸衍生的酰氯,均可顺利进行反应,获得相应的产物5-29,收率为34-71%,ee为81-94%。值得注意的是,一系列活性的基团,如卤素、烷氧羰基、烯基、羰基等,均与体系兼容。其次,一系列不同取代的氧化还原活性酯,也能够顺利进行反应,获得相应的产物30-45,收率为41-75%,ee为76-94%。然而,将保护基团从Bz切换到Boc或邻苯二甲酰亚胺时,导致对映选择性大幅下降(46,47)。同时,α-氯酰氯和三级酰氯,在上述标准的条件下,未能有效的进行反应(48-50)。
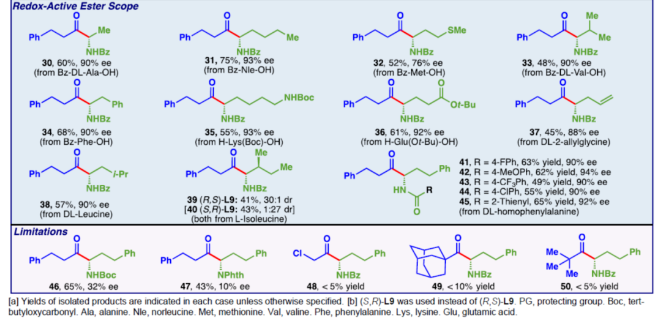
(图片来源:Angew. Chem. Int. Ed.)
紧接着,作者将上述的对映选择性脱羧酰化策略用于一些化合物的简便合成(Figure 2)。首先,化合物1(Figure 2A)的前期合成方法主要涉及6-8步反应,并且需要大量的保护基团、官能团相互转化、氧化还原操作和使用自燃试剂等。相反,化合物2与3通过上述的对映选择性脱羧酰化反应以及随后的水解后处理,即可一步合成化合物1,收率为62%,ee为91%。其次,烯丙基取代的对映体α-氨基酮60(Figure 2B)的合成前期主要通过经典的不对称相转移烷基化化学获得,并涉及七步反应。相比之下,化合物58与59通过上述的对映选择性脱羧酰化反应,可直接合成α-氨基酮60,收率为48%,ee为88%。此外,化合物63和69(Figure 2C)是用于发现针对SARS-CoV 3CL蛋白酶的苯胺抑制剂的药物化学程序中的中间体,通过九步途径获得,其中大多数操作不形成战略键。相反,利用上述的对映选择性脱羧酰化策略,仅需两步即可实现化合物63和69的合成。
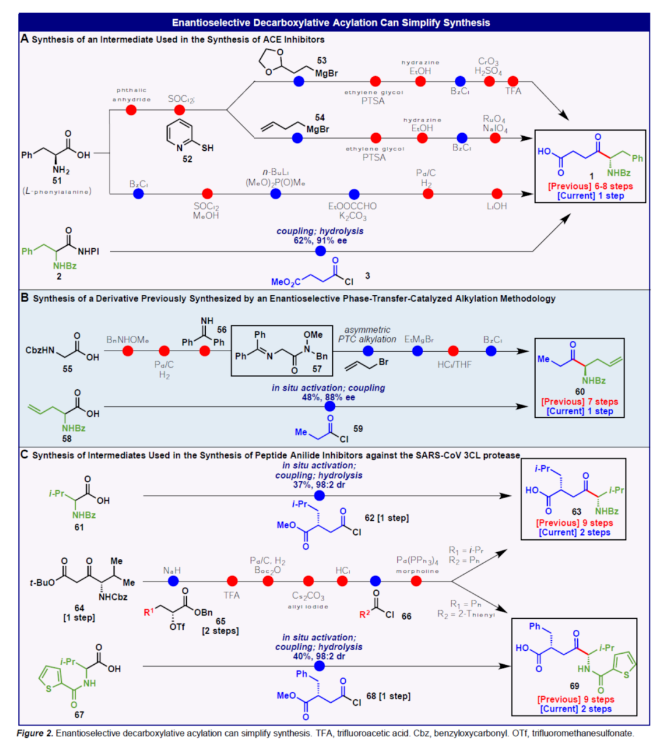
(图片来源:Angew. Chem. Int. Ed.)
此外,作者还对反应的实用性进行了研究(Figure 3)。首先,克级规模实验,同样能够以71%收率和93% ee得到产物31(Figure 3A)。其次,化合物6在LiAl(Ot-Bu)3H条件下进行还原反应,可以93%的收率得到anti-1,2-氨基醇72。72中的苯甲酰基可在Cp2ZrHCl/NH4Cl条件下进行脱除,并在Boc2O/MeCN条件下进行氨基的保护,可以两步62%的收率得到化合物73(Figure 3B)。值得注意的是,在上述的过程中,对映选择性基本不受影响。同时,对于氧化还原活性酯74和76,也能够与10顺利反应,获得相应的产物75(收率为26%,ee为40%)和77(收率为37%,ee为62%)(Figure 3C)。此外,在化合物3与78的标准反应体系中加入一当量的缺电子烯烃79,生成了外消旋加合物80,表明了反应形成了α-氨基自由基(Figure 3D)。
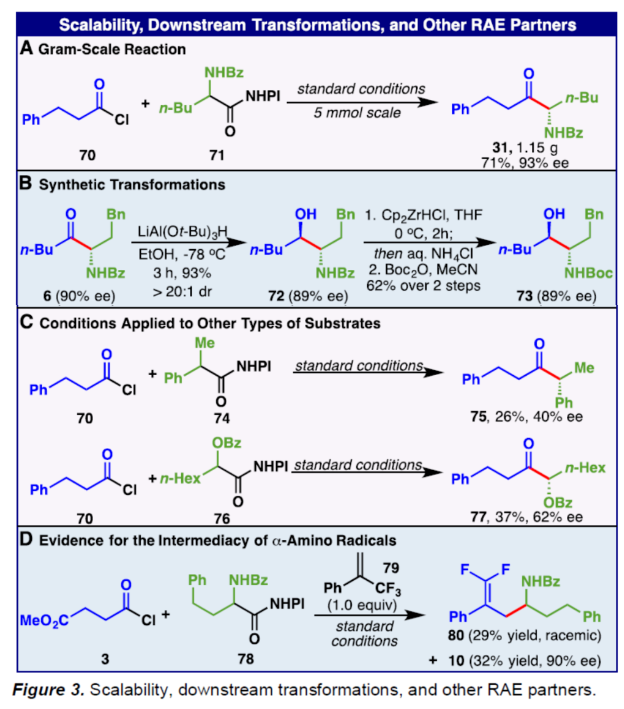
(图片来源:Angew. Chem. Int. Ed.)
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn