

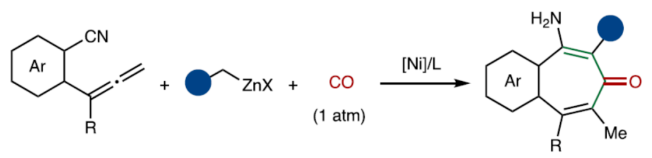
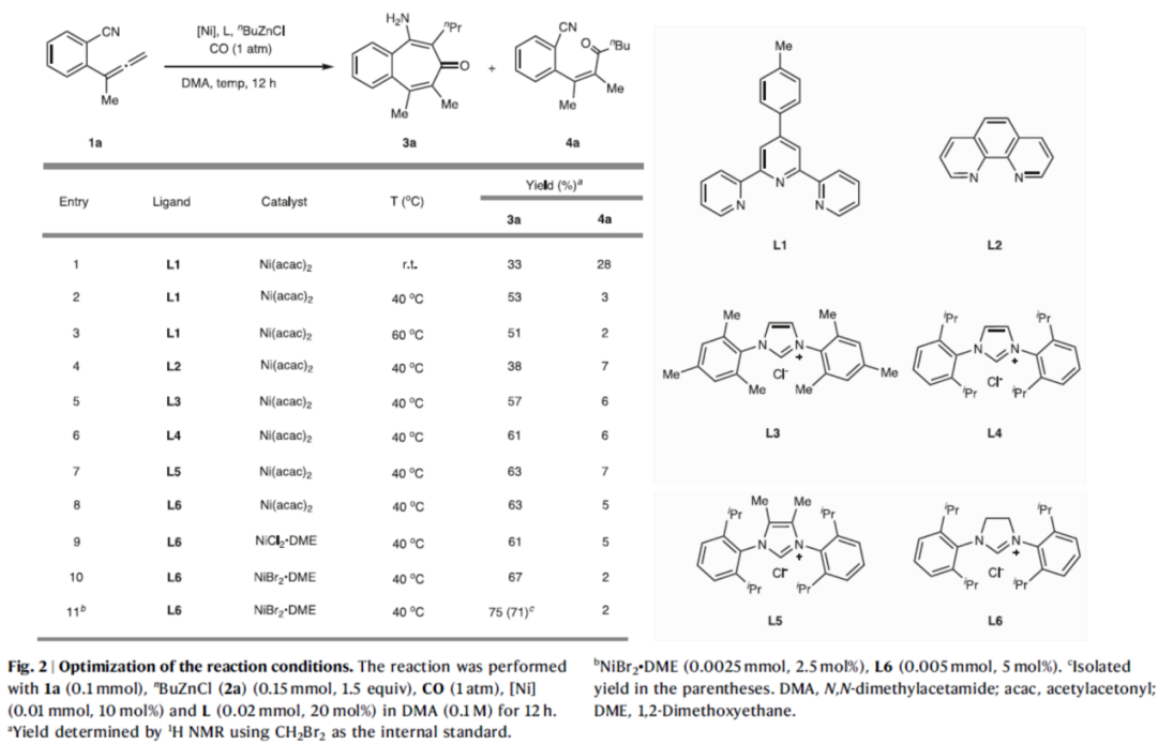
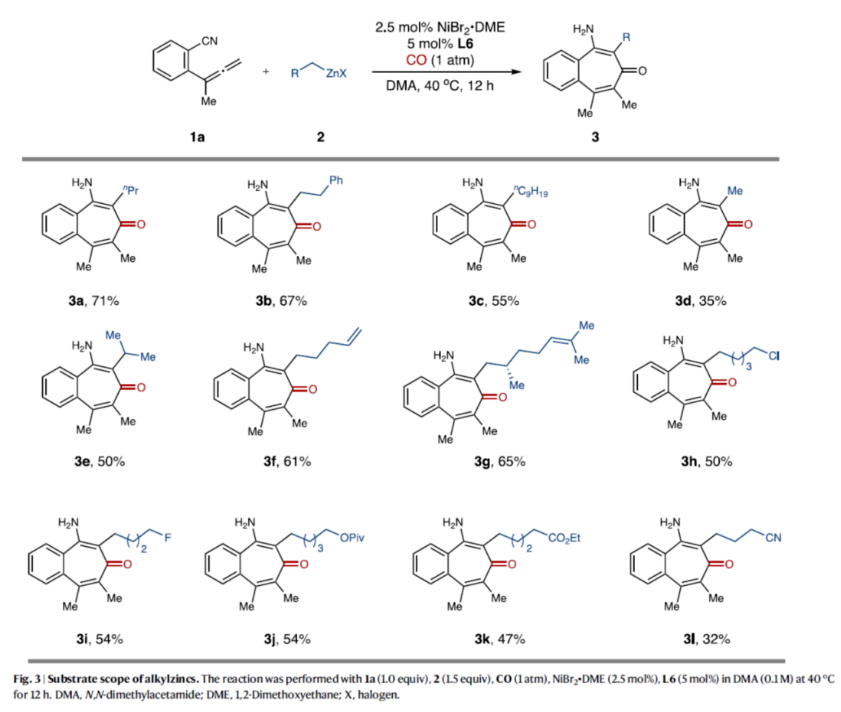
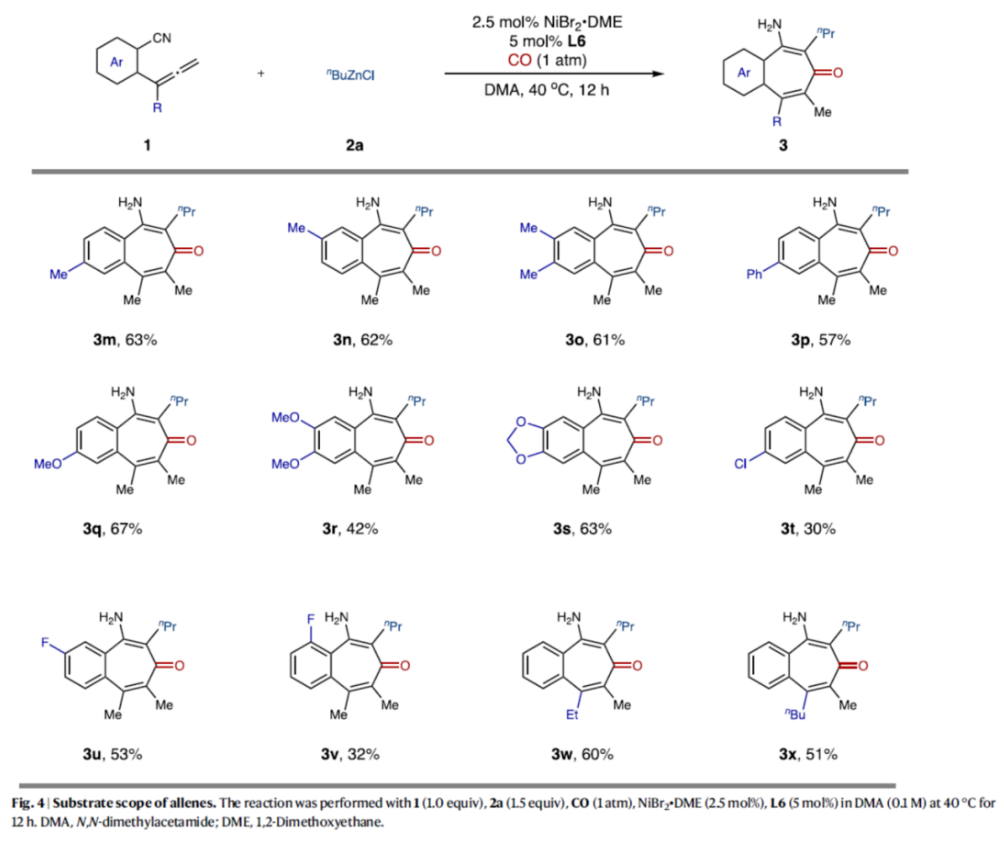
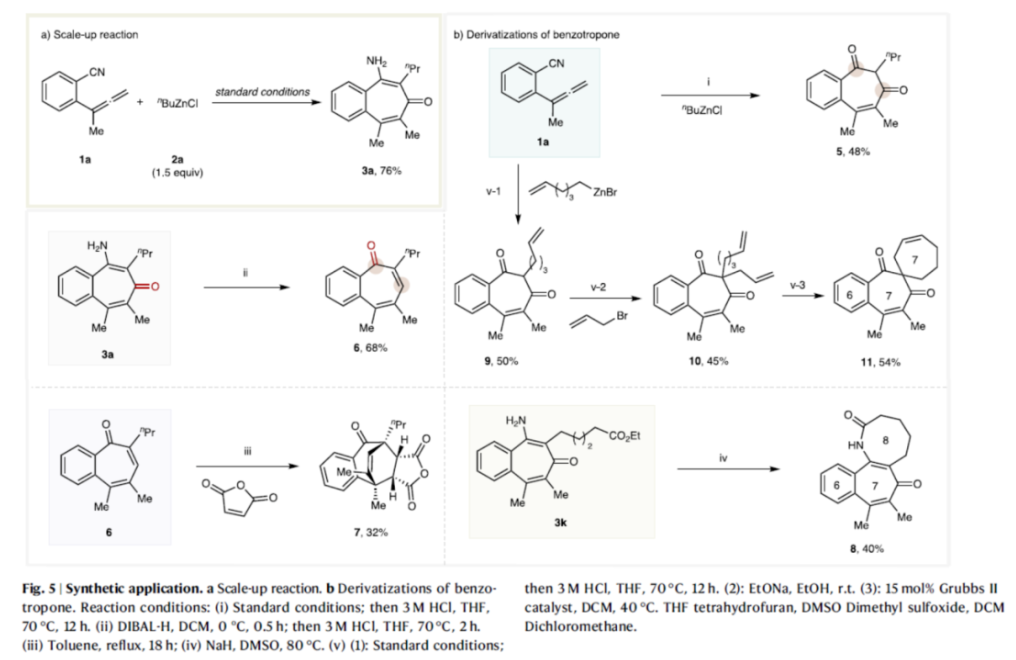
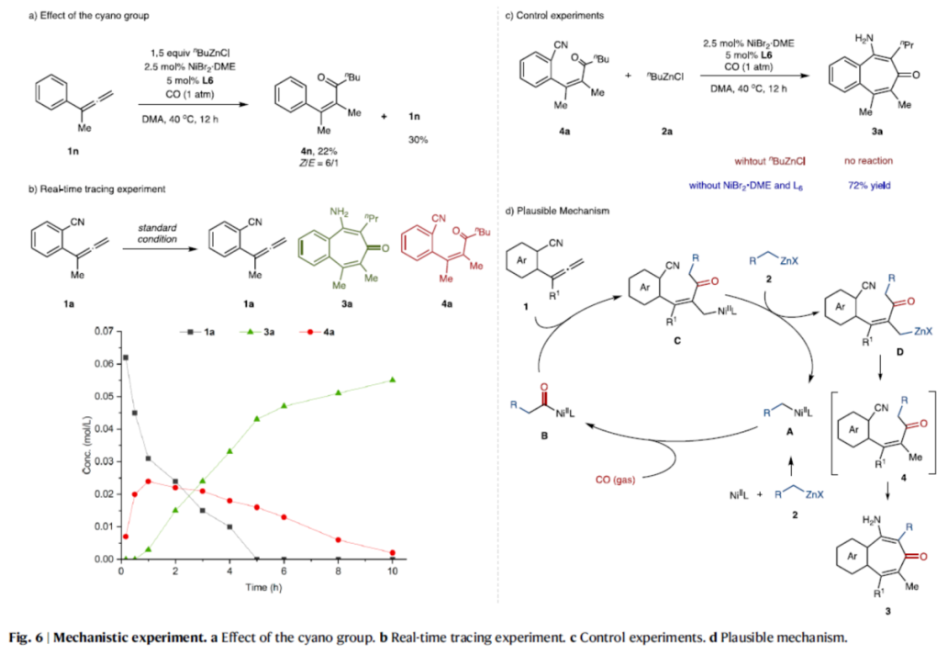
正文 过渡金属催化不饱和烃的碳金属化反应,可同时实现两个C-C键的构建,为从广泛可用的原料中直接获得复杂分子提供了便利(Fig. 1a)。然而,上述的策略主要利用富含电子的有机金属作为亲核单元,如有机锂、格氏试剂和有机锌试剂(Fig. 1a,left)。相比之下,利用酰基合成子作为亲核试剂参与过渡金属催化不饱和碳-碳键的碳金属化反应,却较少有相关的研究报道(Fig. 1a,right)。2023年,陈宜峰课题组(Nat. Synth. 2023, 2, 261.)首次报道了一种镍催化活性不饱和烃、官能团化有机锌试剂与CO的酰基金属化反应,涉及原位形成催化活性酰基镍中间体的过程,其中镍催化剂与双齿或三齿含氮配体的组合抑制了非活性Ni(CO)4配合物的形成。这种化学、区域和立体选择性酰基锌化策略为碳金属化反应开辟了新的应用前景。苯磺酰胺取代炔酰胺的串联酰基锌化/ Smiles重排反应,可合成高度官能团化的四取代的β-氨基烯酮衍生物(Fig. 1b,i);α,β-不饱和酮参与的串联酰基锌化/Aldol缩合反应可以获得多取代的环戊烯酮类衍生物(Fig. 1b,ii)。尽管如此,酰基金属化引发的串联反应仍有待进一步的开发。联烯的不饱和碳-碳键可以发生形式多样的碳金属化反应,从而增加了化学选择性地发生CO参与的酰基金属化的难度(Fig. 1b,iii)。此外,区域选择性和立体选择性的精准调控是另外需要克服的障碍。近日,华东理工大学陈宜峰课题组开发了一种镍催化联烯、烷基锌试剂与CO(1 atm)的三组分串联酰基锌化/环化反应,合成了一系列全取代的苯并环庚三烯酮衍生物(Fig. 1c)。下载化学加APP到你手机,更加方便,更多收获。 (图片来源:Nat. Commun.) 首先,作者以联烯衍生物1a、nBuZnCl 2a与CO(1 atm)作为模型底物,进行了相关反应条件的筛选(Fig. 2)。当以NiBr2•DME(2.5 mol %)作为催化剂,L6(5 mol %)作为配体,在DMA溶剂中40 oC反应12 h,可以71%的分离收率得到产物3a。 (图片来源:Nat. Commun.) 在获得上述最佳反应条件后,作者对烷基锌试剂的底物范围进行了扩展(Fig. 3)。研究表明,一系列不同烷基取代的锌试剂,均可与1a顺利反应,获得相应的产物3a-3l,收率为32-71%。值得注意的是,一系列活性的基团(如烯基、卤素等)均与体系兼容。 (图片来源:Nat. Commun.) 紧接着,作者对联烯的底物范围进行了扩展(Fig. 4)。研究结果表明,当底物1中的芳基上含有-Me、-Ph、-OMe、-Cl、-F等时,均可与2a顺利反应,获得相应的产物3m-3v,收率为30-67%。同时,当底物1中的R为-Et与-nBu时,也能够顺利进行反应,获得相应的产物3w(收率为60%)和3x(收率为51%)。 (图片来源:Nat. Commun.) 随后,作者对反应的实用性进行了研究(Fig. 5)。首先,克级规模实验,同样能够以76%收率得到产物3a。其次,1a在标准条件下反应后,再于3M HCl/THF条件下进行水解反应,可以48%的收率得到1,3-环庚二酮产物5(Fig. 5b, i)。3a在DIBAL-H/DCM与3M HCl/THF条件下分别进行还原与水解反应,可以68%的收率得到羰基转位产物6(Fig. 5b,ii)。化合物6可与马来酸酐通过进一步的Diels-Alder反应,可以32%的收率得到endo型环化产物7(Fig. 5b,iii)。3k在NaH/DMSO条件下进行分子内酯交换反应,可以40%的收率得到苯并-7,8-双环产物8(Fig. 5b,iv)。此外,1a与烯基取代的烷基锌试剂在标准条件下反应后,再于3M HCl/THF条件下进行水解反应,可以50%的收率得到1,3-环庚二酮产物9(Fig. 5b,i)。9与烯丙基溴在EtONa/EtOH条件下进行烯丙基化反应,可以45%的收率得到化合物10。10在Grubbs II/DCM条件下进行分子内RCM反应,可以54%的收率得到螺体化合物11。 (图片来源:Nat. Commun.) 此外,作者还对反应机理进行了进一步的研究(Fig. 6)。首先,1n的对照实验结果表明,氰基不仅作为亲电单元,显著提高了反应效率,而且作为导向基团,提高了该反应的立体选择性和区域选择性(Fig. 6a)。其次,实时跟踪实验结果表明,化合物4a可能是该反应的中间体(Fig. 6b)。此外,控制实验结果表明,有机锌试剂对于中间体4a的环化过程是必需的(Fig. 6c)。基于上述的研究以及相关文献的查阅,作者提出了一种合理的催化循环过程(Fig. 6d)。首先,镍催化剂与烷基锌试剂经金属转移后生成烷基镍配合物A。配合物A与CO经1,1-插入反应后,生成酰基镍中间体B。其次,中间体B与联烯1经迁移插入,生成烯丙基镍配合物C。配合物C与烷基锌试剂再次进行金属转移,生成有机锌中间体D,并再生活性催化剂A。最后,有机锌中间体D通过质子化与分子内缩合反应,可获得目标产物3。 (图片来源:Nat. Commun.) 总结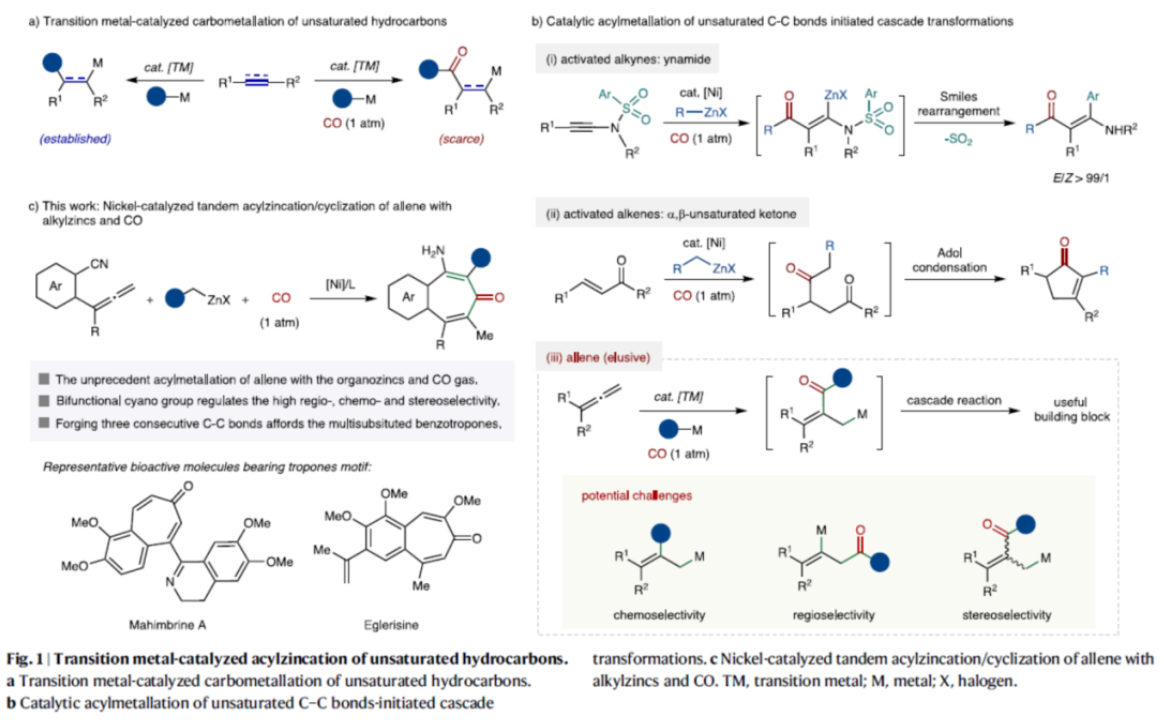
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn