

(图片来源:J. Am. Chem. Soc.)
正文
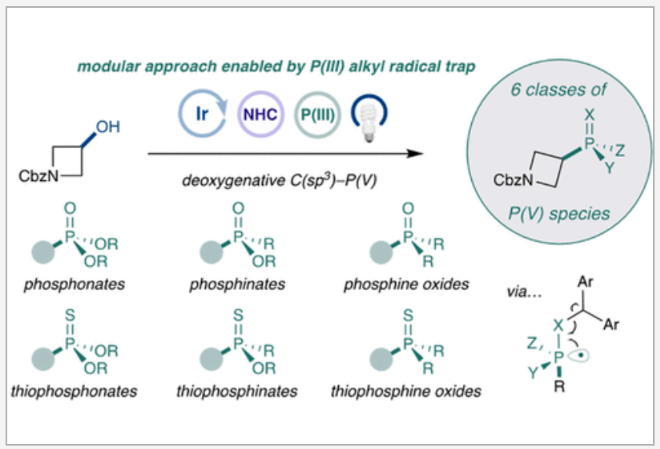
有机膦官能团在调节一系列细胞过程中发挥着极其重要的作用,其中包括蛋白质信号级联、炎症、细胞代谢和基因表达等。因此,有机膦化合物广泛存在于药物、农用化学品和功能材料中。虽然利用钯催化、芳基碘盐以及光氧化还原催化等方法可以实现芳基C−P(V)键的构建,但形成相应的烷基C−P(V)键的方法还有待拓展。近日,美国普林斯顿大学默克催化中心David W. C. MacMillan课题组发展了一种通用的,氧化还原可调控的有机膦烷基自由基捕获策略,实现了C(sp3)−P(V)的构建(Figure 1)。下载化学加APP到你手机,收获更多商业合作机会。
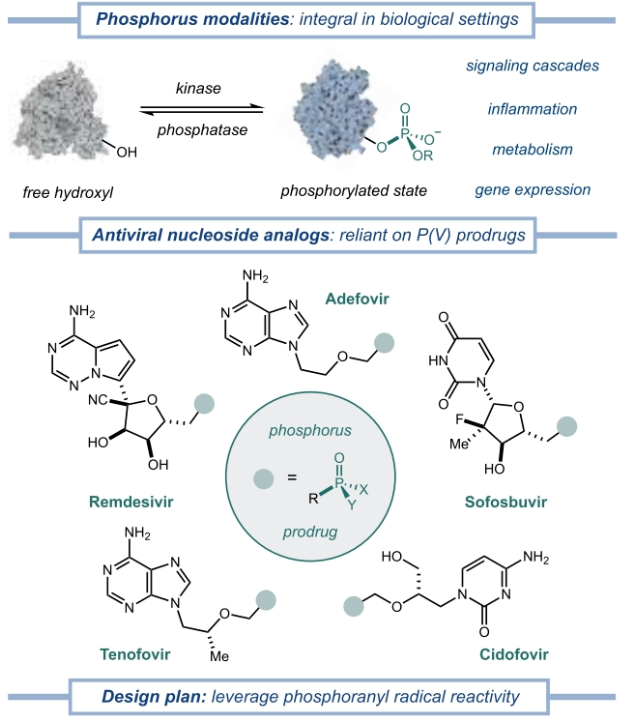
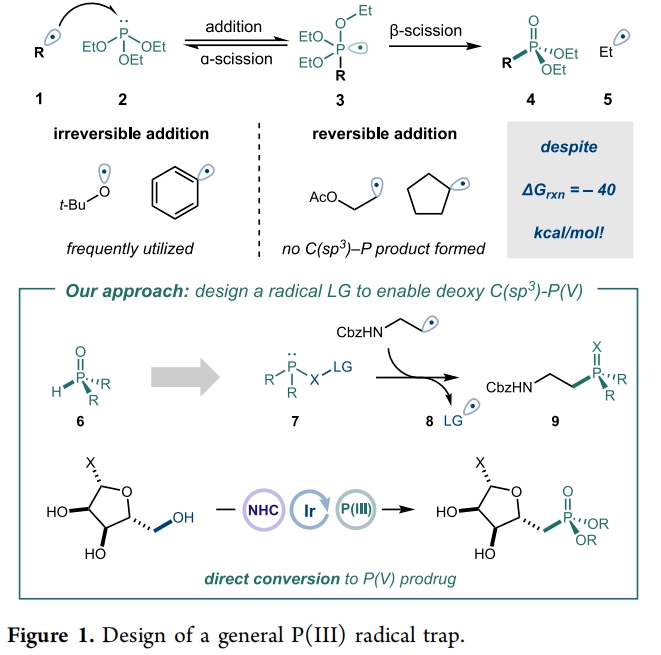
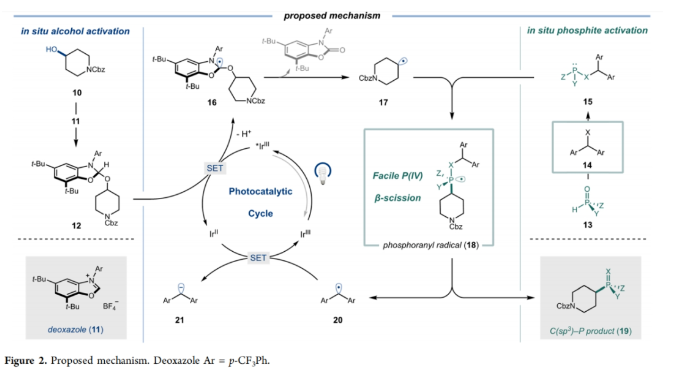
作者使用简单易得的起始原料通过原位预活化过程来实现此转化(Figure 2)。这种模块化方法利用“即插即用”(“plug-and-play”)策略实现了C(sp3)-P(V)键的构建。首先,烷基自由基前体(10)与脱氧噁唑(11, NHC)进行快速(~ 30分钟)、温和的缩合,生成具有活性的醇加合物(12)。与此同时,在另一个单独的反应瓶中,由廉价易得的O=P(R)2H前体(13)和二苯甲醇衍生物(14)可以制备出带有自由基离去基的不对称P(III)试剂(15)。随后作者将这种混合物直接添加到含有活性醇、光催化剂和碱的反应瓶中。在450 nm光照射下,达到了铱光催化剂的长寿命三线态。这种高度氧化状态使得12 (E1/2 ox≈1.0 V vs SCE in MeCN)易于氧化,随后通过去质子化得到杂环自由基(16)。该物种通过β-裂解产生烷基自由基(17)和惰性的重新芳构化NHC副产物。接下来,17通过与活化的P(III)物种进行可逆的加成形成磷酰基自由基(18);随后由弱C−O键驱动的不可逆的β-裂解得到脱氧膦化产物(19)和双苄基自由基(20)。最后,通过还原RPC(radical polar crossover)(E1/2 red≈−0.77 V vs SCE in MeCN)完成光催化循环得到碳负离子(21)。
(图片来源:J. Am. Chem. Soc.)
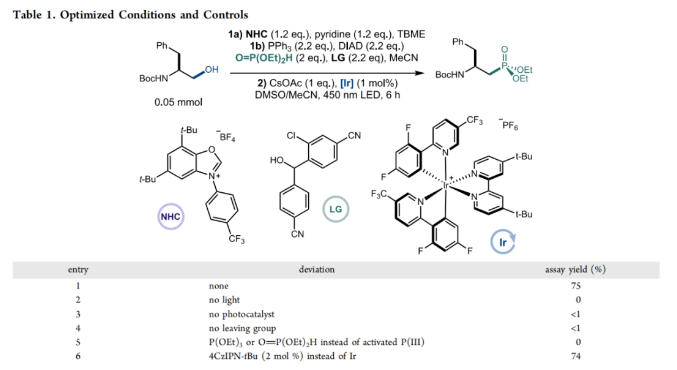
首先,作者以Boc-保护的L-苯丙胺醇和亚磷酸二乙酯作为模板底物对反应条件进行了探索(Table 1)。通过一系列条件筛选,作者发现当首先使用NHC (1.2 equiv), 吡啶(1.2 equiv), 在TBME中反应;随后加入PPh3 (2.2 equiv), DIAD (2.2 equiv), HP(O)(OEt)2 (2.0 equiv), LG (2.2 equiv), 在MeCN中反应;接下来,加入CsOAc (1.0 equiv), [Ir] (1 mol%), 在DMSO/MeCN中450 nm光照射下反应6小时,可以以75%的产率得到相应的脱氧膦化产物(entry 1)。控制实验表明,在不存在光照或光催化剂时反应不发生(entries 2, 3)。此外,LG的存在对此转化至关重要(entry 4)。当使用有机光催化剂4CzIPN-tBu代替铱催化剂参与反应时,仍可以以74%的产率得到脱氧膦化产物(entry 6)。
(图片来源:J. Am. Chem. Soc.)
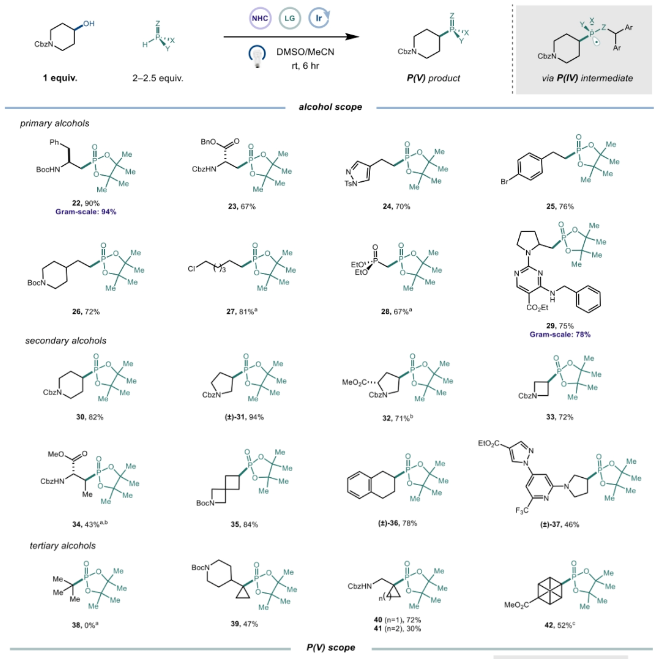
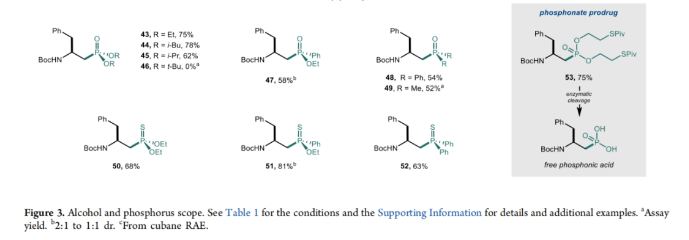
在得到了最优反应条件后,作者对此转化的底物范围进行了考察(Figure 3)。实验结果表明一系列不同取代的一级醇、二级醇和连有三元环的三级醇均可顺利实现转化,以43-90%的产率得到相应的产物22-42。其中包括还原的氨基酸、杂芳环、饱和杂环、烷基卤等骨架和基团均具有良好的兼容性。值得注意的是,此转化在克级规模合成中仍展现出较高的效率(22, 94%; 29, 78%)。此外,不同的膦氢化合物,如亚磷酸酯、二芳基(烷基)氧膦及其相应的硫羰基衍生物均可兼容此转化,以52-81%的产率得到相应的产物43-45, 47-52。遗憾的是,亚磷酸叔丁酯可能由于立体位阻的原因不能参与反应(46)。
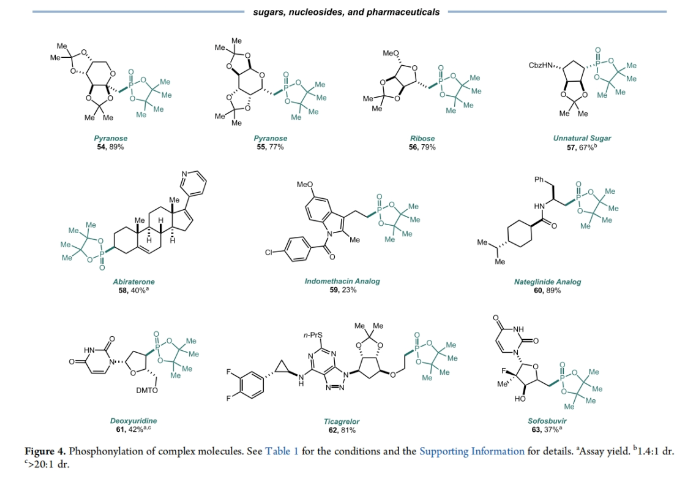
最后,作者探索了糖、核苷以及药物分子在此转化中的普适性(Figure 4)。欣慰的是,吡喃糖、核糖和非天然糖衍生物均可顺利参与反应,以67-89%的产率得到产物54-57。此外,含有杂芳基乙烯骨架的类固醇阿比特龙(abiraterone)同样可以以中等产率(58,40%)实现膦化过程。其它药物骨架,包括吲哚美辛(indomethacin)(59, 23%)、那格列奈(nateglinide)类似物也同样可以实现转化,(60, 89%),由此表明该转化在小分子药物修饰中的潜力。此外,此反应对脱氧尿苷(deoxyuridine)、替格瑞洛(ticagrelor)以及索非布韦(sofosbuvir)等核苷类似物同样兼容,以37-82%的产率得到相应的膦化产物61-63。这种后期官能团化策略为探索核苷衍生的治疗方法提供了新的机会。
(图片来源:J. Am. Chem. Soc.)
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn