

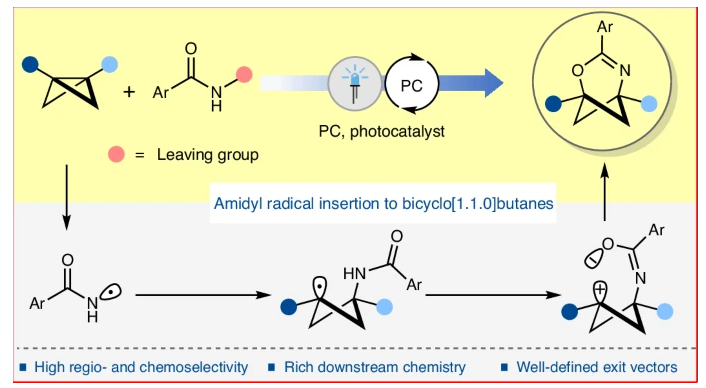
正文
用富含C(sp3)的等排体类似物(如双环[n.1.1]烷烃)来取代药物分子中的平面芳环通常可以显著改变其理化性质和药代动力学性质,并且通常会提高临床成功率。然而,与苯环不同的是,结构刚性的富含C(sp3)的杂芳环等排体类似物是非常罕见的。杂双环[n.1.1]烷烃在这方面很有潜力,但目前缺乏模块化的合成方法阻碍了化学家们对它们的探索。如果在双环[1.1.0]丁烷中策略性地和选择性地引入不同的杂原子单元,可以实现一个高模块化的策略来获取不同的杂环[n.1.1]烷烃。近期,德国明斯特大学Frank Glorius课题组发展了光氧化还原催化策略,实现了酰胺基自由基高区域选择性和化学选择性的插入到了双环[1.1.0]丁烷中,实现了一系列2-氧-4-氮杂环[3.1.1]庚-3-烯的合成(Fig. 1)。欢迎下载化学加APP到手机桌面,合成化学产业资源聚合服务平台。
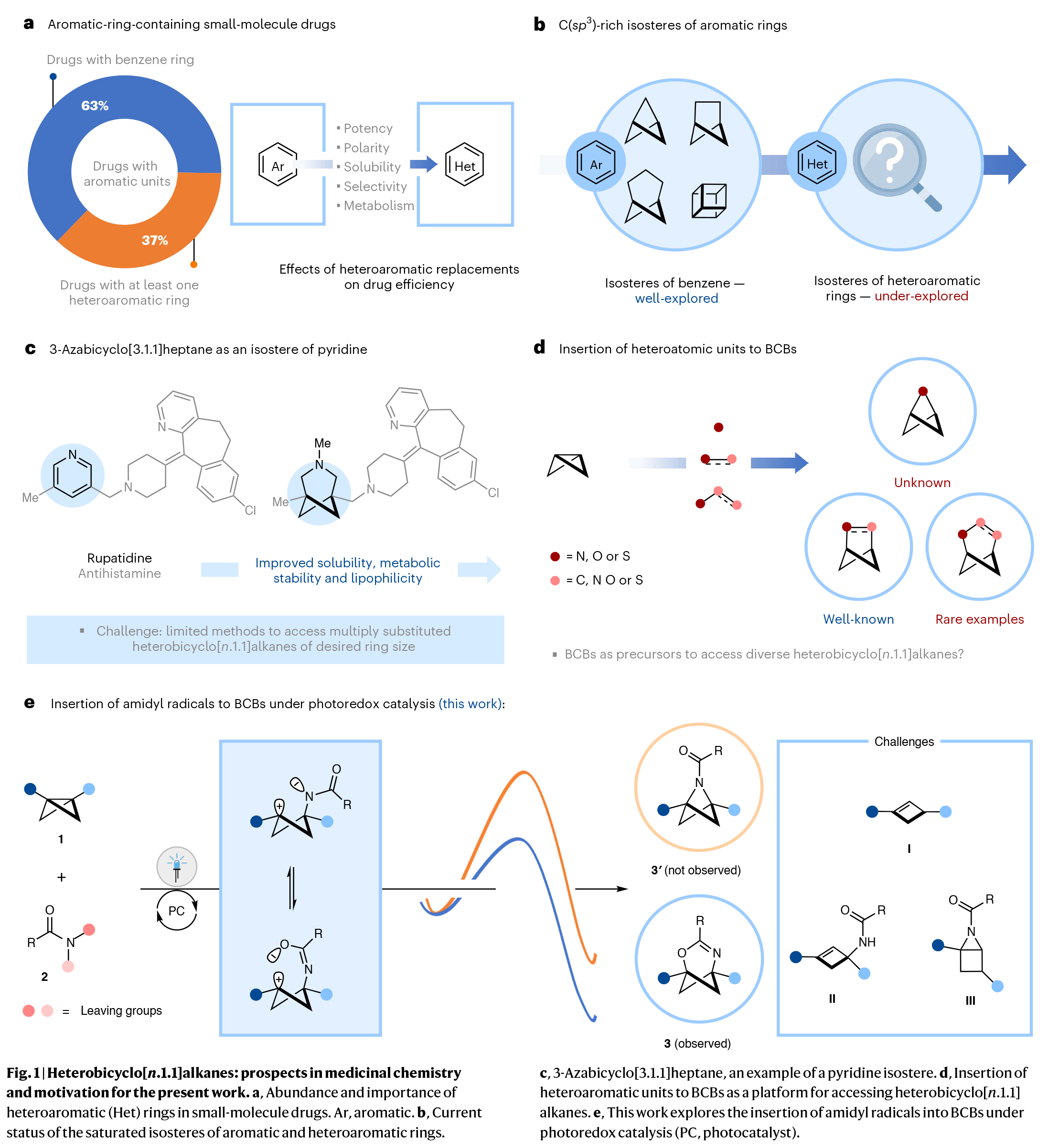
(图片来源:Nat. Catal.)
首先,作者以二取代的BCB(bicyclo[1.1.0]butanes, BCBs, 双环[1.1.0]丁烷) 1a和酰胺基自由基前体2作为模板底物进行条件筛选(Fig. 2)。通过对反应条件和反应试剂所进行的一系列筛选,作者发现当使用1a (1.0 equiv), 2d (2.0 equiv), NaHCO3 (1.0 equiv), fac-Ir(ppy)3 (2 mol%), 在CH2Cl2 (0.1 M)中, 30 W 蓝光 (λmax = 450 nm)照射下室温反应16小时,可以以68%的分离产率得到产物3a(entry 13)。此外,作者基于反应条件的敏感性筛选得出,该方案仅对含水量和高氧敏感,而反应浓度、温度和光照强度对反应结果的影响较小。
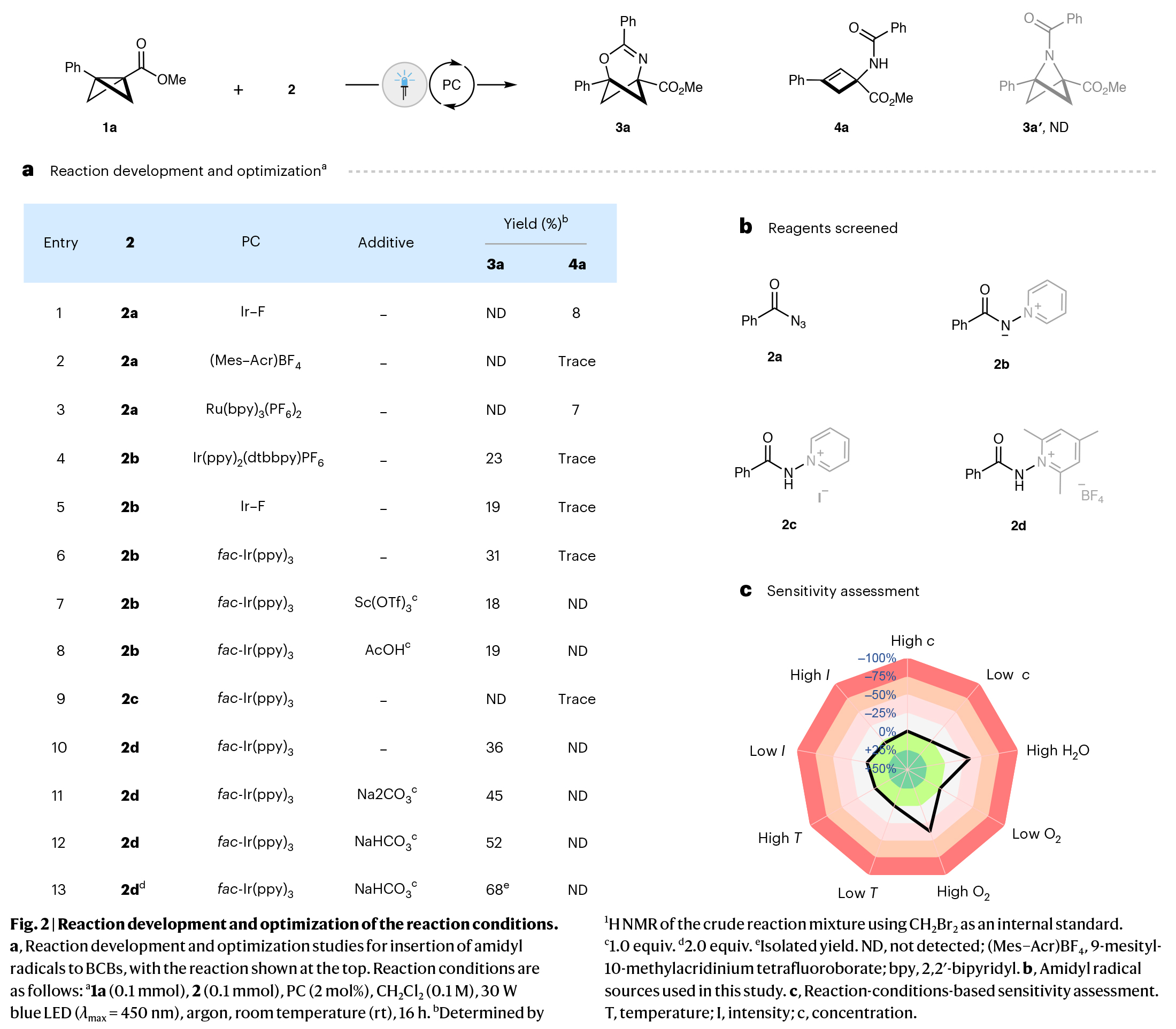
(图片来源:Nat. Catal.)
在得到了最优反应条件后,作者对此转化的底物范围进行了探索(Fig. 3)。实验结果表明,一系列不同取代的BCB化合物具有良好的兼容性,以48-68%的产率得到相应的产物3a-3n。其中包括酯基、卤素、三氟甲基、甲氧基、甲基、苯基、三氟甲氧基、酰胺基、羰基等一系列官能团均可兼容。此外,不同取代的N-酰氨吡啶叶立德同样具有良好的兼容性,以51-71%的产率得到相应的产物3o-3z, 3aa-3ac。值得注意的是,此转化还可以兼容复杂生物活性分子如menthol和geraniol,分别以56%和53%的产率得到相应的产物3ad和3ae。当酰基吡唑取代的BCB 1o与2d反应时,可以以47%的产率得到螺环产物5,而并非常规的酰胺基自由基插入产物。这可能是由于吡唑部分的高亲核性,可以与反应中产生的碳正离子中间体6竞争反应。在目前的酰胺基自由基插入反应中,单取代和甲基取代的BCBs是不可兼容的底物。同样,当使用脂肪族酰胺基自由基前体时,也没有得到期望的产物(3ai和3aj)。
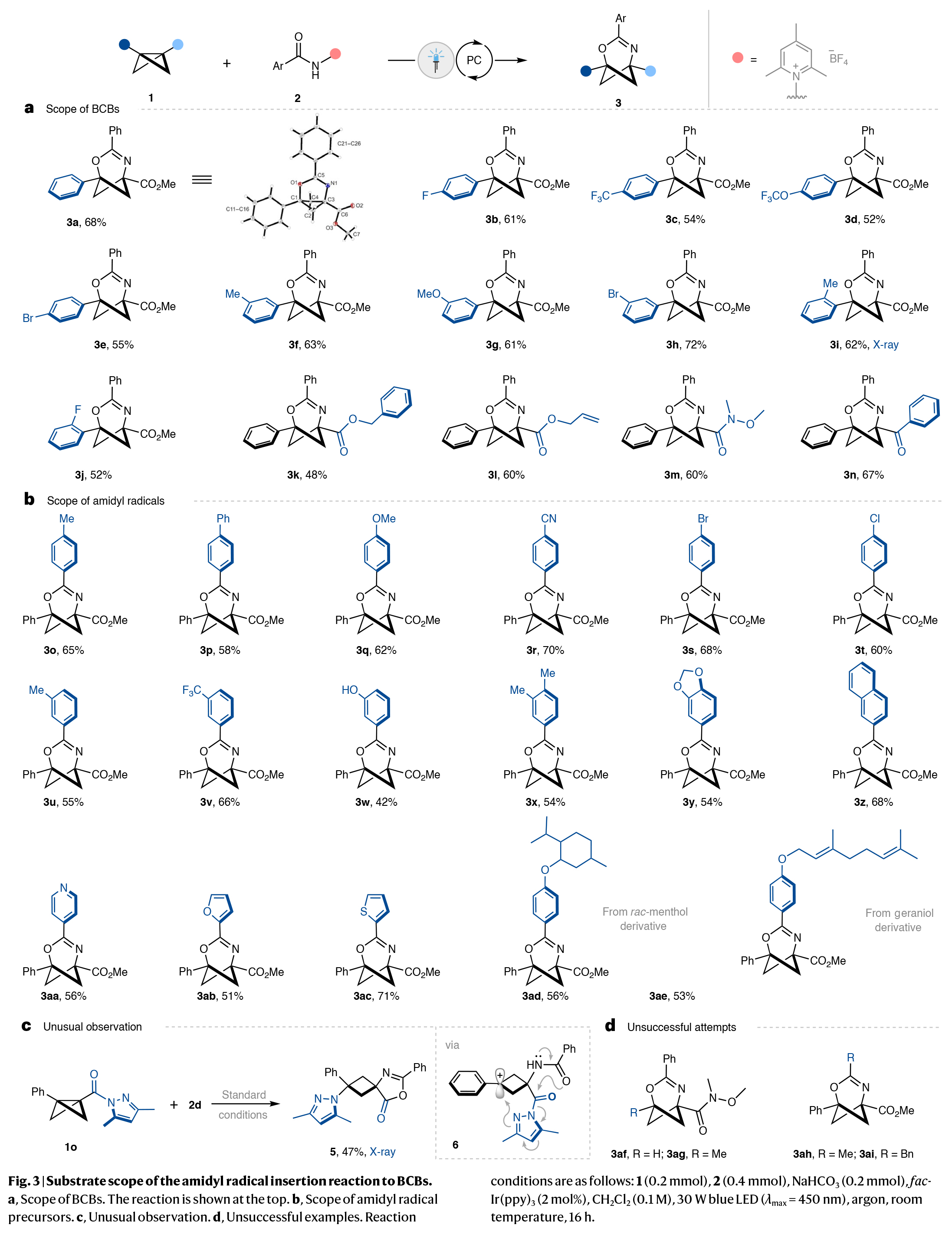
(图片来源:Nat. Catal.)
由于新合成的产物具有结构刚性和明确的exit vectors。因此,作者利用exit vector分析表明,3a的角α值和距离r和d值与吡啶(8)和嘧啶(9)衍生物非常相似,这为这些化合物作为此类重要杂环骨架的潜在等排体类似物的适用性提供了初步的探索(Fig. 4a)。随后,作者对产物3a和3s进行了一系列的衍生化实验,包括将酯基转化为羟基或醛基、芳基卤的Suzuki–Miyaura交叉偶联等,以48-84%的产率得到相应的衍生物10-15(Fig. 4b)。
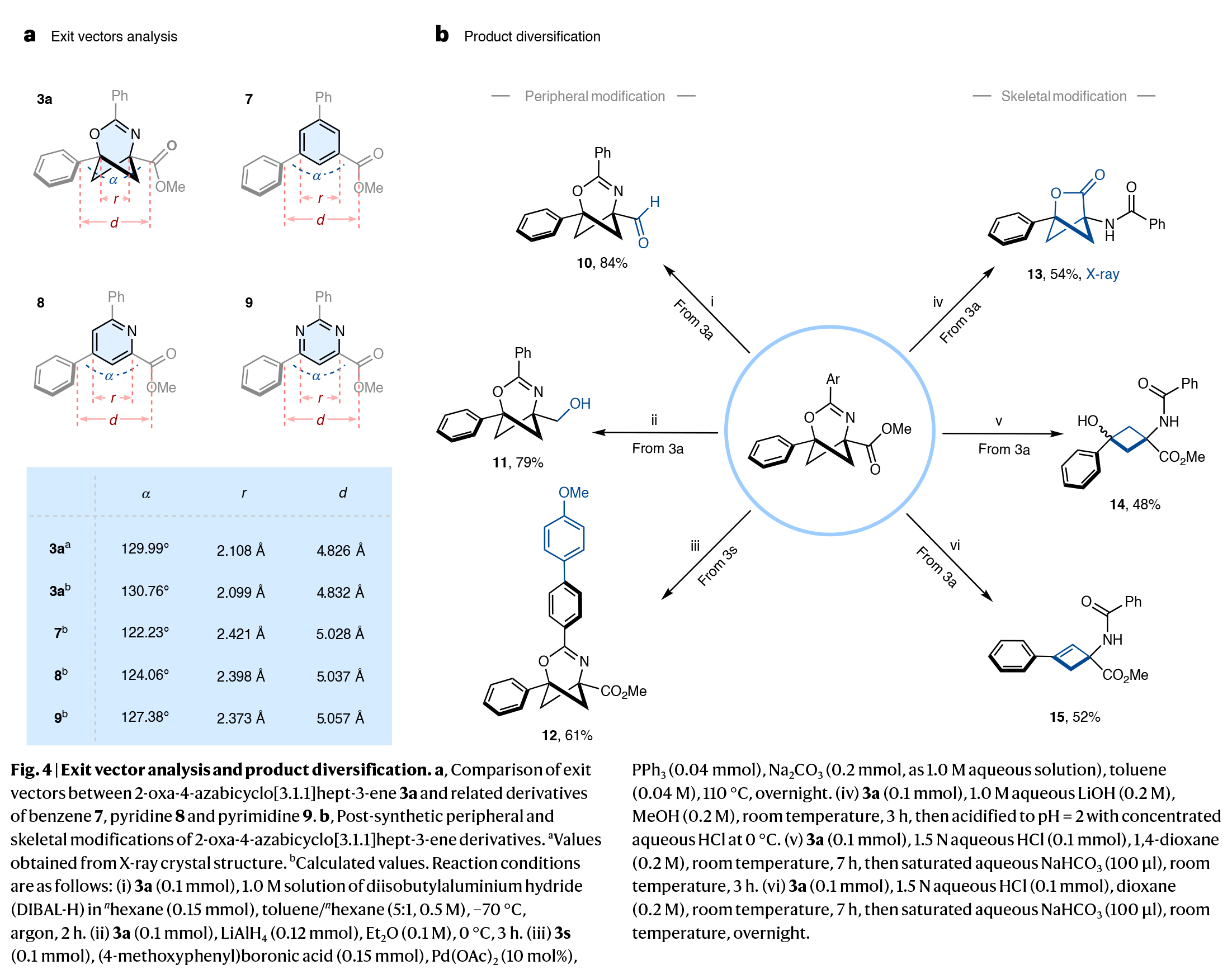
(图片来源:Nat. Catal.)
为了深入理解反应机理,作者进行了一系列机理探索实验(Fig. 5),并得出如下结论:1)2d’可能为此转化的活性物种(Fig. 5a);2)碳酸根可能会与2d的NH质子存在氢键相互作用(Fig. 5b);3) 在没有光催化剂存在下反应基本不发生(Fig. 5c);4) 紫外-可见吸收光谱表明,2d与NaHCO3混合与2d相比,吸收有所增加,但光催化剂在450 nm处仍然是高吸收物质(Fig. 5d);5) CV 实验表明,2d与NaHCO3混合和2d均可以被还原产生酰胺基自由基(Fig. 5e);6) Stern–Volmer荧光淬灭实验表明,2d和2d与NaHCO3混合均能有效淬灭激发态光催化剂(Fig. 5f),但2d的淬灭速率略高(Fig. 5f);7)该转化的量子产率Φ = 0.08,表明自由基链途径在此转化中可能不起作用(Fig. 5g);8)自由基捕获实验表明反应中涉及酰胺基自由基和环丁基自由基(Fig. 5h);9)碳正离子捕获实验表明,反应中涉及环丁基碳正离子中间体(Fig. 5i)。
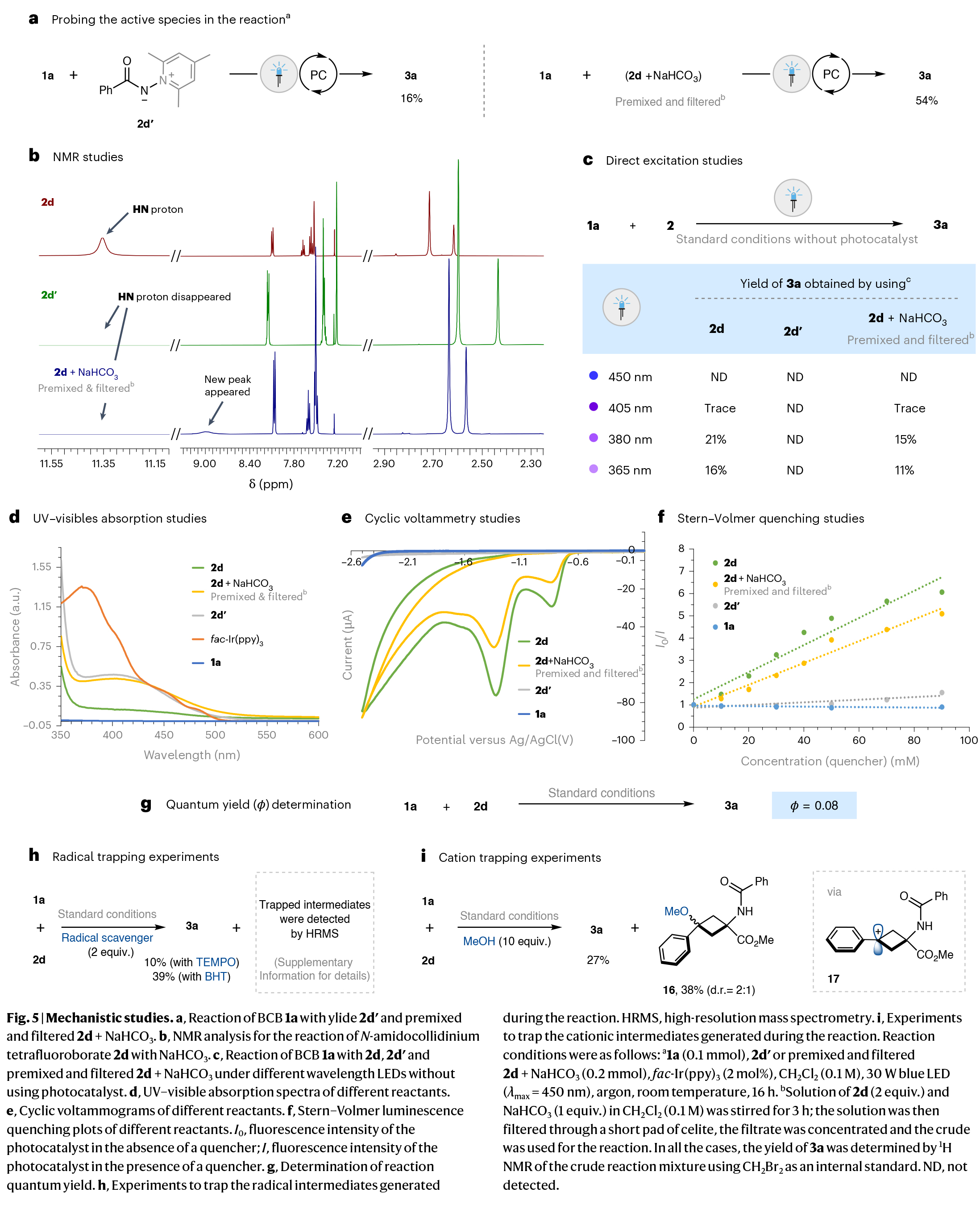
(图片来源:Nat. Catal.)
基于上述实验结果,作者进行了DFT计算,并推测反应可能是按照如下机理进行的(Fig. 6):首先,光照所生成的激发态Ir(III)光催化剂与2d(过渡态与反应物的吉布斯自由能之差ΔG‡= 3.3 kcal mol-1)进行SET反应,形成氧化物种Ir(IV)和氨基自由基Int 1。随后在1a的桥头C1-C3 σ-键上加成的酰胺基自由基产生了环丁基自由基Int-2和Int-2a,是高度放热的。与实验观察结果一致,在动力学和热力学上,苄基自由基Int-2的生成比α-酰氨基自由基Int-2a的形成更有利(过渡态TS-1 ΔG‡= 14.4 kcal mol-1,过渡态TS-1a为16.5 kcal mol-1,吉布斯自由能变化ΔG = -42.8 kcal mol-1,过渡态Int-2a为-36.0 kcal mol-1),这可以从自由基极性匹配的角度来解释。即瞬态亲电酰胺即自由基倾向于在BCB σ-键的亲核位置加成。接下来,利用Int-2的放热SET(ΔG‡= 2.7 kcal mol-1)可以得到稳定的苯基碳正离子Int-3 (ΔG = -9.0 kcal mol-1)并再生Ir(III)光催化剂。通过碱介导的酰氨基氧原子的亲核进攻,可以经历环化产生产物3a,其是高度放热的过程(ΔG = -27.1 kcal mol-1)。另一种环化途径是由酰氨基氮原子介导的亲核进攻,导致2-氮杂BCP 3a’。由于其形成相关的高张力能(TS-2’ΔG‡= 14.2 kcal mol-1, 3a ' ΔG = 1.0 kcal mol-1),因此在动力学和热力学上均是不利的。
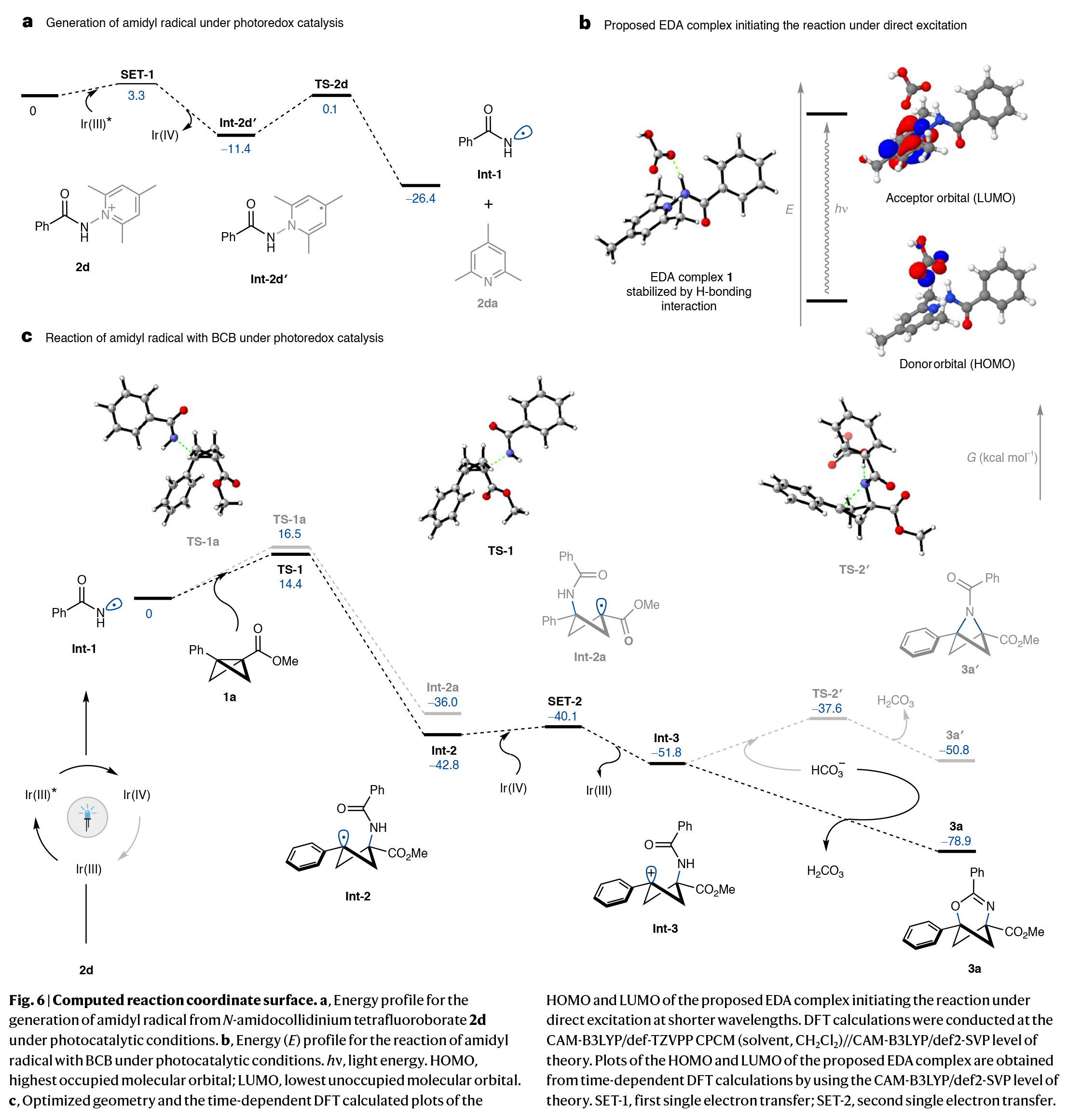
(图片来源:Nat. Catal.)
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn