- 首页
- 资讯
Nature:绝!从两个高张力物种合成双环[2.1.1]己烷
来源:化学加原创 2025-02-16
导读:近日,美国加州大学洛杉矶分校(University of California, Los Angeles)Neil K. Garg课题组与K. N. Houk课题组联合报道了在温和条件下,通过简单操作构建重要分子骨架双环[2.1.1]己烷结构。该转化的反应机理涉及两种高张力片段的非常规偶联:即瞬时生成的环状联烯和双环[1.1.0]丁烷的偶联。该反应是通过双自由基途径进行的σ-键插入反应。然而,与需要外部条件才能生成自由基物种不同的是,该反应的活性源于反应物本身所固有的双自由基特性,即源于每个反应物的严重几何扭曲。此研究提供了一种获取具有药物发现价值的官能化双环[2.1.1]己烷的途径,揭示了如何利用反应物的几何扭曲来实现不常见的反应模式。文章链接DOI:10.1038/s41586-025-08745-1。
(图片来源:Nature)
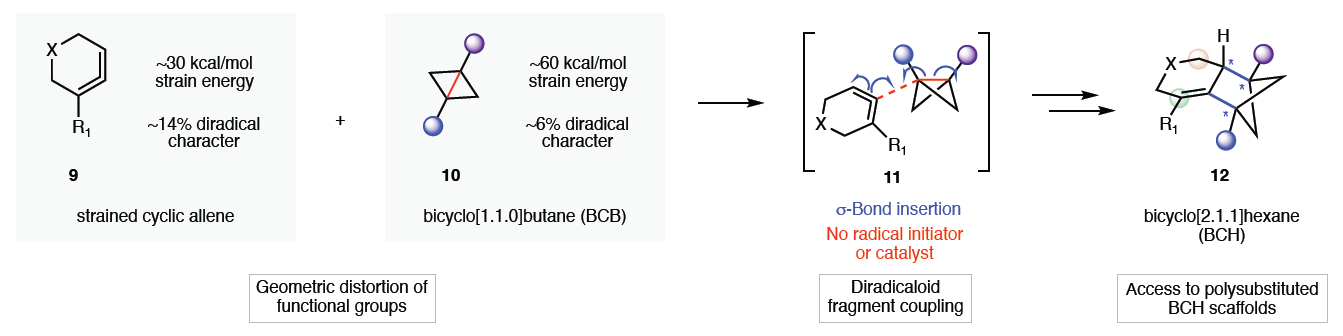
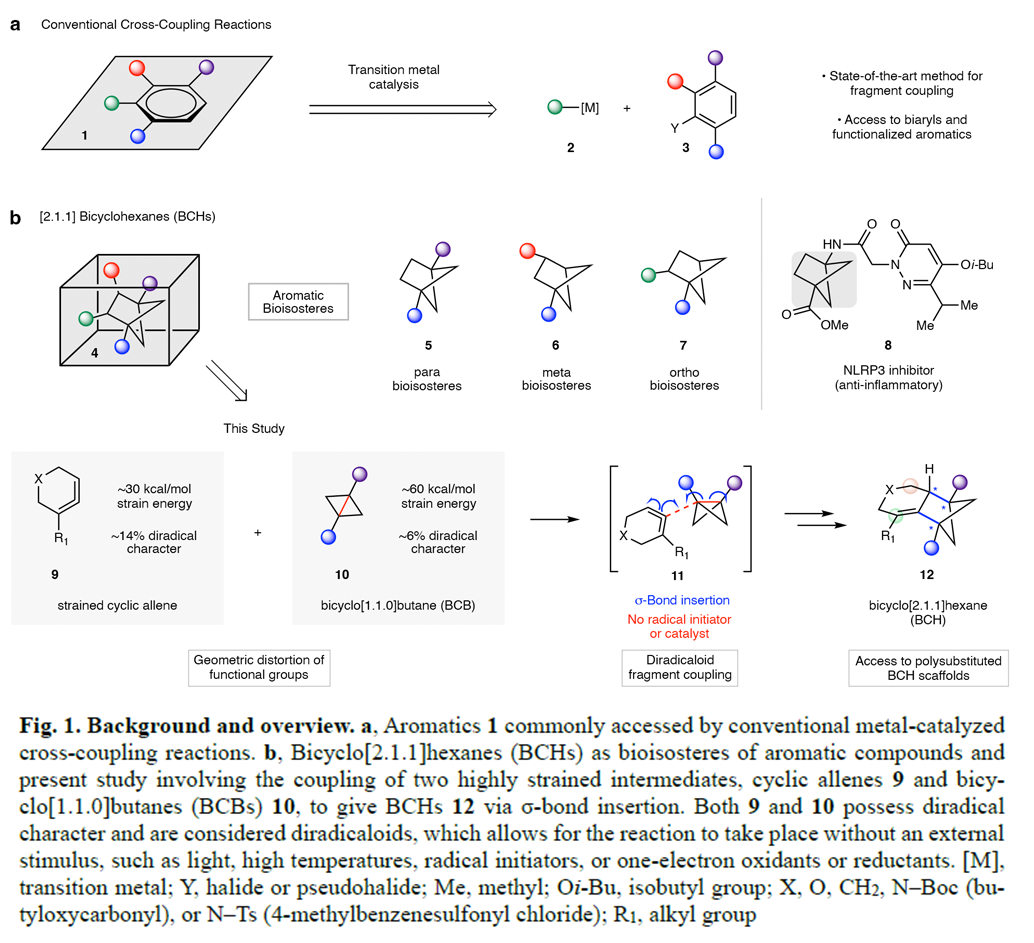
新型合成方法的发展对于新药的发现具有及其重要的推动作用。特别是那些能够高效合成芳香化合物类似物(如芳环的饱和生物电子等排体)的方法,已成为高度追捧的研究方向。这类生物电子等排体的引入通常能够改善药物的类药性,并呈现了一个新兴的研究领域。最近,美国加州大学洛杉矶分校Neil K. Garg课题组与K. N. Houk课题组联合报道了一种构建双环[2.1.1]己烷骨架的新方法。其通过瞬时生成的环状联烯和双环[1.1.0]丁烷这两种高张力片段的非常规偶联,在温和的反应条件下通过σ-键插入反应实现了双环[2.1.1]己烷的构建(Fig. 1)。欢迎下载化学加APP到手机桌面,合成化学产业资源聚合服务平台。首先,作者考察了各反应物的基态结构。Fig. 2a展示了环联烯14与简单线状烯烃13的对比分析。将线状烯烃单元限制在六元环中会产生约30 kcal/mol的张力能。此外,作者通过DFT计算对14的结构进行了几何优化,并分析了其中存在的三种不同类型的几何扭曲。在同一个化合物中同时存在这三种几何扭曲是很罕见的,这使得张力环联烯具有高度的反应活性。Fig. 2b展示了双环[1.1.0]丁烷(BCB)16中的张力和几何扭曲。将饱和骨架限制在BCB的小而刚性的环系中,会产生约64 kcal/mol的高张力能。值得注意的是,尽管环联烯的张力能低于BCB,但它们是瞬态物种,而BCB通常可以分离得到。BCB的张力能比两个环丙烷的张力能之和高出约10 kcal/mol。接下来,作者以环联烯前体17和BCB 18作为模板底物对此转化的反应条件进行了考察(Fig. 2c)。通过一系列条件筛选,作者发现当使用17 (1 equiv.), 18 (3.0 equiv.), CsF (5.0 equiv.), Bu4NBr (1 equiv.), 在DME (0.2 M)中23 ºC反应16 h可以以98%的核磁产率得到双环[2.1.1]己烷(BCH)产物19(entry 9)。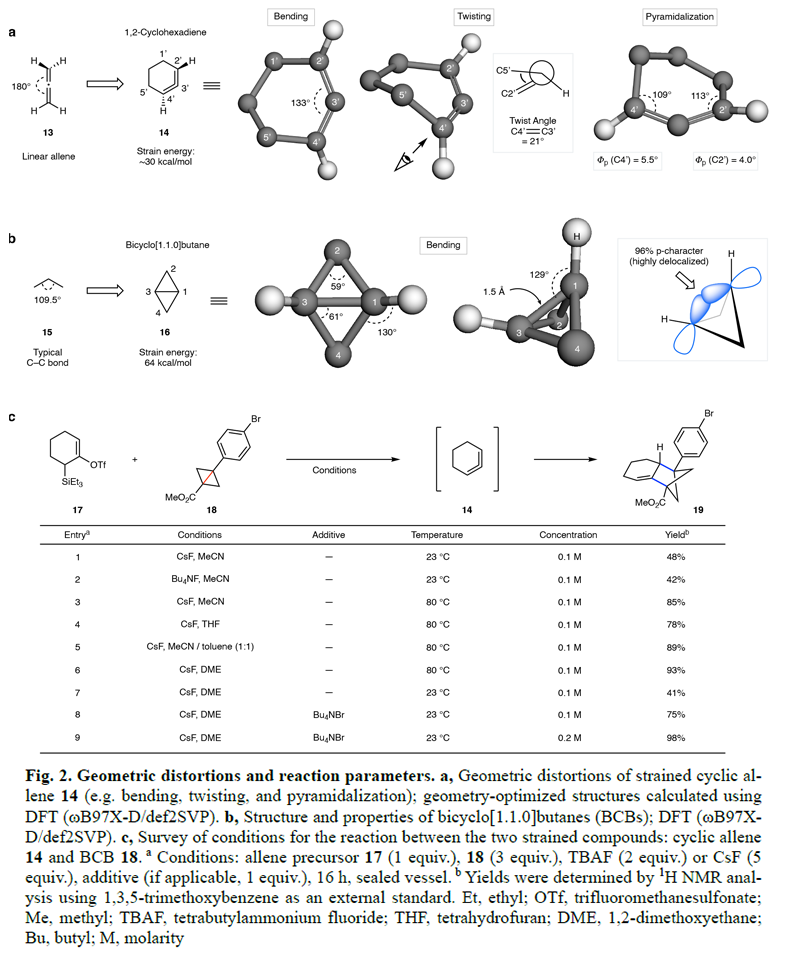
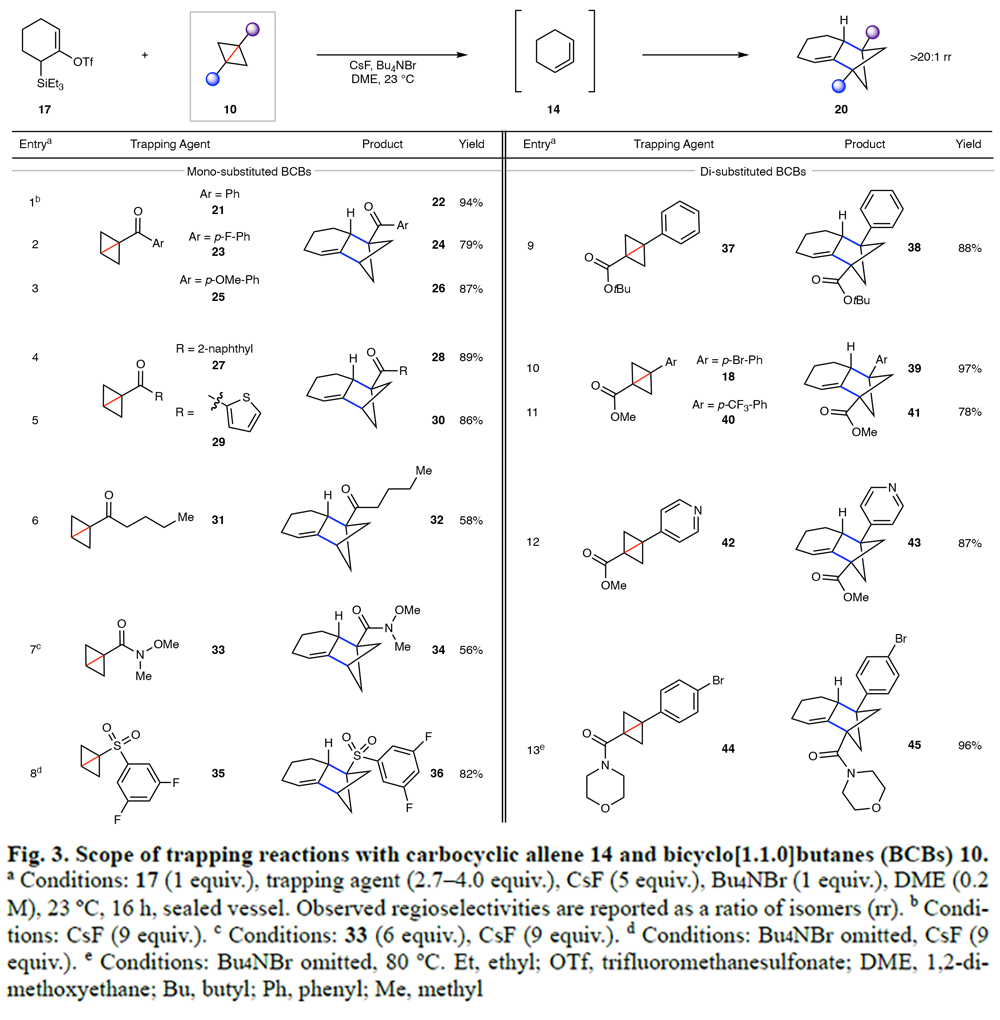
在得到了最优反应条件后,作者分别对BCBs(Fig. 3)和环联烯片段(Fig. 4)的底物范围进行了考察。实验结果表明,单取代和二取代的BCBs以及碳环和杂环联烯均可顺利实现转化,以56-96%的产率得到相应的BCH产物。整体来讲,Fig. 3和Fig. 4的结果共同展示了两类张力化合物(瞬时生成的环联烯和张力双环[1.1.0]丁烷)之间的高效偶联。值得注意的是,这些反应仅需在室温下进行,且无需外部刺激(如高温、路易斯酸、光照、自由基引发剂或单电子氧化剂/还原剂),并且在反应过程中未发生分解或二聚现象。一般而言,BCB环连接处需要带有吸电子基团或芳香取代基,以确保反应高效进行。作者推测,这些取代基对于促进BCB的C-C键断裂以及通过共振稳定生成的自由基中间体至关重要。另一方面,BCB上的烷基取代基则不耐受,这些实验现象的原因有待进一步研究。此反应具有一定的区域选择性,能够生成多取代的(BCH)产物,此类产物非常适合进一步的官能团修饰,从而为合成化学提供了一种有价值的新工具。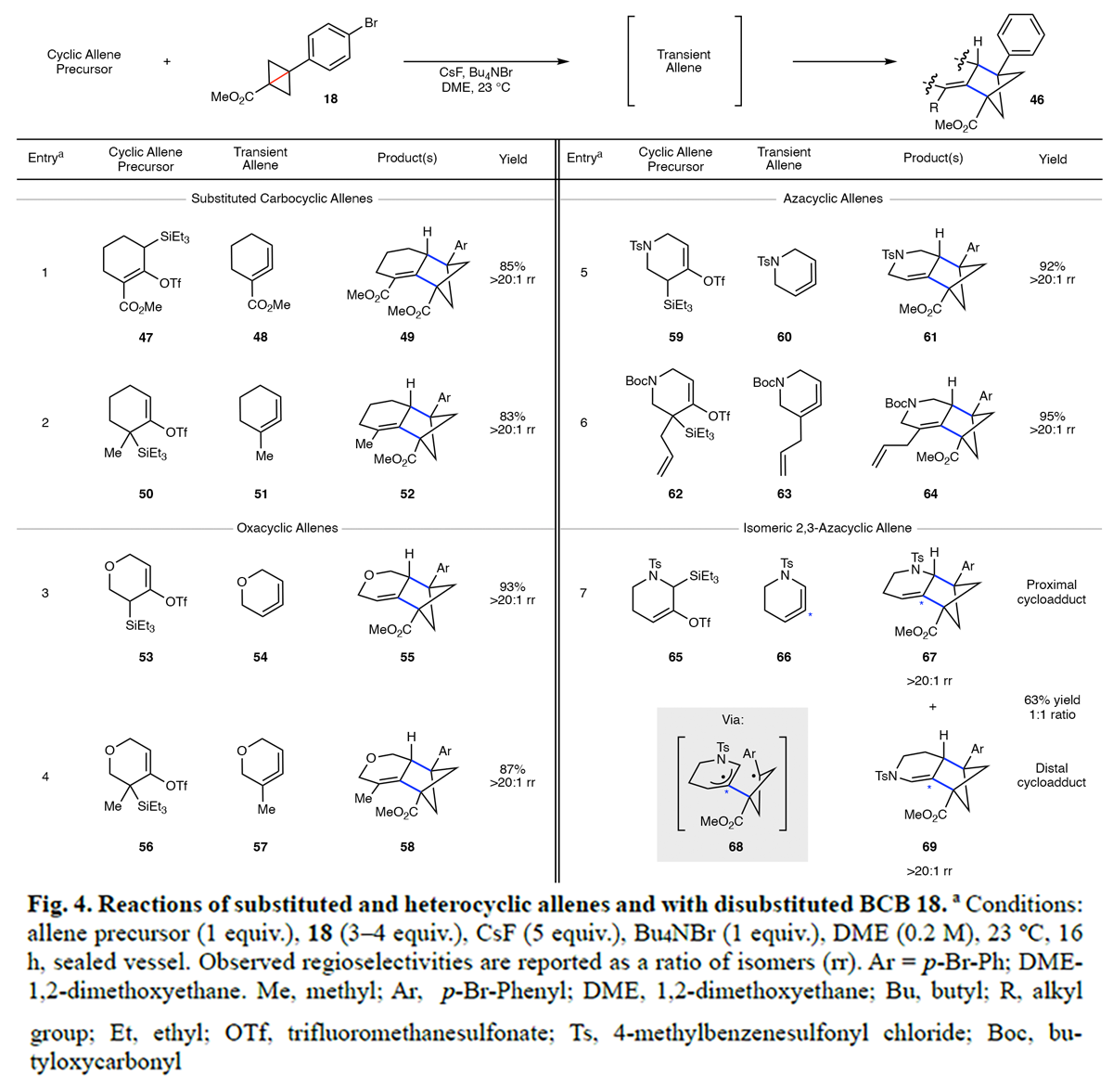
(图片来源:Nature)
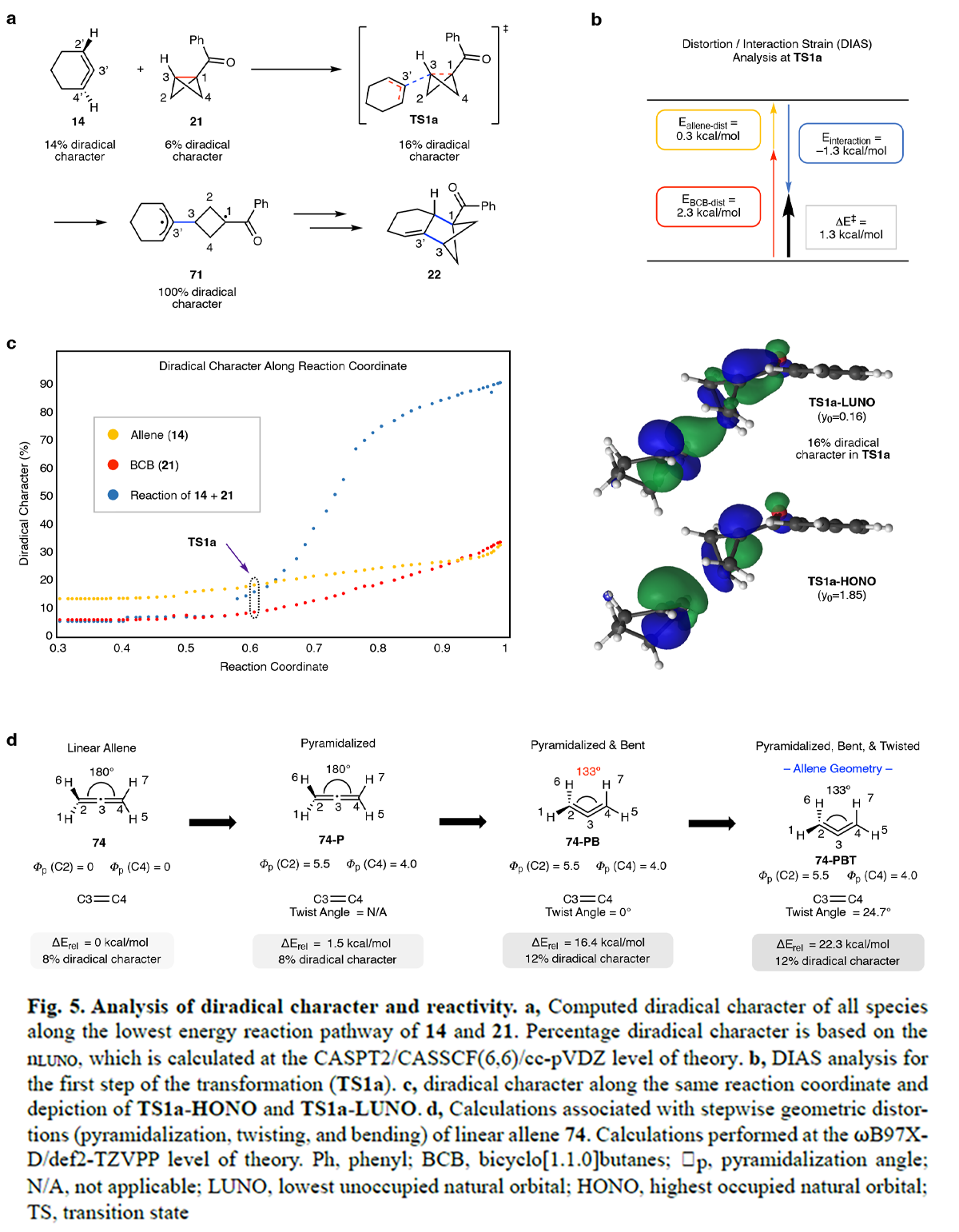
最后,作者通过计算对双自由基特性和活性进行了分析(Fig. 5)。作者对14和21的σ-键插入反应的最低能量路径上的所有物种进行了双自由基特性计算(Fig. 5a)。两种反应物在基态下均显示出显著的双自由基特性(分别为14%和6%)。这种双自由基特性被认为至关重要,因为在此反应条件下,用具有较低双自由基特性的物种替代任一反应物均无法实现有效的偶联(例如,用非活化的联烯或线性联烯替代环状联烯,或用环丙烷或环丁烷替代BCB片段)。作者推测,反应物的双自由基特性有助于后续的低过渡态能垒,其中联烯破坏了张力的σ-键。因此,早期的过渡态TS1a具有16%的双自由基特性。随后的双自由基中间体71则具有100%的双自由基特性。为了进一步分析TS1a的特性,作者使用CASSCF(6,6)/CASPT2/cc-pVDZ单点能量计算对导致片段偶联的反应第一步进行了畸变/相互作用-活化应变(DIAS)分析(Fig. 5b)。由于两种反应物均具有高度张力特性,作者发现形成早期过渡态TS1a所需的畸变能量极低。因此,尽管这一早期过渡态的相互作用能相对较小,但较低的畸变能量贡献了整体较低的动力学能垒(ΔE‡ = 1.3 kcal/mol)。与非畸变的类似物相比,两种反应物显著的双自由基特性降低了π-键(环状联烯)或σ-键(BCB)的键能。此外,作者研究了反应片段14和21双自由基特性的变化,并分别考察了它们单独及共同的变化(Fig. 5c)。与DIAS分析中观察到的低畸变能量一致,环状联烯和BCB片段的双自由基特性在过渡态TS1a之前变化较小,但在过渡态之后随反应进行而迅速增加。底物中的张力诱导了双自由基行为,包括由于低键能导致的低畸变能量。一旦在过渡态中出现了显著的双自由基特性,沿能量表面消除张力能并形成稳定的双自由基结构将不再存在能垒。此外,作者还通过计算得到的HONO和LUNO形状进一步揭示了TS1a的特性。由于TS1a是一个非常早期的过渡态,BCB和环状联烯片段的畸变极小,TS1a的HONO在形状上与BCB和环联烯的双自由基基态的HONO相似。计算得到的TS1a的LUNO显示了中心烯碳与未取代BCB碳之间逐渐增强的σ-键特性。为了更好地理解环状联烯高双自由基特性的起源,作者通过逐步添加金字塔化、弯曲和扭转畸变,系统地将线性联烯74限制为环状联烯的几何结构(Fig. 5d)。总体而言,弯曲是导致环状联烯局部双自由基特性的主要几何畸变。对几何畸变和双自由基特性的这种理解有望为未来设计双自由基反应物提供指导。Neil K. Garg课题组与K. N. Houk课题组联合发展了一种由两类张力化合物参与的片段偶联反应:张力环状联烯(约30 kcal/mol的张力能)和双环[1.1.0]丁烷(约60 kcal/mol的张力能)。尽管两种张力中间体之间的反应并不常见,但这一新转化反应在无外部刺激的条件下于室温高效进行,这归因于每种反应物中存在的显著几何畸变。几何畸变的具体影响体现在两个方面:a)畸变导致每种反应物具有少量的双自由基特性,使其成为能够参与非常规反应的双自由基体;b)反应物的几何畸变使得目标σ-键的插入反应具有较低的动力学能垒,因为反应物在几何结构上已预先向过渡态靠近。此研究提供了一种获取官能化双环[2.1.1]己烷的方法,且这些化合物可以作为芳环生物电子等排体在药物发现中具有重要价值。文献详情:
σ-Bond insertion reactions of two strained diradicaloids.Arismel Tena Meza, Christina A. Rivera, Huiling Shao, Andrew V. Kelleghan, K. N. Houk* & Neil K. Garg*.https://doi.org/10.1038/s41586-025-08745-1
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn