


复杂天然产物(+)-Psiguadial B是由来自暨南大学药学院的长江特聘教授叶文才率领的团队于2010年从传统中药番石榴叶中分离鉴定的,是一种含有二酚结构的萜类化合物。
生物活性研究表明,(+)-Psiguadial B对人肝癌细胞具有强有力的抗增殖活性(HepG2 IC50 = 46 nm),虽然它的生源合成途径也有研究报道,但Reisman团队还是希望发展新的化学来对(+)-Psiguadial B进行全合成。
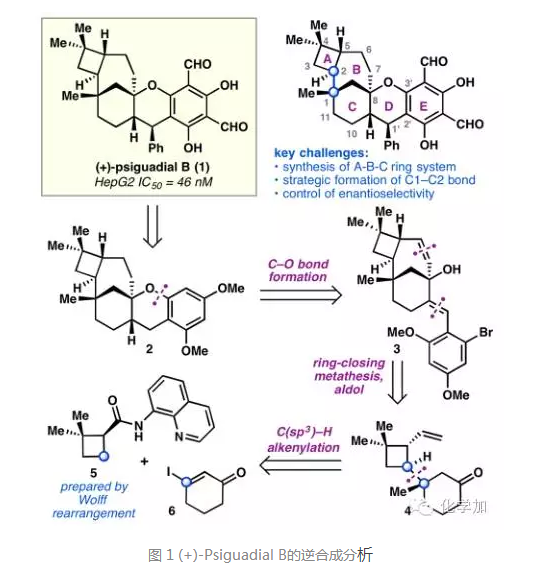
如图1所示,(+)-Psiguadial B具有ABCDE五环结构,其合成挑战在于:1,ABC三环体系的构建,其中A环为带有连续手性中心的四元环,BC环为桥环[4.3.1]骨架;2,C1和C2两个手性碳之间碳碳键的形成;3,分子中其它手性中心的控制。
根据目标分子的结构特点,作者也提出了如下的逆合成分析,首先从D环的碳氧键处切断,逆推至前体化合物3, 3中的桥环结构通过RCM反应来构建,和芳环的连接则通过Aldol反应来完成,这样逆推至化合物4, 4可以由前体化合物5中的四元环直接发生官能团化得到。
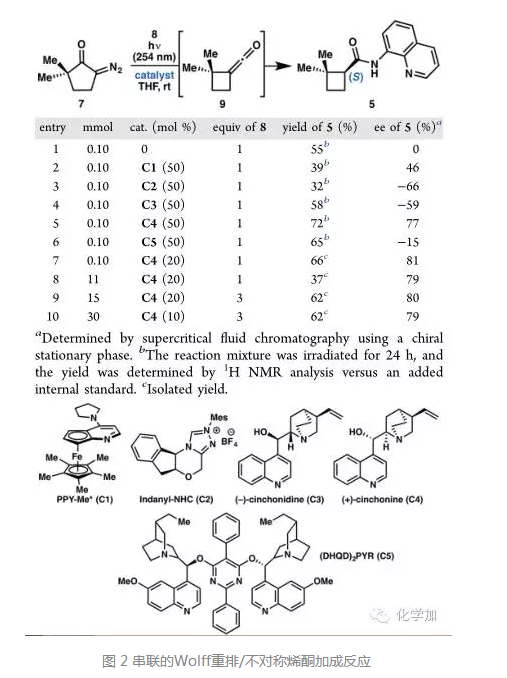
为了不对称地合成重要中间体5,作者发展了首例串联的Wolff重排/不对称烯酮加成反应的方法学。重氮化合物7在254 nm光照下,先发生Wolff重排反应得到含有四元环的烯酮中间体9, 9再在手性胺催化剂的作用下,和化合物8即8-胺基喹啉发生加成反应得到手性化合物5,虽然ee值不高,但经过一次重结晶后,就可以得到光学纯的重要中间体5。这也是一类很重要的构建四元环方法。
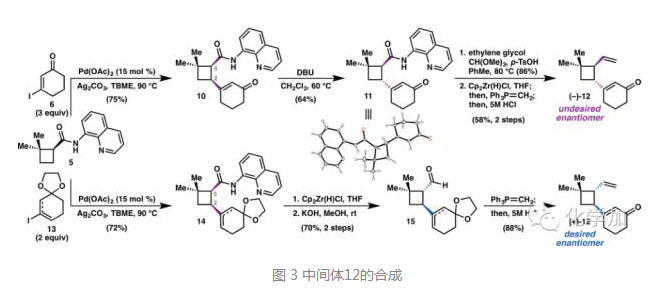
从化合物5出发,先对四元环上的碳氢键直接官能团化,和碘代物6连接后,在DBU作碱的条件下在C2位发生差向异构化,得到化合物11并由单晶确定其结构和立体化学,再将酰胺经两步转化为乙烯基得到光学纯化合物12,但这并不是所期望的对映异构体。而化合物5和化合物13连接后,先把化合物14中的酰胺转化为醛基,进而在C5位差向异构化,得到化合物15,最后Wittig反应把醛基转化为乙烯基,并脱去缩酮保护得到手性纯化合物12,这正是所期望的对映异构体。
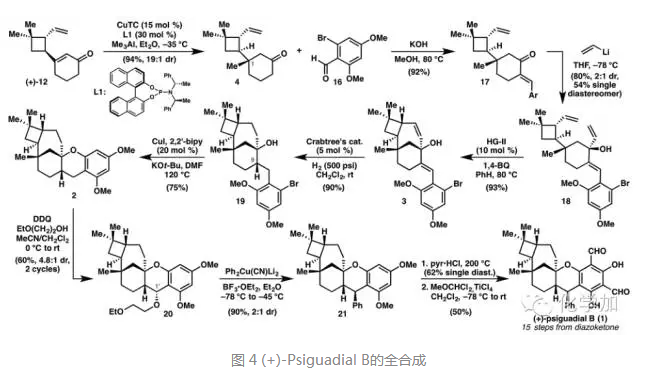
从手性化合物12出发,首先发生不对称Michael反应,以94%的收率和19:1的dr选择性得到化合物4,4再和芳醛化合物16发生缩合反应以92%的收率得到化合物17,乙烯基锂亲核进攻酮羰基,以2:1的选择性得到化合物18, 18在Hoveyda−Grubbs二代催化剂作用下发生RCM反应构建了桥环[4.3.1]结构,氢化拿掉双键得到化合物19,再在铜催化剂作用下发生碳氧键形成,以75%的收率得到化合物2,这样,五个环系均已构建。
接下来只需要装上D环上的苯基取代基和E环上的醛基即可。从化合物2出发,在DDQ和乙氧基乙醇作用下,在苄位引入侧链,再在三氟化硼-乙醚作Lewis酸条件下,和二苯基氰基铜锂试剂经消除再Michael加成得到化合物21,在苄位引入了苯基取代基,产率90%,dr值为2:1。最后,在吡啶盐酸条件下脱去两个甲氧基,再在Rieche条件下引入两个醛基,就完成了天然产物(+)-Psiguadial B的全合成。其核磁数据和分离文献中的完全一致。
总结:Sarah E. Reisman团队从已知的重氮酮化合物出发,经由15步就完成了复杂天然产物(+)-Psiguadial B的首例不对称全合成。其关键步骤包括:作者首次发展的串联Wolff重排/不对称烯酮加成反应构建取代的四元环;钯催化的四元环碳氢键直接官能团化反应等。而且,从同一中间体出发,Psiguadial B的两个对映异构体都可以合成。这也对其它带有四元环天然产物的全合成具有重要的借鉴。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn