

正文
近年来,人们对能够直接官能化芳烃的反应越来越感兴趣,但很少有方法能够在后期交叉偶联的背景下通过C(sp2)-H活化直接形成C(sp2)-C(sp3)键。已有方法通常依赖于烷基卤化物,但烷基卤化物在商业可用性和适用性方面都有限。醇因其广泛的商业可用性、结构多样性和良性性质而被视为理想的合成结构单元(图1A)。经典的Friedel-Crafts烷基化策略使用醇,但通常需要苛刻反应条件和特定的底物,这严重限制了它们的适用性。欢迎下载化学加APP到手机桌面,合成化学产业资源聚合服务平台。
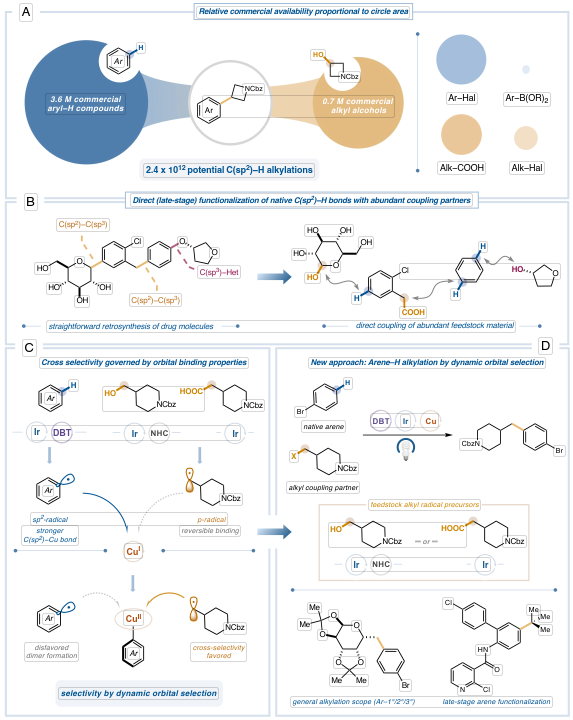
图1. 动态轨道选择的概念化
(图片来源:Nature)
一种强大的通用催化平台,可以通过醇烷基化剂对各种C(sp2)-H键进行功能化,从而扩展烷基-芳基取代模式的化学空间。此外,在后期功能化的背景下,可对结构复杂的分子进行一步式多样化,从而避免了长时间的从头合成(图1B)。基于镍的金属光氧化还原催化策略可形成C(sp2)-C(sp3)键,然而,在复杂的药物骨架中,引入卤化物基团需要改变起始原料或在强制条件下直接安装,这可能是不可行的或以较差的化学选择性和区域选择性进行。
为了应对这一挑战,David W. C. MacMillan教授设想了一个合成平台,通过绕过传统的氧化加成步骤,消除了对预安装功能手柄的需求。受到关于金属中心对不同自由基物种的稳定作用的开创性观察的启发,作者试图通过利用自由基轨道与金属的不同结合特性,进行动态轨道选择,以此作为区分偶联配偶体的手段。具体来说,在Cu(I)催化剂存在下同时生成烷基p自由基和芳基sp2自由基(图1C)。两种自由基及其各自的金属结合状态之间的动态平衡受自由基和金属催化剂之间键解离能差异的支配,可用于实现自由基-自由基偶联中的交叉选择性。为了最大限度地扩大反应平台的范围和模块化,作者寻求使用醇和羧酸作为烷基化剂。使用这两种不同的烷基自由基前体将可对两个不同的关键点进行正交功能化。对于烷基取代的羧酸,设想了铜辅助直接氧化,然后进行不可逆脱羧以生成相应的烷基自由基(图1D)。
为了将本文的方法与传统的Friedel-Crafts 烷基化进行对比,选择氟苯(一种缺电子的芳烃)和Cbz保护的4-羟基哌啶作为偶联配偶体。在优化的条件下,直接添加NHC-OMe-醇加合物I、Cu(I)Cl、Ir[dF(CF3)ppy]2(dtbbpy)PF6、乙酸铯(CsOAc)、四丁基氯化铵(TBACl)、二甲基亚砜(DMSO)和甲基叔丁基醚(MTBE),然后用蓝色发光二极管(LED)照射 2小时,可以高产率形成所需的交叉偶联产物。
添加TBACl显著提高了反应产率,并抑制了由原位形成的Cu(II)物种过度氧化烷基自由基引起的不良烯烃形成。通过自由基捕获研究(包括分子内环化实验和TEMPO加合物形成)检测到了芳基和烷基自由基物种。对照实验进一步支持了铜介导的动态轨道选择途径的存在,DFT计算支持存在由Cu(I)选择性自由基捕获引发的反应网络,从而形成Cu(II)-烷基和Cu(II)-芳基物种。由于键解离能的差异,芳基自由基配位是不可逆过程,而烷基自由基配位是可逆的。高交叉偶联选择性源于溶液中自由芳基自由基的低时间浓度,这是由于它们被Cu(I)无障碍且不可逆地捕获。这最大限度地降低了芳基自偶联的统计可能性。此外,计算揭示了在Cu(II)阶段形成Cu(II)-烷基物种时的二次选择过程。反应倾向于热力学上有利的Cu(III)芳基烷基物种,该物种迅速发生还原消除反应形成交叉偶联产物。因此,铜催化剂会根据自由基的结合特性动态地选择合适的自由基,从而通过引导反应朝向所需的高价Cu(III)芳基烷基物种来控制交叉选择性。
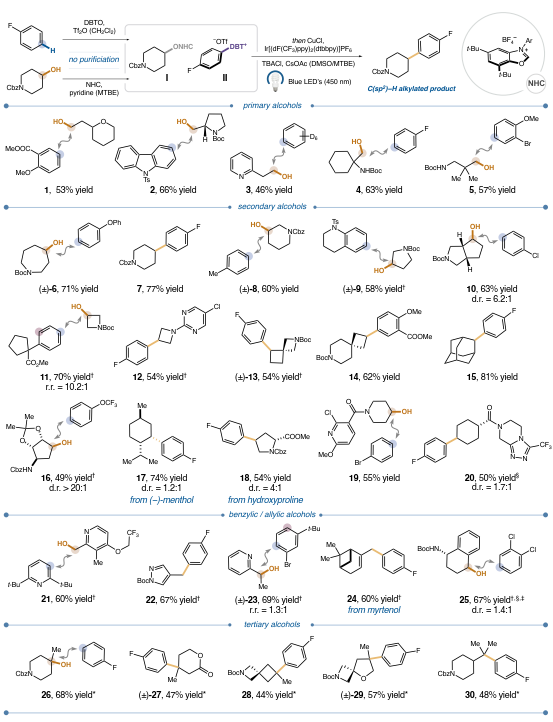
图2. 芳烃和醇反应的底物范围
(图片来源:Nature)
有了最佳条件,作者接下来着手探索芳香烃烷基化策略在醇偶联配偶体方面的应用范围(图2)。一系列具有不同电子和空间性质的一级醇与(杂)芳烃有效地进行了自由基-自由基交叉偶联,以46-67% 产率生成相应的产物。该反应在β-位上可以兼容各种不同的取代模式,包括具有新戊基取代模式的二级(1-3)、三级(4)甚至季碳中心(5)。多种含有环结构的复杂二级醇都是合适的烷基化剂,可以以良好至极好的产率生成交叉偶联产物。此外,带有Boc保护胺的螺环醇(13和 14)的偶联产率分别为54%和62%,而这些胺很难进行传统的Friedel-Crafts烷基化或酰化反应。空间位阻的2-金刚烷醇也可以成功偶联,以81%的产率生成相应的交叉偶联产物。含有高度不稳定的缩醛保护基的核苷类似物在本文的方案中充当了有效的偶联配偶体。此外,天然存在的醇类,如(-)-薄荷醇和天然醇类衍生物,如羟脯氨酸甲酯都是可行的偶联剂,可以高产率生成所需产物。更复杂的取代六元环系统,包括吡啶和三唑哌嗪,可以转化为相应的产物,产率分别为55%和50%。一系列苄醇和烯丙基醇是交叉偶联反应中的可行底物,可有效与苯基芳烃或空间位阻吡啶偶联,以60-67%产率生成所需产物。将CsOAc换成四丁基苯甲酸铵(TBAOBz),并使用专门用于活化叔醇的 NHC试剂(NHC-CF3)变体,可以44-68%产率得到含有季碳的偶联产物,适用于各种叔醇,包括环状、螺环和非环状底物。作者采用组合方法探索了芳烃偶联剂的范围。多种具有各种(杂环)取代模式和电子特征的市售或易得芳烃成功地与不同取代的醇偶联。含卤素的芳烃是有效的偶联剂,反应条件保留了这些宝贵的功能性手柄,可用于进一步的下游操作。
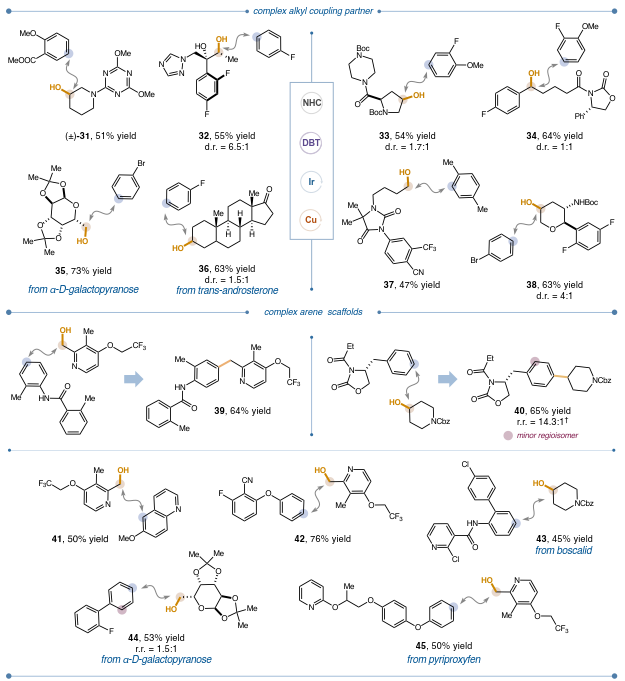
图3. 复杂醇和杂芳基化合物的偶联
(图片来源:Nature)
接下来,将动态轨道选择平台应用于更复杂的醇,特别是那些源自天然存在的生物分子和药理活性化合物中常见的骨架的醇(图3)。作者成功地用一系列复杂的烷基自由基捕获了各种芳基自由基,包括三嗪 31(产率为 51%)和1,2-二醇,如从efinaconazole衍生的二醇合成32(产率为 55%)。在这个例子中,由于NHC 试剂的特殊区域选择性,只有二级醇被活化,而三级醇不受影响,可以进一步功能化。
氨基酸衍生的复合醇也是极好的偶联配偶体,如羟脯氨酸衍生物33(产率54%)和噁唑烷酮34(产率64%),它们为Boc保护的氮原子进一步偶联提供了潜力。此外,利用了生物分子(包括糖和类固醇)作为烷基自由基来源,生成了半乳糖吡喃糖衍生物和雄酮衍生物。抗雄激素衍生物和四氢吡喃的产率分别为 48% 和 63%。这种自由基-自由基交叉偶联方法的一个关键优势是使用天然且普遍存在的C(sp2)-H 键,而无需底物预官能化。通常,DBTO活化的区域选择性由空间因素和芳环的电子密度决定。特别是在带有电子给体杂原子(如氮或氧)的(杂)芳族系统中,观察到了出色的区域选择性,并且以高产率获得了相应的烷基化产物(产率50-76%)。在中性芳烃的情况下,观察到邻位和对位产物,且对位产物更受青睐。对于不能使用既定方法引入卤素原子的复合骨架,啶酰菌胺(43)和吡丙醚(45)都以优异的区域选择性进行了功能化,分别以45% 和50% 的产率得到了相应的产物。
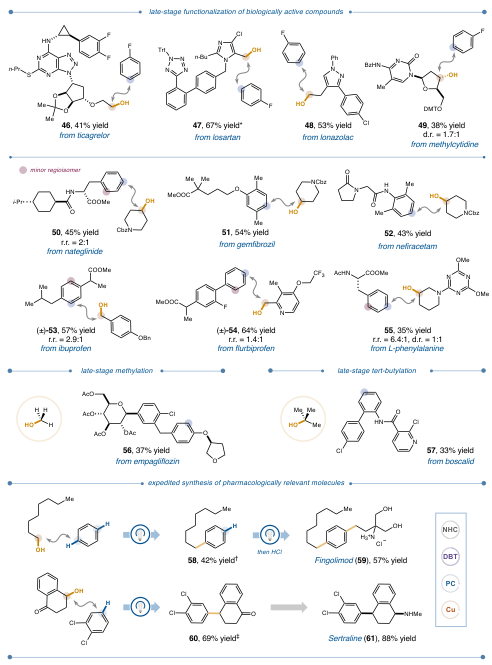
图4. 药物分子的后期功能化
(图片来源:Nature)
作者还将本文的方法应用于药物分子和其他生物活性化合物的后期功能化(图4)。多种含醇药物,包括替格瑞洛(46)、氯沙坦(47)和氯那唑酸(48),与氟苯进行了自由基-自由基交叉偶联,获得了良好至合成有用产率的产物。对于氯沙坦(47),反应的可扩展性通过在单个反应装置中成功生成1.24克交叉偶联产物得到证明。将本文的方法应用于5-甲基-2'-脱氧胞苷的功能化,得到3'-芳基化产物49,产率为 38%,非对映异构体比为1.7:1。在一系列结构差异化的含芳烃药物分子上对本文的系统进行了基准测试,包括那格列奈(50)、吉非贝齐(51)、奈非西坦(52)、布洛芬(53)和氟比洛芬(54)。在所有情况下,与各种醇类进行交叉偶联可获得45-64%的所需产物,且不会影响药物分子的结构完整性。从l-苯丙氨酸产生的芳基自由基很容易进行交叉偶联,生成非天然氨基酸55(产率为35%),为快速合成具有不同取代部分和模式(邻位与对位)的苯丙氨酸衍生非天然氨基酸库提供了可能性。
使用甲醇作为安全、无害的甲基自由基源,以完全区域选择性在2型糖尿病药物恩帕列净(56,产率为37%)上安装了甲基。使用本文的叔醇反应方案,获得了叔丁基化的啶酰菌胺57,其合成产率为33%,并且完全控制了区域选择性。本文的动态轨道选择策略使芬戈莫德(59)从苯通过正辛基苯(58)中间体,总共两步,每步平均产率为50%。该路线显著缩短了合成序列,无需额外的氧化还原相互转化或使用危险化学品和加压反应器。
为了进一步评估动态轨道选择在药物合成中的适用性,将本文的系统与工业应用的Friedel-Crafts烷基化反应进行比较。本文的方案使用市售的起始原料以69%的产率生成60,随后对酮进行还原胺化,以88%的产率生成舍曲林(61)。
作者之前已证明,羧酸可通过金属光氧化还原途径转化为烷基自由基,该途径涉及用铜(II)物种捕获烷基自由基。使用CuCN与对甲苯基三联吡啶配体,通过可能的中间体III(图 5),成功实现了各种羧酸与不同芳烃的自由基-自由基交叉偶联。对一级以及三级羧酸进行了动态轨道选择,产率52-83%。此外,在这些条件下,一系列生物活性药物分子进行了后期功能化,包括萘普生(65,产率 70%)、氟比洛芬(66,产率 69%)、托美丁(67,产率 48%)、卡洛芬(68,产率 42%)和吲哚美辛(69,产率 53%)。
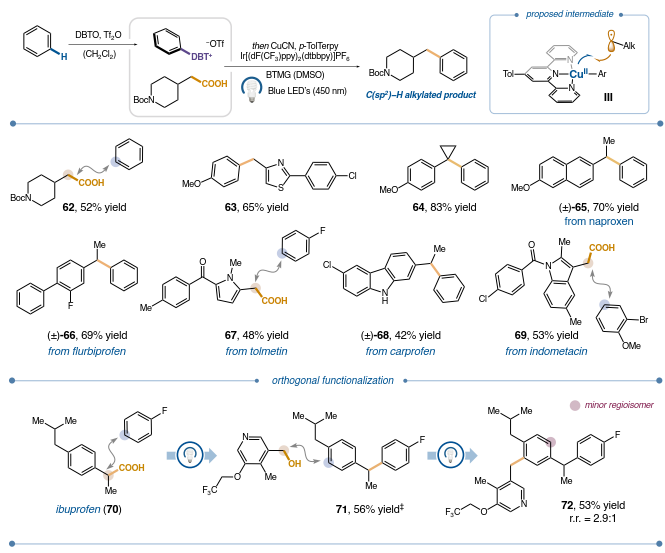
图5. 芳烃和羧酸的偶联及正交功能化
(图片来源:Nature)
最后,作者通过顺序酸-芳基和醇-芳基自由基-自由基交叉偶联来展示后期正交功能化的潜力。使用布洛芬(70)作为模型化合物,首先将相应的烷基自由基与氟苯交叉偶联,以56%的产率生成71。随后用DBTO和Tf₂O处理,然后暴露于醇动态轨道选择方案,导致更富含电子的二烷基化芳烃(72,产率53%)优先于氟化芳环进行烷基化。这一结果突出了功能化策略的正交性,并展示了模块化操纵现有药物骨架的潜力,从而获得新的化学空间和更复杂的结构。
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn